フォルダマー
化学において、 フォルダマー(foldamer)とは、不連続な鎖状分子、または溶液中で立体構造的に秩序立った状態で折りたたまれているオリゴマーである。 タンパク質、核酸、多糖類に見られる α ヘリックスや β シート、二重螺旋などのような特定の構造に折りたたまれる能力を模倣した人工分子を指す。 フォルダマーの構造は、隣接していない モノマー間の非共有結合性相互作用により安定化されている[2] 。予測可能な構造をもつ巨大分子を設計することが、フォルダマーの研究の主な目標である。フォルダマーの研究は、分子の自己組織化、分子認識、ホスト-ゲスト化学のテーマとも関連している。
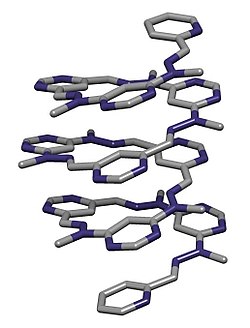
分子設計 編集
フォルダマーのサイズは様々であるが、非共有結合性で隣接しない相互作用の存在によって、その大きさは決められている。 ポリウレタンや ポリ(プロリン) のように「隣接する」繰り返し単位間の共有結合性相互作用により確実にらせん状に折りたたまれる分子は、フォルダマーには含まれない[3][4]。フォルダマーは、大きな巨視的な折りたたみがまず疎溶媒性効果(疎水性凝集)により引き起こされ、最終的な折り畳み構造のエネルギーは非共有性相互作用により安定化されるという動的な折りたたみ過程をとる。これらの相互作用は、協奏的に作用することで最も安定な三次元構造を形成し、完全に折りたたまれた、あるいは完全に展開した状態は、部分的に折りたたまれたどのような状態よりも安定である[5]。
折りたたみの予測 編集
フォルダマーの構造は、しばしばその一次配列から予測できる。 この予測プロセスには様々な条件下の原子レベルでの折りたたみ平衡構造の動的シミュレーションが伴う。 この種のシミュレーションによる分析手法は、タンパク質の一次構造が特に短い部類、つまり、タンパク質を構成するアミノ酸の数が比較的少ない物には適用できるものの、そうでないタンパク質に対しては、2007年現在、コンピュータの処理能力などの技術的な問題のために不可能である[6]。
フォルダマーの折りたたみ経路は、様々な熱力学的および速度論的条件の下で、実験的に決定された好ましい構造からの変化を測定することによって、決定することができる。その構造の変化は、好ましい構造の骨格原子位置から二乗平均平方根偏差を計算することによって測定される。様々な条件下でのフォルダマーの構造は、計算的に決定され、次いで実験的に検証され得る。 温度、溶媒粘度、圧力、pH、および塩濃度を変化させることで、フォルダマーの構造に関する非常に有益な情報を得ることができる。 折りたたみの動力学および折りたたみの平衡を測定することにより、これらの様々な条件がフォルダマー構造に及ぼす影響を観察することができる。
溶媒は折りたたみにしばしば影響する。 例えば、疎水性の崩壊を伴う折りたたみの経路は、非極性溶媒中では全く違った結果となる。この違いは、異なる溶媒では、折りたたみ経路の異なる中間体が安定化されるという事実に起因している、これは分子間の非共有結合性相互作用に基づく最終的なフォルダマー構造が、溶媒により異なっていることと同様である。
非共有性の相互作用 編集
非共有性の分子間相互作用は、個々の作用は小さいものの、その力が合わさることで、化学反応の主な道筋を決めている。以下に示した一般的な分子間力が、化学者がフォルダマーを設計する際に利用されている。
- 水素結合 (特に ペプチド結合)
- π(パイ)スタッキング
- 疎水性崩壊につながる疎溶媒効果
- ファンデルワールス力
- 静電引力
一般的な分子設計 編集
フォルダマーは3種の異なったカテゴリーに分けられる、すなわち、ペプチド模倣型フォルダマー、核酸模倣型フォルダマー、非生物型フォルダマーである。 ペプチド模倣型フォルダマーはタンパク質の構造に似せた合成分子であり、核酸模倣型フォルダマーは核酸の相互作用に基づくものである。非生物型のフォルダマーは一般的に自然界には見られない芳香族や電荷移動相互作用により安定化されているタイプである[7] 。以下に示したフォルダマーの3つの分子設計タイプは、ヒルら のいう厳密なフォルダマーの定義からは外れているものもある、彼らは、らせん型はフォルダマーから除外している。
ペプチド模倣型 編集
ペプチド模倣型フォルダマーは、らせん構造を示すことが多いので、前述のフォルダマーの定義に当てはまらないことが多い。 ただ、らせん構造を示すフォルダマーは、その設計と能力のためフォルダマー研究の主要な歴史的画期となっている[8][9] 。ペプチド模倣型の最大のグループは、β- ペプチド、γ–ペプチド、δ–ペプチド、および可能なモノマーの組み合わせからなっている 。これらのペプチドのアミノ酸は、メチレン炭素の数が1個(β)、2個(γ)または3個(δ)異なるだけだが、その構造変化は極めて大きい。 これらのペプチド配列は、折りたたみを信頼性良く予測できる配列の制御として、非常に良く研究されている。さらに、隣接するペプチド結合のカルボキシル末端とアミノ末端との間に複数のメチレン炭素を有する場合、いろいろなR基側鎖を設計することができる。 一例として、Reiserらにより見出された新規なβ-ペプチドが挙げられる[10] 。彼らは、α-アミノ酸およびcis-β-アミノシクロプロパンカルボン酸(cis-β-ACC)からなるヘテロオリゴペプチドを用いて、そのオリゴマー中の7残基という短い配列にらせん構造を見出し、また5残基に明瞭な立体構造を見出した、それらの構造は環状β-アミノ酸を含有するペプチドに特有の性質である[11][12]。
核酸模倣型 編集
核酸模倣型は、一般的にフォルダマーとしては適当ではない。その大部分は、DNAを非特異的に標的とするために、単一のDNA塩基、ヌクレオシド、またはヌクレオチドを模倣するように設計されている[13][14][15] 。これらは、抗癌、抗ウイルスおよび抗真菌用途を含むいくつかの異なる医薬用途に利用される。 しかし、いくつかの核酸模倣型はフォルダマーの性質を持っている。 例えば、アンチセンス技術は、細胞中のDNAまたはmRNAの特定配列を標的とする[16] 。これらの分子は、DNAと同様な方法で一緒に結びつけられた種々の異なるヌクレオチド類似体から、一般に構成されている。 この種の分子は、一本鎖RNAと同様のやり方で、溶液中において個別に折りたたまれる。
非生物型 編集
非生物型のフォルダマーは、動的な折りたたみを示すように設計された有機分子である。 それらは、設計により最適化されたように、1つまたはいくつかの既知の重要な分子間相互作用を利用する。 一例がピロール誘導体の1種のオリゴピロール(Oligopyrrole)である、この分子は水素結合を通して、例えば塩素イオンのようなアニオンと配位結合する(図参照)。 アニオンの存在が折りたたみを誘起し、ポリピロール基は、ほかに取りようのない立体構造に制限される[17][18]。
ほかの例 編集
- m-フェニレンエチレンオリゴマーは、疎溶媒力と芳香族スタッキング相互作用により、らせん構造に折りたたまれる。
- β-ペプチド は、アミンとカルボン酸の間に CH2 ユニットが追加されたアミノ酸からなっている 。その構造は酵素分解に対し安定であり、抗菌能力をもつことが実証されている。
- ペプトイドは N-置換ポリグリシンであり、立体相互作用を利用することで、ポリプロリンのタイプ-Iのようならせん構造に折りたたまれている。
- Aedamers は、疎水性と芳香族スタッキング相互作用により、水溶液中で折りたたまれている。
- 芳香族オリゴマー状フォルダマー、これらは最も大きく、また最もよく構造的に特徴的フォルダマーの例である[19]。
- アリールアミドフォルダマー[20] 、例えばブリラシジン(Brilacidin)
参考文献 編集
- ^ Lehn, Jean-Marie et al. (2003). “Helicity-Encoded Molecular Strands: Efficient Access by the Hydrazone Route and Structural Features”. Helv. Chim. Acta. 86: 1598–1624. doi:10.1002/hlca.200390137.
- ^ “A field guide to foldamers”. Chem. Rev. 101 (12): 3893–4012. (2001). doi:10.1021/cr990120t. PMID 11740924.
- ^ Hill, David (2001). “A Field Guide to Foldamers”. Chem. Rev. 101: 3893–4011. doi:10.1021/cr990120t. PMID 11740924.
- ^ Green, M. M.;; Park, J.; Sato, T.; Teramoto, A.; Lifson, S.; Selinger, R.L.B.; Selinger, J.V. (1999). “The Macromolecular Route to Chiral Amplification”. Agnew. Chem. Int. Ed. 38: 3138–3154. doi:10.1002/(SICI)1521-3773(19991102)38:21<3138::AID-ANIE3138>3.0.CO;2-C.
- ^ Gellman, S.H. (1998). “Foldamers: A Manifesto”. Acc. Chem. Res. 31: 173–180. doi:10.1021/ar960298r.
- ^ van Gunsteren, Wilfred F. (2007). Foldamers: Structure, Properties, and Applications; Simulation of Folding Equilibria. Wiley-VCH Verlag GmbH & Co. KGaA. pp. 173–192. doi:10.1002/9783527611478.ch6
- ^ Foldamers: Structure, Properties, and Applications" Stefan Hecht, Ivan Huc Eds.
- ^ Anslyn and Dougherty, Modern Physical Organic Chemistry, University Science Books, 2006, ISBN 978-1-891389-31-3
- ^ Martinek, T.A.; Fulop, F. (2012). “Peptidic foldamers: ramping up diversity”. Chem. Soc. Rev. 41: 687–702. doi:10.1039/C1CS15097A.
- ^ De Pol, S.; Zorn, C.; Klein, C.D.; Zerbe, O.; Reiser, O. (2004). “Surprisingly Stable Helical Conformations in alpha/beta-Peptides by Incorporation of cis-beta-Aminocyclopropate Carboxylic Acids”. Angew. Chem. Int. Ed. 43: 511–514. doi:10.1002/anie.200352267.
- ^ Seebach, D.; Beck, A.K.; Bierbaum, D. J.; Chem.
- ^ Seebach, D.; Beck, A.K.; Bierbaum, D.J. (2004). “Chemical and Biological Investigations of B-Oligoarginines”. Chem. Biodiv. 1: 1111–1239. doi:10.1002/cbdv.200490014.
- ^ Longley, DB; Harkin DP; Johnston PG (May 2003). “5-fluorouracil: mechanisms of action and clinical strategies”. Nat. Rev. Cancer 3 (5): 330–338. doi:10.1038/nrc1074. PMID 12724731.
- ^ Secrist, John (2005). “Nucleosides as anticancer agents: from concept to the clinic”. Oxford Journals 49: 15–16. doi:10.1093/nass/49.1.15.
- ^ Rapaport, E.; Fontaine J (1989). “Anticancer activities of adenine nucleotides in mice are mediated through expansion of erythrocyte ATP pools”. Proc. Natl. Acad. Sci. USA 86: 1662–1666. doi:10.1073/pnas.86.5.1662.
- ^ Gupta, S.; Singh, R.; Rabadia, N.; Patel, G.; Panchal, H. (2011). “Antisense Technology”. Int. J. Pharm. Sci. Rev. Res. 9 (2): 38–45.
- ^ Sessler, J.L.; Cyr, M.; Lynch, V. (1990). “Synthetic and structural studies of sapphyrin, a 22-.pi.-electron pentapyrrolic "expanded porphyrin"”. J. Am. Chem. 112: 2810. doi:10.1021/ja00163a059.
- ^ Juwarker, H.; Jeong, K-S. (2010). “Anion-controlled foldamers”. Chem. Soc. Rev. 39: 3664–3674. doi:10.1039/b926162c.
- ^ Huc, I.; Delsuc, N.; Massip, S.; Léger, J-M..; Kauffmann, B. http://pubs.acs.org/doi/abs/10.1021/ja110677a
- ^ De novo design and in vivo activity of conformationally restrained antimicrobial arylamide foldamers.
さらに詳しく知るための資料 編集
- Ivan Huc; Stefan Hecht (2007). Foldamers: Structure, Properties, and Applications. Weinheim: Wiley-VCH. ISBN 3-527-31563-2
- “Foldamers as versatile frameworks for the design and evolution of function”. Nat. Chem. Biol. 3 (5): 252–62. (2007). doi:10.1038/nchembio876. PMID 17438550.
レビュー 編集
- ^ Gellman, S.H. (1998). “Foldamers: a manifesto” (PDF). Acc. Chem. Res. 31 (4): 173–180. doi:10.1021/ar960298r.
- ^ “Aromatic Amide Foldamers: Structures, Properties, and Functions”. Chem. Rev. 112 (10): 5271–5316. (2012). doi:10.1021/cr300116k. PMID 22871167.
- ^ Juwarker, H. (2010). “Anion-controlled foldamers”. Chem. Soc. Rev. 39: 3664–3674. doi:10.1039/b926162c.