フムレン
フムレン(Humulene)は、天然に存在する単環式セスキテルペンである。α-フムレンまたはα-カリオフィレン(α-caryophyllene)とも呼ばれる。
| フムレン | |
|---|---|
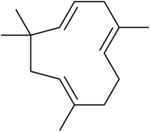
| |

| |
2,6,6,9-Tetramethyl-1,4-8-cycloundecatriene | |
別称 alpha-Caryophyllene; 3,7,10-Humulatriene | |
| 識別情報 | |
| CAS登録番号 | 6753-98-6 |
| PubChem | 5281520 |
| ChemSpider | 4444853 |
| ChEBI | |
| ChEMBL | CHEMBL251280 |
| |
| |
| 特性[1] | |
| 化学式 | C15H24 |
| モル質量 | 204.35 g mol−1 |
| 外観 | 淡黄緑色透明液体 |
| 密度 | 0.886 g/cm3 |
| 沸点 |
106-107 °C at 5 mmHg |
| 危険性 | |
| 安全データシート(外部リンク) | MSDS |
| 半数致死量 LD50 | >48 mg/kg |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ホップ(Humulus lupulus)の精油から発見されたため、この名前が付けられた[2]。β-カリオフィレンの異性体であり、この2つの化合物は、天然ではしばしば混合物として見られる。テンダイウヤク(Lindera aggregata)にも含まれ、またベトナムコリアンダー(Persicaria odorata)のスパイス風味、ホップやアサの香りを与えている。
合成 編集
フムレンは、ファルネシルピロリン酸に由来する多くのセスキテルペンの1つである。生合成は、セスキテルペンシンターゼの作用によって、ファルネシルピロリン酸からピロリン酸基が外れ、分子内アタックを受けやすいアリルカチオンが生じるところから始まる[3]。
この生合成は、研究室でも模倣することができ、Corey合成と呼ばれる。大員環の異なる位置のC-C結合で閉じる合成法もある。McMurry合成では、チタン触媒のカルボニルカップリング反応が用いられる。Takahashi合成では、シアノヒドリンアニオンによるハロゲン化アリルの分子内アルキル化が用いられる。Suginome合成では、ゲラニル基が用いられ、de Groot合成では、ユーカリ油の粗蒸留物からフムレンが合成される[4]。また、下記のように4つの部分を組み合わせてパラジウム触媒で環化させて作ることもできる。この合成は、C-C結合の形成と環化が単純で、関連ポリテルペノイドの合成にも有効であると考えられている[5]。
天然 編集
フムレンは、ホップの毬花で作られる精油の成分の1つである。フムレンの濃度は、植物の品種によって異なる。フムレンやビールの醸造過程におけるその反応生成物は、多くのビールにホップの香りを与えている。ノーブルホップは、フムレンを高濃度で含む品種であるが、その他の苦いホップの品種は、フムレンをあまり含まない[6][信頼性要検証]。ビールの醸造の過程では、多数のフムレンのエポキシドが生成される。GC/MSや官能パネルによる分析によって、フムレンエポキシドIIの加水分解物は、特にビールにホップの香りを与えていることが明らかとなった[7][8]。
生理効果 編集
フムレンは抗炎症作用を持つことが知られており、炎症性疾患の治療に効果がある可能性がある。デキサメタゾンと同様の効果を持ち、ヒスタミン注射による浮腫の形成を抑える働きが知られている。フムレンはまた、カラギーナンを注射したラットにおいて、TNFαやIL-1βの発生を阻害する重要な効果を持つ[9]。
出典 編集
- ^ Merck Index, 12th Edition, 4789
- ^ Glenn Tinseth, "Hop Aroma and Flavor", January/February 1993, Brewing Techniques. <http://realbeer.com/hops/aroma.html> Accessed July 21, 2010
- ^ Moss, G.P., “Humulene derived sesquiterpenoid biosynthesis.” International Union of Biochemistry and Molecular Biology Enzyme Nomenclature. Accessed April 10, 2011. http://www.enzyme-database.org/reaction/terp/humul.html
- ^ Goldsmith, David. "The total synthesis of natural products". Canada: John Wiley & Sons. 1997 pp 129-133
- ^ Hu, Tao & Corey, E.J. (2002). “Short Syntheses of (±)-δ-Araneosene and Humulene Utilizing a Combination of Four-Component Assembly and Palladium-Mediated Cyclization”. Organic Letters 4 (14): 2441-2443. doi:10.1021/ol026205p. PMID 12098267.
- ^ http://www.homebrewtalk.com/wiki/index.php/Humulene#Humulene
- ^ Yange, Xiaogen; Lederer, Cindy; McDaniel, Mina & Deinzer, Max. (1993). “Evaluation of hydrolysis products of humulene epoxides II and III”. Journal of Agricultural and Food Chemistry 41 (8): 1300-1304. doi:10.1021/jf00032a026.
- ^ Peackock, Val & Deinzer, Max (1981). “Chemistry of hop aroma in beer”. Journal of the American Society of Brewing Chemists 39.
- ^ Fernandes E.S., Passos G.F., Medeiros R., da Cunha F.M., Ferreira J., Campos M.M., Pianowski L.F., Calixto J.B. (2007). “Anti-inflammatory effects of compounds alpha-humulene and (-)-trans-caryophyllene isolated from the essential oil of Cordia verbenacea”. European Journal of Pharmacology 569 (3): 228-236. doi:10.1016/j.ejphar.2007.04.059. PMID 17559833.