酸化銀(I)
酸化銀(I) は化学式Ag2Oで表される銀化合物の一つ。黒から褐色の細かい粉末で、他の銀化合物の調製に用いられる。
| 酸化銀(I) | |
|---|---|
| |

| |
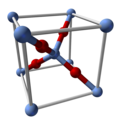
Silver(I) oxide | |
別称 Silver rust, Argentous oxide, Silver monoxide | |
| 識別情報 | |
| CAS登録番号 | 20667-12-3 |
| PubChem | 9794626 |
| ChemSpider | 7970393 |
| EC番号 | 243-957-1 |
| MeSH | silver+oxide |
| RTECS番号 | VW4900000 |
| |
| |
| 特性 | |
| 化学式 | Ag2O |
| モル質量 | 231.74 g mol−1 |
| 外観 | 黒から褐色の固体 |
| 匂い | 無臭[1] |
| 密度 | 7.14 g/cm3 |
| 融点 | |
| 水への溶解度 | 0.013 g/L (20℃) 0.025 g/L (25℃)[2] 0.053 g/L (80 °C)[3] |
| 溶解度平衡 Ksp(AgOH) | 1.52·10−8 (20℃) |
| 溶解度 | 酸、塩基に可溶 エタノールに不溶[2] |
| 構造 | |
| 結晶構造 | 立方晶系 |
| 熱化学 | |
| 標準生成熱 ΔfH |
−31 kJ/mol[5] |
| 標準モルエントロピー S |
122 J/mol·K[5] |
| 標準定圧モル比熱, Cp |
65.9 J/mol·K[2] |
| 危険性 | |
| 安全データシート(外部リンク) | Material Safety Data Sheet |
| GHSピクトグラム |   [6] [6] |
| GHSシグナルワード | 危険(DANGER) |
| Hフレーズ | H272, H315, H319, H335[6] |
| Pフレーズ | P220, P261, P305+351+338[6] |
| EU分類 | |
| NFPA 704 | |
| Rフレーズ | R36/37/38 |
| Sフレーズ | S17, S26, S36 |
| 半数致死量 LD50 | 2.82 g/kg (ラット、経口)[1] |
| 関連する物質 | |
| 関連物質 | 一酸化銀 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
合成 編集
銀イオン Ag+ を含む水溶液に水酸化物イオン OH− を含む物質を加えることで沈殿として得られる。具体的には、硝酸銀とアルカリ金属水酸化物等を用いて合成できる[7]。この反応では水酸化銀が生成するが、これはすぐに分解して酸化銀(I)と水になる[8]。
構造と性質 編集
酸化銅(I)と同一の結晶構造を持つ。このために、化学反応によるものを除いてはあらゆる溶媒にほぼ不溶となっていると考えられる[10]。水にはAg(OH2)−
2のような加水分解産物を生成してごくわずかに溶ける[11]。
Ag2O懸濁液は次のように酸と反応する。
アルカリ塩化物水溶液と反応すると、対応するアルカリ水酸化物と塩化銀(I)が生成する[12][11]。
アンモニア NH3、チオ硫酸イオン S2O2−
3 の水溶液には以下のように反応し溶解する。それぞれジアンミン銀(I)イオン、ビス(チオスルファト)銀(I)酸イオンといった錯イオンを生じる。
多くの銀化合物と同様に感光性である。また、280℃以上では銀と酸素に分解する[10]。
利用 編集
有機化学では温和な酸化剤として利用され、例えばアルデヒドのカルボン酸への酸化に用いられる[13]。この場合は、硝酸銀とアルカリ水酸化物によってin situ で調製されることが多い。また、一酸化銀 Ag4O4と同様に酸化銀電池に用いられる。
微細な電子回路の製造時に導電性材料として銀粉が用いられることがあるが、より粉末化の容易な酸化銀を用いて、加熱することで導電性の銀に変換する手法が開発されている[14]。
脚注 編集
- ^ a b “Silver Oxide MSDS”. http://www.saltlakemetals.com. Salt Lake Metals. 2014年6月8日閲覧。
- ^ a b c Lide, David R. (1998). Handbook of Chemistry and Physics (87 ed.). Boca Raton, FL: CRC Press. pp. 4–83. ISBN 0-8493-0594-2
- ^ a b Perry, Dale L. (1995). Handbook of Inorganic Compounds (illustrated ed.). CRC Press. pp. 354. ISBN 0849386713
- ^ http://chemister.ru/Database/properties-en.php?dbid=1&id=4098
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. p. A23. ISBN 0-618-94690-X
- ^ a b c Sigma-Aldrich Co., Silver(I) oxide. 2014年6月7日閲覧。
- ^ Janssen, D. E.; Wilson, C. V. (1963). "4-Iodoveratrole". Organic Syntheses (英語).; Collective Volume, vol. 4, p. 547
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ^ Biedermann, George; Sillén, Lars Gunnar (1960). “Studies on the Hydrolysis of Metal Ions. Part 30. A Critical Survey of the Solubility Equilibria of Ag2O”. Acta Chemica Scandinavica 14: 717. doi:10.3891/acta.chem.scand.14-0717.
- ^ a b Merck Index of Chemicals and Drugs, 14th ed. monograph 8521
- ^ a b Cotton, F. Albert; Wilkinson, Geoffrey (1966). Advanced Inorganic Chemistry (2nd Ed.). New York:Interscience. p. 1042
- ^ General Chemistry by Linus Pauling, 1970 Dover ed. p703-704
- ^ “Oxidation of Aldehydes to Carboxylic Acids”. 2015年4月6日閲覧。
- ^ Replacement for silver powder as electroconductive paste filler; controlling particle sizes; neutralization aqueous solution containing sodium hydroxide, potassium hydroxide; filtration of precipitate 2015年4月6日閲覧。
関連項目 編集
外部リンク 編集
- Annealing of Silver Oxide Demonstration experiment: Instruction and video
- Silver Oxide, Ag2O
