アイソタイプ (免疫学)
免疫学では、抗体(免疫グロブリン(Ig))はアイソタイプ(isotype)またはクラス(class)と呼ばれるいくつかの種類に分類される。抗体の先端付近にある可変(V)領域は分子ごとに無数の違いがあり、それによって抗原(より正確にはエピトープ)を特異的に標的にすることができる。一方、定常(C)領域は幾つかの変異のみ存在し、抗体のクラスを決定する。異なるクラスの抗体は、抗原に応答して異なるエフェクター機構を活性化する(自然免疫系の異なる要素を誘発する)。これらは、免疫反応のさまざまな段階で現れ、構造的特徴や体の周りの場所も異なる[1]。

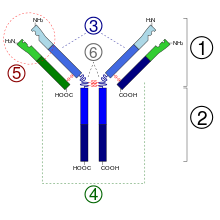
- フラグメント抗原結合
- フラグメント結晶化可能領域
- 重鎖(青)は、1つの可変(VH)ドメインに続いて、定常ドメイン(CH1)、ヒンジ領域、さらに2つの定常ドメイン(CH2とCH3)を持つ
- 軽鎖(緑)は1つの可変ドメイン(VL)と1つの定常ドメイン(CL)を持つ
- 抗原結合部位 (パラトープ)
- ヒンジ領域
アイソタイプの発現は、B細胞の成熟段階を反映している。ナイーブB細胞は、変異していない可変遺伝子を持つIgMとIgDのアイソタイプを発現しており、これらの遺伝子は、選択的スプライシング後に同じ初期転写物から生成される。他の抗体アイソタイプ(ヒトではIgG、IgA、IgE)の発現は、抗原曝露後のクラススイッチのプロセスを介して行われる。クラススイッチは、酵素AID(活性化誘導シチジンデアミナーゼ)によって行われ、B細胞がB細胞受容体を介して抗原に結合した後に起こる。クラススイッチには、通常、Tヘルパー細胞との相互作用が必要である[2][3]。
ヒトでは、5つの抗体アイソタイプに対応する5つの重鎖アイソタイプ α, δ, γ, ε, μ がある。
また、軽鎖のアイソタイプには κ および λ もあるが、両者の間に機能上の大きな違いはない。したがって、抗体のアイソタイプは、重鎖の定常領域のみで決定される[1]。
IgMは最初に、未熟B細胞の表面に単量体として発現する。抗原刺激を受け IgM+ B細胞は、5つのIg単量体がジスルフィド結合で結合した五量体のIgM抗体を分泌する。五量体はまた、ポリペプチド J鎖が含まれており、J鎖は2つの単量体を連結し、粘膜表面での分泌を促進する。IgM抗体の五量体構造により、反復エピトープ(例:細菌莢膜、ウイルスのカプシド)を持つ抗原に効率的に結合し、また補体カスケードを活性化する。IgM抗体は、B細胞応答の初期に発現するため、高度に変異することはほとんどなく、幅広い抗原反応性を示すため、T細胞の助けを必要とせずに、幅広い抗原に対して早期に応答することができる[4]。
IgDアイソタイプは、ナイーブB細胞が骨髄から離れ、二次リンパ系器官に移動する際に発現する。IgDアイソタイプの表面発現レベルは、B細胞の活性化状態の違いに関連付けられているが、血清中での役割はよくわかっていない[5]。
IgG、IgE、IgAの各抗体アイソタイプは、胚中心反応の際にクラススイッチに続いて生成され、特定の抗原に応答して異なるエフェクター機能を提供する。IgGは血清中で最も豊富な抗体クラスであり、定常領域遺伝子の構造の違いや、さまざまなエフェクター機能を誘発する能力の違いにより、4つのサブクラスに分類される。各サブクラスは配列の類似性が高い(アミノ酸単位で90%の同一性)にもかかわらず、異なる半減期、固有の抗原結合プロファイル、補体活性化の異なる能力を持っている。IgG1抗体は、最も豊富なIgGクラスであり、タンパク質抗原に対する応答を支配する。免疫不全のいくつかの症例でIgG1の産生障害が認められ、反復感染と関連している[6]。細菌莢膜多糖抗原に対するIgG応答は、主にIgG2サブクラスを介して行われ、このサブクラスが欠損すると、特定の細菌種に対して感染しやすくなる[7]。IgG2は、糖鎖抗原に反応する主要な抗体サブクラスであるが、IgG1およびIgG3サブクラスも、特にタンパク質-糖鎖結合体の場合は、そのような反応が観察されている[8]。
IgG3は、古典的補体経路を誘発することにより、炎症誘発性応答の効率的な活性化因子である[9]。他のIgGサブクラスと比較して半減期が最も短く[10]、ウイルス感染後にタンパク質抗原に反応してIgG1と一緒に存在することが多い[11]。IgG4は、血清中に最も少ないIgGサブクラスであり、同じ抗原に繰り返しさらされたり、または持続性感染症の際に生成されることが多い。
IgA抗体は、呼吸器または腸管で分泌され、粘膜免疫の主要なメディエーターとして働く[12]。それらは血清中では単量体であるが、粘膜表面では分泌型IgA(sIgA)と呼ばれる二量体として現れる。分泌型IgAは、J鎖と分泌因子(secretory component、SC)と呼ばれる別のポリペプチド鎖と関連付けられている[13]。IgA抗体は、ヒンジ領域の大きさが異なる2つのサブクラスに分けられる[14]。IgA1は、細菌プロテアーゼに対する感受性を高めるより長いヒンジ領域を持っている[15]。そのため、このサブクラスは血清IgAの大半を占め、IgA2は主に粘膜分泌物で見られる。IgAによる補体結合反応(complement fixation、CF)は、粘膜表面での主要なエフェクター機構ではないが、IgA受容体は好中球に発現しており、抗体依存性細胞傷害を媒介するために活性化される可能性がある[16]。sIgAはまた、樹状細胞が抗原と結合抗体を取り込むことにより、腸組織の免疫応答を増強することも示されている[17]。
IgE抗体は、末梢血中に最も低い濃度で存在するが、肥満細胞、好酸球、ランゲルハンス細胞の関与によるアレルギー反応の主要な抗体クラスを構成する[18]。また、特定の蠕虫(ぜんちゅう)に対する反応は、IgE抗体レベルの上昇によって特徴付けられる[19]。
参照項目 編集
脚注 編集
- ^ a b Janeway, CA (2001年). “Immunobiology: The Immune System in Health and Disease. 5th edition.”. NCBI. NCBI. 2016年1月19日閲覧。
- ^ Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002-01-01) (英語). Helper T Cells and Lymphocyte Activation.
- ^ Chandra, Vivek; Bortnick, Alexandra; Murre, Cornelis (2015-09-01). “AID targeting: old mysteries and new challenges”. Trends in Immunology 36 (9): 527–535. doi:10.1016/j.it.2015.07.003. PMC 4567449. PMID 26254147.
- ^ Chen, J, Boes, M (1998). “A critical role of natural immunoglobulin M in immediate defense against systemic bacterial infection”. J Exp Med 188 (12): 2381–6. doi:10.1084/jem.188.12.2381. PMC 2212438. PMID 9858525.
- ^ Achatz, G., Geisberger, R. (2006). “The riddle of the dual expression of IgM and IgD”. Immunology 118: 429–37. doi:10.1111/j.1365-2567.2006.02386.x. PMC 1782314. PMID 16895553.
- ^ Acton, R. T., Barton, J. C. (2016). “Selective Subnormal IgG1 in 54 Adult Index Patients with Frequent or Severe Bacterial Respiratory Tract Infections”. J Immunol Res 2016: 1405950. doi:10.1155/2016/1405950. PMC 4830719. PMID 27123464.
- ^ Out, T. A., Kuijpers, T. W. (1992). “IgG subclass deficiencies and recurrent pyogenic infections, unresponsiveness against bacterial polysaccharide antigens”. Allergol Immunopathol (Madr) 20: 28–34. PMID 1509985.
- ^ Jonsdottir, I., Vidarsson, G. (1998). “Isotypes and opsonophagocytosis of pneumococcus type 6B antibodies elicited in infants and adults by an experimental pneumococcus type 6B-tetanus toxoid vaccine”. Infect Immun 66: 2866–70. PMC 108283. PMID 9596761.
- ^ Barandun, S., Morell, A. (1972). “IgG subclasses: development of the serum concentrations in "normal" infants and children”. J Pediatr 80 (6): 960–4. doi:10.1016/s0022-3476(72)80007-6. PMID 4623683.
- ^ Smith, C. I., Hassan, M. S. (1991). “Biological half-life of normal and truncated human IgG3 in scid mice”. Eur J Immunol 21 (5): 1319–22. doi:10.1002/eji.1830210534. PMID 2037016.
- ^ Wahren, B., Linde, G. A. (1983). “Virus-specific antibody activity of different subclasses of immunoglobulins G and A in cytomegalovirus infections”. Infect Immun 42: 237–44. PMC 264549. PMID 6311746.
- ^ Honjo, T., Fagarasan, S. (2001). “In situ class switching and differentiation to IgA-producing cells in the gut lamina propria”. Nature 413 (6856): 639–43. doi:10.1038/35098100. PMID 11675788.
- ^ Hilschmann, N., Bastian, A. (1992). “Intra- and interchain disulfide bridges of the human J chain in secretory immunoglobulin A”. Biol Chem Hoppe-Seyler 373 (2): 1255–63. doi:10.1515/bchm3.1992.373.2.1255. PMID 1292512.
- ^ Perkins, S. J., Furtado, P. B. (2004). “Solution structure determination of monomeric human IgA2 by X-ray and neutron scattering, analytical ultracentrifugation and constrained modelling: a comparison with monomeric human IgA1”. J Mol Biol 338 (5): 921–41. doi:10.1016/j.jmb.2004.03.007. PMID 15111057.
- ^ Frandsen, E. V., Kilian, M. (1992). “Biological significance of IgA1 proteases in bacterial colonization and pathogenesis: critical evaluation of experimental evidence”. APMIS 104 (1–6): 321–38. doi:10.1111/j.1699-0463.1996.tb00724.x. PMID 8703438.
- ^ Palese, P., Mullarkey, C. E. (2016). “Broadly Neutralizing Hemagglutinin Stalk-Specific Antibodies Induce Potent Phagocytosis of Immune Complexes by Neutrophils in an Fc-Dependent Manner”. mBio 7 (5): e01624-16. doi:10.1128/mBio.01624-16. PMC 5050345. PMID 27703076.
- ^ van Kooten, C., Heystek, H. C. (2002). “Human immature dendritic cells efficiently bind and take up secretory IgA without the induction of maturation”. J Immunol 168: 102–7. doi:10.4049/jimmunol.168.1.102. PMID 11751952.
- ^ Walport M, Janeway CA Jr (2001). Immunobiology: The Immune System in Health and Disease.
- ^ Groenen, P. J, Appenzeller, S. (2015). “Immunoglobulin rearrangement analysis from multiple lesions in the same patient using next-generation sequencing”. Histopathology 67 (6): 843–58. doi:10.1111/his.12714. PMID 25891511.
外部リンク 編集
- Immunoglobulin Isotypes - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)
- 免疫学概要 - サウスカロライナ大学医学部
- 免疫グロブリン - 南イリノイ大学カーボンデール校