オルガノイド
オルガノイド(英:organoid)、試験管内など生体外(in vitro)、3次元(3D)的につくられた臓器である。「器官」(organ)と「~もどき」(-oid)を組み合わせた造語[1]。日本語では「臓器もどき[2]」「ミニ臓器[3]」とも呼ばれ、拡大しても本物そっくりの解剖学的構造を示すが、2020年時点では数ミリメートル大が上限[3]で、実際の臓器よりも小型・単純である。これらは、組織の細胞、ES細胞またはiPS細胞から、自己複製能力および分化能力で、3次元的な培養で、自己組織化により形成される。オルガノイドをつくり出す技術は、2010年代初めから急速に進歩しており、『ザ・サイエンティスト』誌はオルガノイドを「2013年の最大の科学的進歩の一つ」に選んだ[4]。
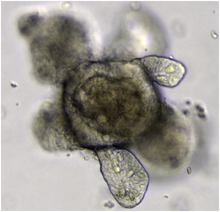
用途としては、発生学、様々な病気の原因や発病プロセス、創薬を含む医学・薬学の研究、再生医療やオーダーメイド医療[3]、移植[5]といった実際の治療への応用が挙げられる
歴史 編集
臓器をin vitroでつくるという試みの始まりは、ヘンリー・ヴァン・ピーターズ・ウィルソンによる。ウィルソンは、機械的に海綿動物を細胞までばらばらに解離し、その細胞が再集合し、自己組織化して生物全体を生成できることを実証した。これは最初の解離 - 再構成実験であった[6][7]。その後、数十年に亘り複数の研究室が、両生類や鳥類の雛から得られた臓器組織を用い、異なる種類の臓器をin vitroで解離させ再集合させることができた[6][8][9]。機械的にばらばらにされた細胞が集まって組織を再形成するために組織を再構成する現象は、後にMalcolm Steinbergによる差次接着仮説の提唱につながった[6]。幹細胞生物学分野の到来と共に、in vitroで器官を形成するという幹細胞の能力は初期に認識された。これは、幹細胞が奇形腫または胚様体を形成するとき、分化した細胞が複数の組織で見られるような異なる構造に組織化できるという観察による[6]。それまで幹細胞は平面の培地で培養や分化がなされていたが、立体的な培地での培養や、臓器の複雑な三次元構造の形成が可能になり、オルガノイドの研究分野が始まった[6]。研究者たちは1987年以来、3次元培養のための様々な方法を考案し、様々な種類の幹細胞を利用し、多数の臓器に似たオルガノイドができた。2008年、理化学研究所の笹井芳樹らのチームは、幹細胞が自ら組織化し、神経細胞の球に分化し、その球には層も観察できることを、実証した[10] 。2009年には、オランダのヒューブレヒト研究所(Hubrecht Institute)とUniversity Medical Center、ハンス・クレヴァース研究所が、単一のLGR5幹細胞が間葉系ニッチを伴わずにin vitroで陰窩-絨毛構造を構築することを示した[11]。2010年に、Mathieu UnbekandtとJamie A. Daviesは、マウス胎児由来の再生幹細胞からの腎臓オルガノイドの作成を実証した。その後、これらのオルガノイドのin vitroおよび生体内(in vivo)で生理学的機能を示したと報告されている[12][13][14]。
オーストリア科学アカデミーのマデリーン・ランカスター(Madeline Lancaster)は、2013年にヒトの脳の細胞組織の形成を模倣した幹細胞由来の大脳オルガノイドを培養するためのプロトコールを確立した[15]。
2014年、 米国イリノイ大学アーバナ・シャンペーン校のArtem Shkumatov等は、ES細胞が接着する基質の固さを調節することによって、心臓の血管のオルガノイドが形成されることを示した。生理的固さは、EBの三次元構造構築と心筋への分化を促進した[16]。
Takebeらは、多能性幹細胞由来の組織特異的前駆細胞または関連する組織サンプルを、内皮細胞および間充織幹細胞と組み合わせることにより、多様な組織からの器官芽(organ bud)形成の一般的な方法を実証した。彼らは、分化がより進んだものではなく、成熟していない組織や器官芽が、移植後の成熟した臓器の機能形成に効果的であることを示した[17]。
特性 編集
ランカスターらは[6]オルガノイドを臓器に特異的な種類の細胞の集合体として定義している。幹細胞または臓器前駆細胞から発生した細胞が、細胞選別や、空間的に制限された細胞どうしが接着し、自己組織化する。In vivoの臓器と同様、以下の性質を示す。
- 1つ以上の臓器特異的な細胞型を有する。
- 臓器のいくつかの特定の機能(例えば排泄、濾過、神経活動、収縮)を再現することができる。
- その細胞は一緒にグループ化され、臓器と同様に空間的に組織される。
工程 編集
オルガノイドは一般的に、立体的な培地中で、幹細胞または前駆細胞が培養され、形成される[6]。立体的な培地は、Engelbreth-Holm-Swarm腫瘍の細胞株によって分泌されるラミニンに富む細胞外マトリクスであるヒドロゲル・マトリゲル(hydrogel Matrigel)を使用して作製することができる[18]。オルガノイドは、幹細胞を立体的な培地に包埋することによって作製することができる[6]。多能性幹細胞がオルガノイドの生成に使用される場合、細胞は通常は胚様体を形成することが可能である。これらの胚様体は、パターニング因子で薬理学的に処理され、望みのオルガノイドの形成を促進する[6]。オルガノイドはまた、標的器官から採取された成体の幹細胞を用いて作製され、3D培地で培養されている[19]。
オルガノイドの種類 編集
オルガノイドを用いて多数の臓器の構造が再現されている[6]。オルガノイドの最新の文献に基づいた簡単な概要と、作成されたオルガノイドのリストと利用例、現状の状況を概説する。
オルガノイドを用いた基礎研究 編集
オルガノイドは、生物学の基礎研究をサポートするツールとなる。オルガノイドは、臓器内での細胞の相互作用、体内環境との相互作用、その臓器での疾患、薬物の効果の研究に役立つ。試験管内での培養は、扱いやすく、観察も容易である。実際の臓器は栄養素の問題で、培養は困難であるが、オルガノイドは大きさが小さいため、培養も可能である。一方、それらは臓器の特徴全てを示すわけではなく、他の臓器との相互作用はin vitroではわからない。
腸オルガノイドを用いて、幹細胞の研究がされてきたが[11]、栄養の取り込み、薬物輸送、およびインクレチンホルモンの分泌の研究にも用いられている[37]。これは、吸収不良疾患、ならびに肥満、インスリン抵抗性、および糖尿病などの代謝性疾患の研究において非常に重要である。
発生生物学のモデルとして 編集
オルガノイドは、発生生物学を研究するための特別なモデルとなる[38]。多能性幹細胞の運命の方向性を導く技術の進歩は、3D培養技術の進歩とあわさり、多数の人間の臓器の様々な特定の小領域の特性を再現するオルガノイドの作成を可能にした[38]。これらのオルガノイドの使用は、臓器形成の過程、および発生生物学の理解に大きく貢献した[38]。 例えば、中枢神経系の発生の理解に貢献している。さらに、オルガノイドは網膜形成の基礎となる物理的力の理解や、生物の種類に特徴的な眼の構造形成の理解に貢献した[39][40][38]。また 、大脳皮質における前駆細胞を制御する因子を同定した[41][42][38]。
医学研究・医療への利用 編集
病気のオルガノイドのモデル 編集
オルガノイドは、ヒト疾患の細胞モデルとして、病気の原因の解明や、治療法の研究に使用できる。1つの例では、CRISPRと呼ばれるゲノム編集システムを、ヒト多能性幹細胞に適用して、2つの異なる腎疾患、多嚢胞腎臓病および局所分節性糸球体硬化症に関連する遺伝子をターゲットに突然変異を導入した[33]。これらのCRISPRによる遺伝子改変された多能性幹細胞はその後、疾患に特異的な表現型を示すヒト腎臓オルガノイドを形成した。多嚢胞性腎臓疾患の変異を有する幹細胞由来の腎臓オルガノイドは、腎臓細管からの大きな半透明の嚢胞構造を形成した。局所分節性糸球体硬化症に関連する遺伝子に変異を有する腎臓オルガノイドは、その病気に罹患している濾細胞である足細胞間の接合部欠損を発症した。変異を入れる前の幹細胞からつくった、同じ遺伝的背景の、対照実験となるオルガノイドは、これらの疾患の表現型を示さなかった[33]。これらの実験は、オルガノイドが、ヒトの病気の複雑なモデルとして、実験室での研究に利用できるかを実証するものであり、ペトリ皿で、組織レベルの表現型が再現された。
オルガノイドを使ったオーダーメイド医療 編集
クレヴァースのグループによって確立された培養プロトコルを用いて、直腸の生検から育てた腸オルガノイドは、嚢胞性線維症をモデル化するために使用されており[43]、オーダーメイド医療のためのオルガノイドの最初の応用につながった[44]。嚢胞性線維症は、健康な上皮表面の粘液に必要なイオンチャネルをコードする遺伝子変異によって引き起こされる遺伝性疾患である。フォルスコリンやコレラ毒素のようなcAMP上昇アゴニストによって腸オルガノイドを刺激すると、完全にCFTRに依存してオルガノイドの急速な腫脹を誘発することをJeffrey Beekmanが報告している[43]。嚢胞性線維症でない人からつくったオルガノイドは、フォルスコリンに応答して、オルガノイドの管腔内へ液体が輸送され膨潤するが、これは嚢胞性線維症の人からつくったオルガノイドにおいては著しく減少または欠如している。 CFTRタンパク質を修復する治療薬(CFTR調節薬)によって腫れが回復する可能性があり、CFTR調節薬を、まずはオルガノイドで試して、個々の反応を、生体で治療する前に、実験室環境で定量できることを示している。 Schwankらはまた、腸の嚢胞性線維症オルガノイドの表現型が、2013年にCRISPR-Cas9ゲノム編集によって修復され得ることを実証した[45]。Dekkersらによる2016年のフォローアップ研究では、嚢胞性線維症の人々からつくった腸オルガノイドの、フォルスコリン誘発腫脹の定量的な差異が、CFTR機能の既知の診断マーカーと関連していることを明らかにし[44]、さらに、特定のCFTR変異を有する腸オルガノイドにおけるCFTR調節薬への応答が、これらの治療の公表された臨床試験データと相関することを実証した。これにより、治療を受ける前のCFTR変異の患者由来のオルガノイドを用い、CFTR調節薬が有効かを調べるという、前臨床試験が行われた。これらの研究は、オルガノイドが個々の治療またはオーダーメイド医療のために使用できることを初めて示した。
オルガノイドのヒトへの移植 編集
日本の東京医科歯科大学は、潰瘍性大腸炎治療のため、患者本人から採取した組織からつくった腸上皮幹細胞を含むオルガノイドを移植したと2022年7月7日発表した[46][5]。
新型コロナウイルス感染症 編集
新型コロナウイルス感染症の病原体であるSARS-CoV-2は全身の臓器に感染するウイルスであることが疑われている[47]。ヒトの組織を構成している細胞を用いて様々な組織のオルガノイドを作製し、試験管内でSARS-CoV-2を感染させて、ウイルスがどの組織の、どの細胞に感染するのかを直接検証する研究が始まっている[47]。ウイルス感染症の研究へのオルガノイドの利用は新型コロナウイルスの世界的流行を機に本格化し、その一環として日本の京都大学では、鼻腔のオルガノイドを作製して後遺症の一つである嗅覚障害の発症プロセスについて調べている[48]。
オルガノイドを用いたSARS-CoV-2感染モデルは、新型コロナウイルス感染症治療薬の探索にも有用であり、血管、気管支、肝臓のそれぞれのオルガノイドを用いて、可溶性ACE2蛋白質 、カモスタット、イマチニブにSARS-CoV-2の感染・増殖抑制活性があることが証明されて、治験が計画・実行されている[47]。
脚注 編集
- ^ 木村ちえみ「オルガノイドとは 臓器・組織を模倣した3次元構造体」日経バイオテクONLINE(2023年4月21日)2024年2月21日閲覧
- ^ (延期)オルガノイドをテーマとする国際シンポジウム(2020年3月)、開催のお知らせ 理化学研究所(2019年11月7日)2022年5月4日閲覧
- ^ a b c 【科学の扉】ミニ臓器、実力アップ 脳・目・肝…構造や機能再現、コロナ研究にも『朝日新聞』朝刊2020年10月26日(扉面)2020年11月23日閲覧
- ^ Grens, Kerry (2013年12月24日). “2013’s Big Advances in Science”. The Scientist. 2013年12月26日閲覧。
- ^ a b 『読売新聞』朝刊2022年7月8日:1面「腸粘膜細胞培養し移植 オルガノイド 潰瘍性大腸炎根治図る 東京医科歯科大」および社会面関連記事(潰瘍性大腸炎研究 患者団体「新たな一手」 専門家「コストが課題」/「ミニ臓器」活用へ期待)
- ^ a b c d e f g h i j k Lancaster, M. A.; Knoblich, J. A. (2014). “Organogenesis in a dish: Modeling development and disease using organoid technologies”. Science 345 (6194): 1247125-1247125. doi:10.1126/science.1247125.
- ^ H. V. Wilson (1907). “A new method by which sponges may be artificially reared”. Science 25: 912–915. doi:10.1126/science.25.649.912. PMID 17842577.
- ^ J Holtfreter (1944). “Experimental studies on the developmental of the pronephros”. Rev. Can. Biol. 3: 220–250.
- ^ P. Weiss, A. C. Taylor (1960). “Reconstitution of complete organs from single-cell suspensions of chick embryos in advanced stages of differentiation”. Proc. Natl. Acad. Sci. U.S.A. 46: 1177–1185. doi:10.1073/pnas.46.9.1177. PMID 16590731.
- ^ “Lab-Grown Model Brains”. The Scientist (2013年8月28日). 2013年12月26日閲覧。
- ^ a b c Sato T, Vries RG, Snippert HJ, van de Wetering M, Barker N, Stange DE, van Es JH, Abo A, Kujala P, Peters PJ, Clevers H. (2009). “Single Lgr5 stem cells build cryptvillus structures in vitro without a mesenchymal niche”. Nature 459 (7244): 262–265. doi:10.1038/nature07935. PMID 19329995.
- ^ a b Unbekandt M, Davies JA (2010). “Dissociation of embryonic kidneys followed by reaggregation allows the formation of renal tissues”. Kidney Int. 77 (5): 407–416. doi:10.1038/ki.2009.482. PMID 20016472.
- ^ Lawrence ML, Chang CH, Davies JA (2015). “Transport of organic anions and cations in murine embryonic kidney development and in serially-reaggregated engineered kidneys”. Scientific Reports 77 (5): 9092-9092. doi:10.1038/srep09092. PMC 4357899. PMID 25766625.
- ^ Xinaris C, Benedetti V, Rizzo P, Abbate M, Corna D, Azzollini N, Conti S, Unbekandt M, Davies JA, Morigi M, Benigni A, Remuzzi G (2012). “In vivo maturation of functional renal organoids formed from embryonic cell suspensions”. J. Am. Soc. Neprhol. 23 (11): 1857–1868. doi:10.1681/ASN.2012050505. PMC 3482737. PMID 23085631.
- ^ Chambers SM, Tchieu J, Studer L. (October 2013). “Build-a-Brain”. Cell Stem Cell 13 (4): 377–8. doi:10.1016/j.stem.2013.09.010. PMID 24094317.
- ^ Shkumatov, A; Baek, K; Kong, H (2014). “Matrix Rigidity-Modulated Cardiovascular Organoid Formation from Embryoid Bodies”. PLoS ONE 9 (4): e94764. doi:10.1371/journal.pone.0094764. PMC 3986240. PMID 24732893.
- ^ Takebe T, Enomura M, Yoshizawa E, Kimura M, Koike H, Ueno Y, Matsuzaki T, Yamazaki T, Toyohara T, Osafune K, Nakauchi H, Yoshikawa HY, Taniguchi H (2015). “Vascularized and Complex Organ Buds from Diverse Tissues via Mesenchymal Cell-Driven Condensation”. Cell Stem Cell 16 (5): 556–565. doi:10.1016/j.stem.2015.03.004. PMID 25891906.
- ^ Li ML, Aggeler J, Farson DA, Hatier C, Hassell J, Bissell MJ (1987). “Influence of a reconstituted basement membrane and its components on casein gene expression and secretion in mouse mammary epithelial cells”. Proc. Natl. Acad. Sci. U.S.A. 84: 136–140. doi:10.1073/ pnas.84.1.136. PMC 304157. PMID 3467345.
- ^ Pastuła A, Middelhoff M, Brandtner A, Tobiasch M, Höhl B, Nuber AH, Demir IE, Neupert S, Kollmann P, Mazzuoli-Weber G, Quante M (2016). “Three-Dimensional Gastrointestinal Organoid Culture in Combination with Nerves or Fibroblasts: A Method to Characterize the Gastrointestinal Stem Cell Niche”. Stem Cells Int. 2016: 3710836. doi:10.1155/2016/3710836. PMC 4677245. PMID 26697073.
- ^ Muguruma, Keiko; Nishiyama, Ayaka; Kawakami, Hideshi; Hashimoto, Kouichi; Sasai, Yoshiki (2015-02-03). “Self-organization of polarized cerebellar tissue in 3D culture of human pluripotent stem cells”. Cell Reports 10 (4): 537–550. doi:10.1016/j.celrep.2014.12.051. ISSN 2211-1247. PMID 25640179.
- ^ Muguruma, Keiko (2017). “3D Culture for Self-Formation of the Cerebellum from Human Pluripotent Stem Cells Through Induction of the Isthmic Organizer”. Methods in Molecular Biology (Clifton, N.J.) 1597: 31–41. doi:10.1007/978-1-4939-6949-4_3. ISSN 1940-6029. PMID 28361308.
- ^ Koehler, Karl R.; Mikosz, Andrew M.; Molosh, Andrei I.; Patel, Dharmeshkumar; Hashino, Eri (2013-08-08). “Generation of inner ear sensory epithelia from pluripotent stem cells in 3D culture”. Nature 500 (7461): 217–221. doi:10.1038/nature12298. ISSN 1476-4687. PMC 3739998. PMID 23842490.
- ^ Koehler, Karl R.; Nie, Jing; Longworth-Mills, Emma; Liu, Xiao-Ping; Lee, Jiyoon; Holt, Jeffrey R.; Hashino, Eri (06 2017). “Generation of inner ear organoids containing functional hair cells from human pluripotent stem cells”. Nature Biotechnology 35 (6): 583–589. doi:10.1038/nbt.3840. ISSN 1546-1696. PMC 5462862. PMID 28459451.
- ^ Martin A, Barbesino G, Davies TF (1999). “T-Cell Receptors and Autoimmune Thyroid Disease—Signposts for T-Cell-Antigen Driven Diseases”. International Reviews of Immunology 18 (1–2): 111–40. doi:10.3109/08830189909043021. PMID 10614741.
- ^ Bredenkamp N, Ulyanchenko S, O'Neill KE, Manley NR, Vaidya HJ, Blackburn CC. “An organized and functional thymus generated from FOXN1-reprogrammed fibroblasts”. Nature Cell Biology 16 (9): 902–908. doi:10.1038/ncb3023. PMC 4153409. PMID 25150981.
- ^ a b c Vianello, F.; Poznansky, M. C. (2007). “Generation of a tissue-engineered thymic organoid”. Methods Mol. Biol. 380: 163-170. doi:10.1007/978-1-59745-395-0_9. PMID 17876092.
- ^ Huch M. et al. (2015). “Long-Term Culture of Genome-Stable Bipotent Stem Cells from Adult Human Liver”. Cell 160 (1–2): 299–312. doi:10.1016/j.cell.2014.11.050. PMC 4313365. PMID 25533785.
- ^ Huch M. et al. (2013). “Unlimited in vitro expansion of adult bi-potent pancreas progenitors through the Lgr5/R-spondin axis”. The EMBO Journal 32 (20): 2708–2721. doi:10.1038/emboj.2013.204. PMC 3801438. PMID 24045232.
- ^ Hajime U, et al. A xenogeneic-free system generating functional human gut organoids from pluripotent stem cells. JCI Insight. 2017 Jan 12;2(1):e86492. doi: 10.1172/jci.insight.86492.
- ^ Barker N, van Es JH, Kuipers J, Kujala P, van den Born M, Cozijnsen M, Haegebarth A, Korving J, Begthel H, Peters PJ, Clevers H (2007). “Identification of stem cells in small intestine and colon by marker gene Lgr5”. Nature 449 (7165): 1003–1007. doi:10.1038/nature06196. PMID 17934449.
- ^ Lee JH, Bhang DH, Beede A, Huang TL, Stripp BR, Bloch KD, Wagers AJ, Tseng YH, Ryeom S, Kim CF. “Lung Stem Cell Differentiation in Mice Directed by Endothelial Cells via a BMP4-NFATc1-Thrombospondin-1 Axis”. Cell 156 (3): 440–455. doi:10.1016/j.cell.2013.12.039. ISSN 0092-8674. PMC 3951122. PMID 24485453.
- ^ Takasato M2, Er PX, Chiu HS, Maier B, Baillie GJ, Ferguson C, Parton RG, Wolvetang EJ, Roost MS, Chuva de Sousa Lopes SM, Little MH. “Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis”. Nature 526 (7574): 564–568. doi:10.1038/nature15695. PMID 26444236.
- ^ a b c Freedman, B. S.; Brooks, C. R.; Lam, A. Q.; Fu, H.; Morizane, R.; Agrawal, V.; Saad, A. F.; Li, M. K. et al. (2015). “Modelling kidney disease with CRISPR-mutant kidney organoids derived from human pluripotent epiblast spheroids”. Nat. Commun. 6: 8715. doi:10.1038/ncomms9715. PMC 4620584. PMID 26493500.
- ^ Morizane, R.; Lam, A. Q; Freedman, B. S; Kishi, S.; Valerius, M T.; Bonventre, J. V. (2015). “Nephron organoids derived from human pluripotent stem cells model kidney development and injury”. Nature Biotechnology 33 (11): 1193–1200. doi:10.1038/nbt.3392. PMC 4747858. PMID 26458176.
- ^ van den Brink SC, Baillie-Johnson P, Balayo T, Hadjantonakis AK, Nowotschin S, Turner DA, Martinez Arias A (2014). “Symmetry breaking, germ layer specification and axial organisation in aggregates of mouse embryonic stem cells”. Development (Cambridge, England) 141 (22): 4231–4242. doi:10.1242/dev.113001. PMC 4302915. PMID 25371360.
- ^ Turner DA, Baillie-Johnson P, Martinez Arias A (2016). “Organoids and the genetically encoded self-assembly of embryonic stem cells”. BioEssays 38 (2): 181–191. doi:10.1002/bies.201500111. PMC 4737349. PMID 26666846.
- ^ Zietek T, Rath E, Haller D, Daniel H. “Intestinal organoids for assessing nutrient transport, sensing and incretin secretion”. Sci. Rep. 5. doi:10.1038/srep16831. PMC 4652176. PMID 26582215.
- ^ a b c d e Ader, M.; Tanaka, E. M. (2014). “Modeling human development in 3D culture”. Curr. Opin. Cell Biol. 31: 23-28. doi:10.1016/j.ceb.2014.06.013. PMID 25033469.
- ^ Nakano T, Ando S, Takata N, Kawada M, Muguruma K, Sekiguchi K, Saito K, Yonemura S, Eiraku M, Sasai Y (2012). “Self-formation of optic cups and storable stratified neural retina from human ESCs”. Cell Stem Cell 10: 771–785. doi:10.1016/j.stem.2012.05.009. PMID 22704518.
- ^ M. Eiraku, N. Takata, H. Ishibashi, M. Kawada, E. Sakakura, S. Okuda, K. Sekiguchi, T. Adachi, Y. Sasai Self-organizing optic-cup morphogenesis in three-dimensional culture Nature, 472 (2011), pp. 51–56
- ^ Eiraku M, Watanabe K, Matsuo-Takasaki M, Kawada M, Yonemura S, Matsumura M, Wataya T, Nishiyama A, Muguruma K, Sasai Y (2008). “Self-organized formation of polarized cortical tissues from ESCs and its active manipulation by extrinsic signals”. Cell Stem Cell 3: 519–532. doi:10.1016/j.stem.2008.09.002. PMID 18983967.
- ^ Mariani J, Simonini MV, Palejev D, Tomasini L, Coppola G, Szekely AM, Horvath TL, Vaccarino FM (2012). “Modeling human cortical development in vitro using induced pluripotent stem cells”. Proc. Natl. Acad. Sci. U. S. A. 109: 12770–12775. doi:10.1073/pnas.1202944109. PMC 3411972. PMID 22761314.
- ^ a b Dekkers JF, Wiegerinck CL, de Jonge HR, Bronsveld I, Janssens HM, de Winter-de Groot KM, Brandsma AM, de Jong NW, Bijvelds MJ, Scholte BJ, Nieuwenhuis EE, van den Brink S, Clevers H, van der Ent CK, Middendorp S, Beekman JM (2012). “A functional CFTR assay using primary cystic fibrosis intestinal organoids”. Nat. Med. 19: 939–945. doi:10.1038/nm.3201. PMID 23727931.
- ^ a b Dekkers JF, Berkers G, Kruisselbrink E, Vonk A, de Jonge HR, Janssens HM, Bronsveld I, van de Graaf EA, Nieuwenhuis EE, Houwen RH, Vleggaar FP, Escher JC, de Rijke YB, Majoor CJ, Heijerman HG, de Winter-de Groot KM, Clevers H, van der Ent CK, Beekman JM. “Characterizing responses to CFTR-modulating drugs using rectal organoids derived from subjects with cystic fibrosis”. Sci. Transl. Med. 8: 344ra84. doi:10.1126/scitranslmed.aad8278. PMID 27334259.
- ^ Schwank G, Koo BK, Sasselli V, Dekkers JF, Heo I, Demircan T, Sasaki N, Boymans S, Cuppen E, van der Ent CK, Nieuwenhuis EE, Beekman JM, Clevers H. “Functional repair of CFTR by CRISPR/Cas9 in intestinal stem cell organoids of cystic fibrosis patients.”. Cell Stem Cell 13: 635–638. doi:10.1016/j.stem.2013.11.002. PMID 24315439.
- ^ 「世界初、自家腸上皮オルガノイドを潰瘍性大腸炎患者に移植」―オルガノイド医療の実用化に道を拓く大きな第一歩―東京医科歯科大学プレスリリース(2022年7月7日)2022年7月19日閲覧
- ^ a b c “新型コロナによる多臓器傷害の機序をオルガノイドが解明”. 日経バイオテク (2020年7月14日). 2020年7月15日閲覧。
- ^ 【Techワード】オルガノイド/病の臓器再現、創薬促す コロナ後遺症の解明も『日本経済新聞』朝刊2022年4月8日テック面(2022年5月4日閲覧)
推薦文献 編集
- Willyard, Cassandra (2015). “The boom in mini stomachs, brains, breasts, kidneys and more”. Nature 523: 520–522. doi:10.1038/523520a.
- Kelly Rae Chi (2015). Orchestrating Organoids. A guide to crafting tissues in a dish that reprise in vivo organs. The Scientist.
- Turner, David A.; Baillie-Johnson, Peter; Martinez Arias, Alfonso (February 2016). “Organoids and the genetically encoded self-assembly of embryonic stem cells”. Bioassays 38 (2): 181–91. doi:10.1002/bies.201500111. PMC 4737349. PMID 26666846.