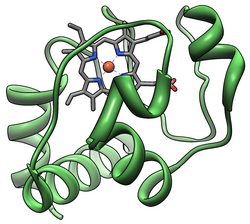
シトクロムc
シトクロムc(cytochrome c, cyt c)は、ミトコンドリアの内膜に弱く結合しているヘムタンパク質の一種である。タンパク質のシトクロムcファミリーに属する。他のシトクロムと異なり可溶性(100 g/L)で、電子伝達系において不可欠な因子である。電子伝達系では複合体IIIから1電子を受け取り、複合体IVに1電子を引き渡す。酸化型をフェリシトクロムc、還元型をフェロシトクロムcと呼ぶこともある。ヒトではシトクロムcは CYCS 遺伝子にコードされている[5][6]。
| シトクロムc | |
|---|---|
| 識別情報 | |
| CAS登録番号 | 9007-43-6 |
| KEGG | C00524 C00125 (酸化型、フェリシトクロムc) C00126 (還元型、フェロシトクロムc) |
| 関連する物質 | |
| 関連する酵素 | 鉄-シトクロムcレダクターゼ、 シトクロムcオキシダーゼ、 シトクロムcペルオキシダーゼ |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |

機能 編集
電子伝達系における役割 編集
シトクロムcはミトコンドリアで電子伝達系の構成要素を成す。シトクロムcのヘム基がb-c1複合体から電子を受け取り、シトクロムオキシダーゼ複合体に電子を渡す。また、シトクロムcはアポトーシスの開始にも関与する(後述)。シトクロムcは、細胞質に放たれるとアポトーシスプロテアーゼ活性化因子に結合する[5]。
シトクロムcはヒドロキシル化や芳香族酸化など幾つかの反応の触媒能を持つほかペルオキシダーゼ活性を有し、2,2-azino-bis(3-ethylbenzthiazoline-6-sulphonic acid (ABTS) や 2-keto-4-thiomethyl butyric acidや4-aminoantipyrine といった電子伝達体を酸化する。
アポトーシスにおける役割 編集
シトクロムcは、アポトーシス(胚発生の段階や感染・DNA損傷への応答として細胞が自殺する制御的プロセス)においてシグナル仲介の役割を担っていることが知られている[7]。
細胞がアポトーシス誘導刺激を受けると、ミトコンドリアからシトクロムcが放出される。これは、細胞内のカルシウムイオン濃度が上昇することで、ミトコンドリアPTP(permeability transition pore)の開口が促されることによる。少量放出されたシトクロムcは小胞体膜上にあるIP3受容体と相互作用し、小胞体からカルシウムが放出される。このプロセスにより、濃度が上がったカルシウムはシトクロムcの大量放出を引き起こし、正のフィードバックループを形成して小胞体からのカルシウム放出を持続させる。これにより、小胞体から放出されたカルシウムの量は細胞毒性をきたすまで上昇する。細胞質中に放出されたシトクロムcは、今度はカスパーゼ9と呼ばれるシステインプロテアーゼを活性化する。カスパーゼ9はカスパーゼ3とカスパーゼ7を活性化し(カスパーゼカスケード)、最終的にアポトーシスを引き起こす。
種間保存性 編集
シトクロムcは高度に保存されたタンパク質で、植物、動物、単細胞生物など非常に多様な生物で確認されている。この保存性と、約 12,000 Da という分子量の小ささから、分子系統学において有用なツールとなっている。一次構造はおよそ100アミノ酸残基から成るポリペプチド鎖であるが、多くの多細胞生物では104アミノ酸残基のポリペプチド鎖となっている[8]。
シトクロムcは進化生物学の分野でも研究対象となっている。例えばニワトリとシチメンチョウにおけるシトクロムcのアミノ酸配列は全く同じであるが、これらとアヒルとの間には1アミノ酸残基の違いがある。同様に、ヒトとチンパンジーのシトクロムcはまったく同一であるが、アカゲザルとの間には1アミノ酸残基の違いがある[9]。ヒトとチンパンジーでは66番目のアミノ酸残基がイソロイシンであるが、アカゲザルではこれがスレオニンになっている[8]。ブタ、ウシ、ヒツジのシトクロムcは全て同一である。
クラス 編集
1991年、R・P・アンブラーはシトクロムcには以下の4つのクラスがあると考えた[10]。
応用 編集
シトクロムcは、いわゆる低レベルレーザー治療(Low-Level laser therapy; LLLT)において機能的な働きを担っているのではないかと言われている。低レベルレーザー治療とは、赤色光や近赤外線を照射して組織を貫通させ、細胞の再生を高めるという治療法である。この波長の光はシトクロムcの活性を高める働きを持つとされ、これにより代謝が活性化し、組織再生のためのエネルギーを効率的に生み出すことが出来ているのではないか、と考えられている[11]。
相互作用 編集
シトクロムcはCOX4I2と相互作用することが判明している[12][13][14][15]。
シトクロムCは図の左中央近くにある。
アミノ酸配列 編集
ヒトにおける一次構造(105アミノ酸残基):
MGDVEKGKKIFIMKCSQCHTVEKGGKHKTGPNLHGLFGRKTGQAPGYSYTAANKNKGIIW GEDTLMEYLENPKKYIPGTKMIFVGIKKKEERADLIAYLKKATNE
出典 編集
- ^ a b c GRCh38: Ensembl release 89: ENSG00000172115 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000063694 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ a b “Entrez Gene: cytochrome c”. 2010年4月18日閲覧。
- ^ Tafani M, Karpinich NO, Hurster KA, Pastorino JG, Schneider T, Russo MA, Farber JL (March 2002). “Cytochrome c release upon Fas receptor activation depends on translocation of full-length bid and the induction of the mitochondrial permeability transition”. J. Biol. Chem. 277 (12): 10073–82. doi:10.1074/jbc.M111350200. PMID 11790791.
- ^ Liu X, Kim C, Yang J, Jemmerson R, Wang X (1996). “Induction of apoptotic program in cell-free extracts: requirement for dATP and cytochrome c”. Cell 86 (1): 147–57. doi:10.1016/S0092-8674(00)80085-9. PMID 8689682.
- ^ a b Amino acid sequences in cytochrome c proteins from different species, adapted from Strahler, Arthur; Science and Earth History, 1997. page 348.
- ^ Linda Stone; Paul F. Lurquin; Luigi Luca Cavalli-Sforza. Genes, Culture, and Human Evolution: A Synthesis, Blackwell Publishing, 2007, page 79. ISBN 1405150890
- ^ Ambler RP (May 1991). “Sequence variability in bacterial cytochromes c”. Biochim. Biophys. Acta 1058 (1): 42–7. PMID 1646017.
- ^ Silveira PC, Streck EL, Pinho RA. (2005). “Cellular effects of low power laser therapy can be mediated by nitric oxide.”. Lasers Surg Med. 36 (4): 307–14. doi:10.1002/lsm.20148. PMID 15739174.
- ^ Michel, B; Bosshard H R (Aug. 1984). “Spectroscopic analysis of the interaction between cytochrome c and cytochrome c oxidase”. J. Biol. Chem. (UNITED STATES) 259 (16): 10085–91. ISSN 0021-9258. PMID 6088481.
- ^ Wiedemann, F R; Vielhaber S, Schröder R, Elger C E, Kunz W S (Mar. 2000). “Evaluation of methods for the determination of mitochondrial respiratory chain enzyme activities in human skeletal muscle samples”. Anal. Biochem. (UNITED STATES) 279 (1): 55–60. doi:10.1006/abio.1999.4434. ISSN 0003-2697. PMID 10683230.
- ^ Sampson, V; Alleyne T (Dec. 2001). “Cytochrome c/cytochrome c oxidase interaction. Direct structural evidence for conformational changes during enzyme turnover”. Eur. J. Biochem. (Germany) 268 (24): 6534–44. ISSN 0014-2956. PMID 11737208.
- ^ Lynch, S R; Sherman D, Copeland R A (Jan. 1992). “Cytochrome c binding affects the conformation of cytochrome a in cytochrome c oxidase”. J. Biol. Chem. (UNITED STATES) 267 (1): 298–302. ISSN 0021-9258. PMID 1309738.
- ^ KEGG Homo sapiens (human): 54205
関連文献 編集
- Kumarswamy R and Chandna S (2009). “Putative partners in Bax mediated cytochrome-c release: ANT, CypD, VDAC or none of them?”. Mitochondrion. 9 (1): 1–8. doi:10.1016/j.mito.2008.10.003. PMID 18992370.
- Skulachev VP (1998). “Cytochrome c in the apoptotic and antioxidant cascades.”. FEBS Lett. 423 (3): 275–80. doi:10.1016/S0014-5793(98)00061-1. PMID 9515723.
- Mannella CA (1998). “Conformational changes in the mitochondrial channel protein, VDAC, and their functional implications.”. J. Struct. Biol. 121 (2): 207–18. doi:10.1006/jsbi.1997.3954. PMID 9615439.
- Ferri KF, Jacotot E, Blanco J, et al. (2001). “Mitochondrial control of cell death induced by HIV-1-encoded proteins.”. Ann. N. Y. Acad. Sci. 926: 149–64. PMID 11193032.
- Britton RS, Leicester KL, Bacon BR (2002). “Iron toxicity and chelation therapy.”. Int. J. Hematol. 76 (3): 219–28. doi:10.1007/BF02982791. PMID 12416732.
- Haider N, Narula N, Narula J (2003). “Apoptosis in heart failure represents programmed cell survival, not death, of cardiomyocytes and likelihood of reverse remodeling.”. J. Card. Fail. 8 (6 Suppl): S512–7. doi:10.1054/jcaf.2002.130034. PMID 12555167.
- Castedo M, Perfettini JL, Andreau K, et al. (2004). “Mitochondrial apoptosis induced by the HIV-1 envelope.”. Ann. N. Y. Acad. Sci. 1010: 19–28. doi:10.1196/annals.1299.004. PMID 15033690.
- Ng S, Smith MB, Smith HT, Millett F (1977). “Effect of modification of individual cytochrome c lysines on the reaction with cytochrome b5.”. Biochemistry 16 (23): 4975–8. doi:10.1021/bi00642a006. PMID 199233.
- Lynch SR, Sherman D, Copeland RA (1992). “Cytochrome c binding affects the conformation of cytochrome a in cytochrome c oxidase.”. J. Biol. Chem. 267 (1): 298–302. PMID 1309738.
- Garber EA, Margoliash E (1990). “Interaction of cytochrome c with cytochrome c oxidase: an understanding of the high- to low-affinity transition.”. Biochim. Biophys. Acta 1015 (2): 279–87. doi:10.1016/0005-2728(90)90032-Y. PMID 2153405.
- Bedetti CD (1985). “Immunocytochemical demonstration of cytochrome c oxidase with an immunoperoxidase method: a specific stain for mitochondria in formalin-fixed and paraffin-embedded human tissues.”. J. Histochem. Cytochem. 33 (5): 446–52. PMID 2580882.
- Tanaka Y, Ashikari T, Shibano Y, et al. (1988). “Construction of a human cytochrome c gene and its functional expression in Saccharomyces cerevisiae.”. J. Biochem. 103 (6): 954–61. PMID 2844747.
- Evans MJ, Scarpulla RC (1989). “The human somatic cytochrome c gene: two classes of processed pseudogenes demarcate a period of rapid molecular evolution.”. Proc. Natl. Acad. Sci. U.S.A. 85 (24): 9625–9. doi:10.1073/pnas.85.24.9625. PMID 2849112.
- Passon PG, Hultquist DE (1972). “Soluble cytochrome b 5 reductase from human erythrocytes.”. Biochim. Biophys. Acta 275 (1): 62–73. doi:10.1016/0005-2728(72)90024-2. PMID 4403130.
- Dowe RJ, Vitello LB, Erman JE (1984). “Sedimentation equilibrium studies on the interaction between cytochrome c and cytochrome c peroxidase.”. Arch. Biochem. Biophys. 232 (2): 566–73. doi:10.1016/0003-9861(84)90574-5. PMID 6087732.
- Michel B, Bosshard HR (1984). “Spectroscopic analysis of the interaction between cytochrome c and cytochrome c oxidase.”. J. Biol. Chem. 259 (16): 10085–91. PMID 6088481.
- Broger C, Nałecz MJ, Azzi A (1980). “Interaction of cytochrome c with cytochrome bc1 complex of the mitochondrial respiratory chain.”. Biochim. Biophys. Acta 592 (3): 519–27. doi:10.1016/0005-2728(80)90096-1. PMID 6251869.
- Smith HT, Ahmed AJ, Millett F (1981). “Electrostatic interaction of cytochrome c with cytochrome c1 and cytochrome oxidase.”. J. Biol. Chem. 256 (10): 4984–90. PMID 6262312.
- Geren LM, Millett F (1981). “Fluorescence energy transfer studies of the interaction between adrenodoxin and cytochrome c.”. J. Biol. Chem. 256 (20): 10485–9. PMID 6270113.
- Favre B, Zolnierowicz S, Turowski P, Hemmings BA (1994). “The catalytic subunit of protein phosphatase 2A is carboxyl-methylated in vivo.”. J. Biol. Chem. 269 (23): 16311–7. PMID 8206937.
- Gao B, Eisenberg E, Greene L (1996). “Effect of constitutive 70-kDa heat shock protein polymerization on its interaction with protein substrate.”. J. Biol. Chem. 271 (28): 16792–7. doi:10.1074/jbc.271.28.16792. PMID 8663341.
外部リンク 編集
- The Cytochrome c Protein
- Apoptosis & Caspase 3 - PMAP The Proteolysis Map-animation
- UMich Orientation of Proteins in Membranes families/superfamily-78 - Calculated orientations of cytochromes c in the lipid bilayer
- Cytochrome c - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)