三フッ化臭素
三フッ化臭素(さんフッかしゅうそ、英: bromine trifluoride)は、化学式BrF3の、臭素とフッ素によるハロゲン間化合物。毒性と腐食性のある液体で、硫酸に溶けるが水や有機化合物とは爆発的に反応する。強力なフッ素化剤であり、核燃料処理において六フッ化ウランの製造に使われる[2]。
| 三フッ化臭素 | |
|---|---|

| |
| |
| 特性 | |
| 化学式 | BrF3 |
| モル質量 | 136.90 g/mol |
| 外観 | 吸湿性のある、無色ないし麦わら色の液体 |
| 匂い | 刺激臭 |
| 密度 | 2.803 g/cm3 [1] |
| 融点 |
8.77℃ |
| 沸点 |
125.72℃ |
| 水への溶解度 | 分解 |
| 硫酸への溶解度 | 可溶 |
| 構造 | |
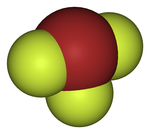
| 分子の形 | T字形 |
| 双極子モーメント | 1.19 D |
| 危険性 | |
| EU分類 | 未分類 |
| NFPA 704 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
合成 編集
1906年に、フランスの科学者ポール・ルボー (Paul Lebeau) が臭素とフッ素を20℃で反応させて製造した:[3]。
構造 編集
他の三フッ化ハロゲンである三フッ化塩素や三フッ化ヨウ素と同様、T字形の構造をしている。臭素原子からは2つの孤立電子対が出ている。臭素からの距離は、軸方向のフッ素が1.81Å、赤道方向のフッ素が1.72Å。孤立電子対の反発のため、軸方向とフッ素方向の角度は90°~86.2°となっている.[5][6]。
性質 編集
フッ素化剤として使われるが、三フッ化塩素に比べ反応は弱い。自己解離により導電性を持つ[2]。
多くのフッ化物イオンを溶かし、solvobasesを形成する[2]。
安全性 編集
日本の消防法では第6類危険物に分類される。自体は不燃性だが、有機化合物などと反応し、火災を起こすことがある。加水分解によりフッ化水素などを生じる。皮膚や眼に対し強い刺激性がある。吸入や経口・経皮摂取により黄疸や呼吸困難を生じる[7]。
脚注 編集
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
- ^ a b c グリーンウッド, ノーマン; アーンショウ, アラン (1997). Chemistry of the Elements (英語) (2nd ed.). バターワース=ハイネマン. ISBN 978-0-08-037941-8。
- ^ Lebeau P. (1906). “The effect of fluorine on chloride and on bromine”. Annales de Chimie et de Physique 9: 241–263.
- ^ Simons JH (1950). “Bromine (III) Fluoride - Bromine Trifluoride”. Inorganic Synthesis 3: 184–186. doi:10.1002/9780470132340.ch48.
- ^ Gutmann V (1950). “Die Chemie in Bromtrifuoride”. Angewante Chemie 62: 312–315. doi:10.1002/ange.19500621305.
- ^ Meinert H (1967). “Interhalogenverbindungen”. Zeitschrift für Chemie 7: 41.
- ^ 神戸海難防止研究会 (PDF)
関連項目 編集
外部リンク 編集
| ハロゲン間化合物 | |||||
|---|---|---|---|---|---|
| フッ素 | 塩素 | 臭素 | ヨウ素 | アスタチン | |
| フッ素 | F2 | ||||
| 塩素 | ClF ClF3 ClF5 | Cl2 | |||
| 臭素 | BrF BrF3 BrF5 | BrCl BrCl3 | Br2 | ||
| ヨウ素 | IF IF3 IF5 IF7 | ICl I2Cl6 | IBr IBr3 | I2 | |
| アスタチン | AtCl | AtBr | AtI | At2? | |
