八硫黄
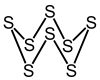
八硫黄(Octasulfur)またはオクタチオカン(octathiocane)は、S8の化学式を持つ無機化合物である。黄色の固体で、無色無味である。
| 八硫黄 | |
|---|---|
|

|

| |

| |
| 識別情報 | |
| CAS登録番号 | 10544-50-0 |
| PubChem | 66348 |
| ChemSpider | 59726 |
| MeSH | Cyclooctasulfur |
| ChEBI | |
| ChEMBL | CHEMBL1235452 |
| Gmelin参照 | 2973 |
| |
| 特性 | |
| 化学式 | S8 |
| モル質量 | 256.52 g mol−1 |
| 外観 | 鮮やかな黄色の透明の結晶 |
| 密度 | 2.07 g cm-3 |
| 融点 |
119 °C, 392 K, 246 °F |
| 沸点 |
159 °C, 432 K, 318 °F ((分解)) |
| log POW | 6.117 |
| 熱化学 | |
| 標準生成熱 ΔfH |
0 kJ・mol-1[2] |
| 標準モルエントロピー S |
32 J・mol-1・K-1[2] |
| 関連する物質 | |
| 関連物質 | 六硫黄 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
性質 編集
八硫黄は、菱面体晶と2つの単斜晶の合計3つの異なる多形として存在し、このうち2つだけが標準状態で安定である。菱面体晶のものが標準として扱われる。残りの多形は、100kPaで96℃から115℃の間でのみ安定で、115℃を超えるとゆっくりと不均化が起き始める。しかし、加熱が十分に急速だと、分解は最小限となり、八硫黄は119℃で溶解し、159℃以上で完全に分解する。
八硫黄は、いくつかの硫黄の同素体を形成する。
- α-硫黄
- β-硫黄
- γ-硫黄
- λ-硫黄
λ-硫黄は液体であり、これを冷却によって結晶化させることでγ-硫黄を得ることができる。λ-硫黄がゆっくり結晶化されると、β-硫黄に戻る。これは115℃以上に加熱されているはずなので、β-硫黄もγ-硫黄も純粋ではない。 純粋なγ-硫黄を得る既知の唯一の方法は、溶液からの結晶化である。
八硫黄は、容易に大きなサイズの結晶を生成する。これらの結晶の色は鮮やかな黄色であり、若干透明である。結晶になる化合物にはよくあることであるが、粉末状になった硫黄の外見はこれとは完全に異なり、図で見られるように色が薄く不透明である。
製法 編集
非常に純粋な八硫黄は、水溶性のピリジンを触媒とする4,4'-ジピリジルジスルフィドの光分解で作ることができる。多形の割合は、ピリジンと水の比によって変わる。この過程では、γ型の八硫黄も作られる。
出典 編集
- ^ “cyclooctasulfur (CHEBI:29385)”. Chemical Entities of Biological Interest. UK: European Bioinformatics Institute. 2014年7月24日閲覧。
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. p. A23. ISBN 0-618-94690-X