フェナントロリン
フェナントロリン(phenanthroline、phen)は、フェナントレンの炭素のうち2つを窒素で置換した複素環式化合物。化学式は、C12N2H8、分子量は180.21g/molで、窒素の位置によりいくつかの構造異性体が存在する。そのうち 1,10-フェナントロリンが遷移金属に対するキレート性配位子として用いられる[1]。有機溶媒に溶けやすく、水に微量溶ける塩基性物質である。フェナントロリンの性質の一部は2,2'-ビピリジン(英語版)と似ている。
| フェナントロリン | |
|---|---|
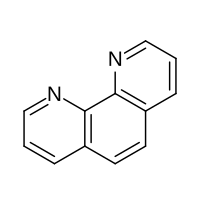
| |

| |
1,10-phenanthroline | |
| 識別情報 | |
| CAS登録番号 | 66-71-7 |
| ChemSpider | 1278 |
| DrugBank | DB02365 |
| ChEBI | |
| ChEMBL | CHEMBL415879 |
| RTECS番号 | SF8300000 |
| |
| |
| 特性 | |
| 化学式 | C12H8N2 |
| モル質量 | 180.21 g/mol |
| 外観 | 無色の結晶 |
| 密度 | 1.31 g/cm3 |
| 融点 |
117 °C, 390 K, 243 °F |
| 水への溶解度 | 中程度 |
| その他溶媒への溶解度 | アセトン、エタノール |
| 危険性 | |
| 主な危険性 | 軽度の神経毒、強い腎毒素、強い利尿効果 |
| Rフレーズ | R25, R50/53 |
| Sフレーズ | S45,S60,S61 |
| 関連する物質 | |
| 関連物質 | 2,2'-ビピリジン フェロイン フェナントレン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
1,10-フェナントロリンの鉄(II) 錯体はフェロイン (ferroin) と呼ばれ、電位の酸化還元指示薬(標準酸化還元電位 E0 = +1.06 V) として滴定分析、吸光光度分析に用いられる試薬である。
合成 編集
フェナントロリンは、スクラウプ反応で合成することができる。硫酸を触媒としてグリコールとo-フェニレンジアミンを反応させ、ヒ酸水溶液またはニトロベンゼンで酸化処理する[2]。グリコールの脱水によりアクロレインが生成し、アミンが付加、続けて環化が起こる。
フェロインと類似体 編集
フェナントロリンの鉄(II)錯体はフェロインと呼ばれ、化学式[Fe(phen)3]2+で表される[3]。フェロインは酸化還元指示薬として用いられる。標準電極電位は+1.06Vである。還元されたフェロインは赤を、酸化されたフェロインはライトブルーを呈する[4]。フェロインは細胞透過性があり、細胞内で金属プロテアーゼに対する酵素阻害剤として働く。
またニッケルの錯体([Ni(phen)3]2+)はピンク色をしており、Δ体とΛ体に分解する[5]。アナログであるルテニウム錯体([Ru(phen)3]2+)は古くから生理活性があることが知られている[6]。
出典 編集
- ^ C.R. Luman, F.N. Castellano "Phenanthroline Ligands" in Comprehensive Coordination Chemistry II, 2003, Elsevier. ISBN 978-0-08-043748-4.
- ^ B. E. Halcrow, W. O. Kermack (1946). “43. Attempts to find new antimalarials. Part XXIV. Derivatives of o-phenanthroline (7 : 8 : 3′ : 2′-pyridoquinoline)”. J. Chem. Soc.: 155–157. doi:10.1039/jr9460000155.
- ^ Belcher, R. "Application of chelate Compounds in Analytical Chemistry" Pure and Applied Chemistry, 1973, volume 34, pages 13-27.
- ^ Bellér, Gábor; Lente, Gábor; Fábián, István (2010). “Central Role of Phenanthroline Mono-N-oxide in the Decomposition Reactions of Tris(1,10-phenanthroline)iron(II) and -iron(III) Complexes”. Inorganic Chemistry 49 (9): 3968–3970. doi:10.1021/ic902554b. PMID 20415494.
- ^ ジョージ・カウフマン, Lloyd T. Takahashi (1966). “Resolution of the tris-(1,10-Phenanthroline)Nickel(II) Ion”. 無機合成 5: 227–232. doi:10.1002/9780470132395.ch60.
- ^ F. P. Dwyer, E. C. Gyarfas, W. P. Rogers, J. H. Koch (1952). “Biological Activity of Complex Ions”. ネイチャー 170 (4318): 190–191. doi:10.1038/170190a0. PMID 12982853.