ICAM-1
ICAM-1または細胞間接着分子1(さいぼうかんせっちゃくぶんし1、英: intercellular adhesion molecule 1)は、ヒトではICAM1遺伝子にコードされるタンパク質である[5][6]。CD54(cluster of differentiation 54)としても知られる。ICAM-1は細胞表面の糖タンパク質であり、一般的には血管内皮細胞と免疫系の細胞で発現している。CD11a/CD18、CD11b/CD18型のインテグリンに結合し、またライノウイルスが呼吸上皮に進入する際の受容体としても利用される[7]。
構造 編集
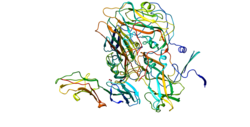
ICAM-1は免疫グロブリンスーパーファミリーのメンバーであり、このスーパーファミリーには抗体やT細胞受容体なども含まれる。ICAM-1は、N末端の細胞外ドメイン、1つの膜貫通ドメイン、C末端の細胞質ドメインから構成される膜貫通タンパク質である。ICAM-1の構造は高度なグリコシル化によって特徴づけられ、タンパク質の細胞外ドメインは分子内ジスルフィド結合によって形成された複数のループから構成される。タンパク質の主要な二次構造はβシートであり、二量体化ドメインが存在すると予想されている[8]。
機能 編集
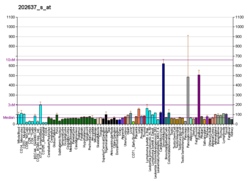
ICAM-1は白血球や血管内皮細胞の細胞膜に常に低濃度で存在する細胞間接着分子である。サイトカインによる刺激によって、その濃度は大きく上昇する。ICAM-1はIL-1とTNFによって誘導され、血管内皮、マクロファージ、リンパ球で発現する。ICAM-1の高度なグリコシル化と他の構造的特徴は多数のリガンドタンパク質の結合部位となっており、ICAM-1には免疫と関係した多数のリガンドの結合部位が存在する。特に、ICAM-1はMac-1、LFA-1やフィブリノゲンなど内皮細胞や白血球で一般的に発現しているタンパク質と結合し、血管外遊出や炎症応答など白血球が血管内皮を越えて移動する過程を促進する[9][10][11]。可溶性のLFA-1も発見されており、これはICAM-1に結合して遮断を行うようである[12]。こうした結合特性のため、ICAM-1は古典的な細胞間接着分子として認識されており、細胞間相互作用の安定化と白血球の内皮の通過の促進に重要であることが古くから知られている。
また、ICAM-1と可溶性ICAM-1は血液精巣関門を形成するタイトジャンクションに対して拮抗的作用を示し、精子形成に重要な役割を果たす[13]。
ICAM-1は大部分のヒトライノウイルスがさまざまな細胞種に進入する際の結合部位となっていることが発見されており、単なる接着分子以上の役割を持つことが示唆されている[8][14]。ICAM-1はマラリア原虫Plasmodium falciparumが感染した赤血球に対して親和性を持つようになることが知られており[15]、感染症におけるICAM-1の役割はより明確になりつつある。
こうした接着分子やウイルス進入分子としての古典的機能に加えて、ICAM-1はシグナル伝達の役割を持っていることが明らかになっている。ICAM-1のシグナル伝達機能は、主に炎症促進経路に関連しているようである。特に、ICAM-1によるシグナル伝達は、マクロファージや顆粒球などの炎症性免疫細胞のリクルートを引き起こすようである[16]。
また、ICAM-1はポジティブフィードバックループを形成してICAM-2と競合し、白血球の血管内皮への移行を助長する炎症性環境を維持している可能性がある。ICAM-1によるライゲーションはmRNAとタンパク質の両方のレベルで自身の発現をアップレギュレーションし、正のフィードバックループを形成することが判明している。さらに、ICAM-1によるライゲーションによって、RANTESのmRNAとタンパク質の発現が上昇することも判明している。RANTESは、顆粒球やマクロファージなどさまざまな炎症性免疫細胞に対する走化性を有する、炎症メディエーターのサイトカインである[17]。
臨床的意義 編集
ICAM-1はクモ膜下出血(SAH)への関与が示唆されている。健常人と比較してSAHの患者では、ICAM-1のレベルが大きく上昇していることが多くの研究で示されている[18][19]。SAHの患者の70%に影響を与える二次症状である脳血管攣縮とICAM-1との直接的な関係は示されていないが、抗ICAM-1治療は血管攣縮の重症度を低下させる。
呼吸上皮で発現しているICAM-1は、一般的なかぜの原因となるライノウイルスの結合部位ともなっている[20]。ICAM-1は腫瘍溶解性ウイルスであるコクサッキーウイルスA21(商標名: Cavatak、Viralytics社による開発)の進入のための主要な受容体でもある[21]。
カンナビノイド受容体CB2のアゴニストは、炎症性メディエーターにさらされたヒトの脳組織や脳微小血管内皮細胞(BMVEC)の表面でのICAM-1とVCAM-1の発現誘導を低下させることが示されている[22]。
相互作用 編集
ICAM-1はCD11a[23][24][25]、CD18[23][26][27]、エズリン[28]と相互作用することが示されている。
出典 編集
- ^ a b c GRCh38: Ensembl release 89: ENSG00000090339 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000037405 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ “Isolation and mapping of a polymorphic DNA sequence (pMCT108.2) on chromosome 18 [D18S24”]. Nucleic Acids Research 16 (9): 4188. (May 1988). doi:10.1093/nar/16.9.4188. PMC 336612. PMID 2453850.
- ^ “Chromosome mapping of cell membrane antigens expressed on activated B cells”. European Journal of Immunology 15 (1): 103–06. (Jan 1985). doi:10.1002/eji.1830150121. PMID 3871395.
- ^ “Entrez Gene: intercellular adhesion molecule 1”. 2021年5月4日閲覧。
- ^ a b “The structure of the two amino-terminal domains of human ICAM-1 suggests how it functions as a rhinovirus receptor and as an LFA-1 integrin ligand”. Proceedings of the National Academy of Sciences 95 (8): 4140–45. (Apr 1998). Bibcode: 1998PNAS...95.4140B. doi:10.1073/pnas.95.8.4140. PMC 22455. PMID 9539703.
- ^ “A human intercellular adhesion molecule (ICAM-1) distinct from LFA-1”. Journal of Immunology 137 (4): 1270–4. (August 1986). PMID 3525675.
- ^ “ICAM-1 regulates neutrophil adhesion and transcellular migration of TNF-alpha-activated vascular endothelium under flow”. Blood 106 (2): 584–92. (July 2005). doi:10.1182/blood-2004-12-4942. PMC 1635241. PMID 15811956.
- ^ Langer, Harald F.; Chavakis, Triantafyllos (2009-07). “Leukocyte-endothelial interactions in inflammation”. Journal of Cellular and Molecular Medicine 13 (7): 1211–1220. doi:10.1111/j.1582-4934.2009.00811.x. ISSN 1582-4934. PMC 2861890. PMID 19538472.
- ^ “Decreased plasma levels of soluble CD18 link leukocyte infiltration with disease activity in spondyloarthritis”. Arthritis Research & Therapy 16 (1): R42. (February 2014). doi:10.1186/ar4471. PMC 3978678. PMID 24490631.
- ^ “Intercellular adhesion molecules (ICAMs) and spermatogenesis”. Human Reproduction Update 19 (2): 167–86. (2013). doi:10.1093/humupd/dms049. PMC 3576004. PMID 23287428.
- ^ “Many rhinovirus serotypes share the same cellular receptor”. Journal of Virology 51 (2): 340–45. (Aug 1984). doi:10.1128/JVI.51.2.340-345.1984. PMC 254443. PMID 6086949.
- ^ Berendt, A. R.; Simmons, D. L.; Tansey, J.; Newbold, C. I.; Marsh, K. (1989-09-07). “Intercellular adhesion molecule-1 is an endothelial cell adhesion receptor for Plasmodium falciparum”. Nature 341 (6237): 57–59. doi:10.1038/341057a0. ISSN 0028-0836. PMID 2475784.
- ^ “ICAM-1-coupled signaling pathways in astrocytes converge to cyclic AMP response element-binding protein phosphorylation and TNF-alpha secretion”. Journal of Immunology 163 (2): 668–74. (Jul 1999). PMID 10395656.
- ^ “Selective regulation of ICAM-1 and RANTES gene expression after ICAM-1 ligation on human renal fibroblasts”. Journal of the American Society of Nephrology 14 (1): 116–27. (Jan 2003). doi:10.1097/01.ASN.0000040595.35207.62. PMID 12506144.
- ^ “Detection of soluble E-selectin, ICAM-1, VCAM-1, and L-selectin in the cerebrospinal fluid of patients after subarachnoid hemorrhage”. Journal of Neurosurgery 89 (4): 559–67. (Oct 1998). doi:10.3171/jns.1998.89.4.0559. PMID 9761049.
- ^ “Inflammatory cell adhesion molecules in ischemic cerebrovascular disease”. Stroke: A Journal of Cerebral Circulation 33 (8): 2115–22. (Aug 2002). doi:10.1161/01.STR.0000021902.33129.69. PMID 12154274.
- ^ Shukla, Shakti Dhar; Mahmood, Malik Quasir; Weston, Steven; Latham, Roger; Muller, Hans Konrad; Sohal, Sukhwinder Singh; Walters, Eugene Haydn (2017-01-05). “The main rhinovirus respiratory tract adhesion site (ICAM-1) is upregulated in smokers and patients with chronic airflow limitation (CAL)”. Respiratory Research 18 (1): 6. doi:10.1186/s12931-016-0483-8. ISSN 1465-993X. PMC 5217320. PMID 28056984.
- ^ “Viral targeting of non-muscle invasive bladder cancer and priming of anti-tumour immunity following intravesical Coxsackievirus A21”. Clinical Cancer Research 25 (19): 5818–5831. (July 2019). doi:10.1158/1078-0432.CCR-18-4022. PMID 31273010.
- ^ “Activation of cannabinoid receptor 2 attenuates leukocyte-endothelial cell interactions and blood-brain barrier dysfunction under inflammatory conditions”. The Journal of Neuroscience 32 (12): 4004–16. (March 2012). doi:10.1523/JNEUROSCI.4628-11.2012. PMC 3325902. PMID 22442067.
- ^ a b “Association of the membrane proximal regions of the alpha and beta subunit cytoplasmic domains constrains an integrin in the inactive state”. The Journal of Biological Chemistry 276 (18): 14642–48. (May 2001). doi:10.1074/jbc.M100600200. PMID 11279101.
- ^ “Structures of the alpha L I domain and its complex with ICAM-1 reveal a shape-shifting pathway for integrin regulation”. Cell 112 (1): 99–111. (Jan 2003). doi:10.1016/S0092-8674(02)01257-6. PMC 4372089. PMID 12526797.
- ^ “Synergistic inhibitory activity of alpha- and beta-LFA-1 peptides on LFA-1/ICAM-1 interaction”. Peptides 22 (12): 1955–62. (Dec 2001). doi:10.1016/S0196-9781(01)00546-0. PMID 11786177.
- ^ “ICAM-2 and a peptide from its binding domain are efficient activators of leukocyte adhesion and integrin affinity”. Journal of Immunology 162 (11): 6613–20. (Jun 1999). PMID 10352278.
- ^ “A binding interface on the I domain of lymphocyte function-associated antigen-1 (LFA-1) required for specific interaction with intercellular adhesion molecule 1 (ICAM-1)”. The Journal of Biological Chemistry 270 (32): 19008–16. (Aug 1995). doi:10.1074/jbc.270.32.19008. PMID 7642561.
- ^ “Association of ezrin with intercellular adhesion molecule-1 and -2 (ICAM-1 and ICAM-2). Regulation by phosphatidylinositol 4, 5-bisphosphate”. The Journal of Biological Chemistry 273 (34): 21893–900. (Aug 1998). doi:10.1074/jbc.273.34.21893. PMID 9705328.
関連文献 編集
- “Permissive factors for HIV-1 infection of macrophages”. Journal of Leukocyte Biology 68 (3): 303–10. (Sep 2000). PMID 10985244.
- “Targeting leukocyte integrins in human diseases”. Journal of Leukocyte Biology 77 (2): 129–40. (Feb 2005). doi:10.1189/jlb.0804460. PMID 15548573.
- “The role of ICAM-1 in Plasmodium falciparum cytoadherence”. European Journal of Cell Biology 84 (1): 15–27. (Jan 2005). doi:10.1016/j.ejcb.2004.09.002. PMID 15724813.
- “ICAM-1 co-stimulates target cells to facilitate antigen presentation”. Current Opinion in Immunology 17 (3): 251–58. (Jun 2005). doi:10.1016/j.coi.2005.04.008. PMID 15886114.
- “ICAM-1 regulates neutrophil adhesion and transcellular migration of TNF-alpha-activated vascular endothelium under flow”. Blood 106 (2): 584–92. (Jul 2005). doi:10.1182/blood-2004-12-4942. PMC 1635241. PMID 15811956.
外部リンク 編集
- Intercellular Adhesion Molecule-1 - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)