トリフルリジン
抗がん剤、抗ウイルス剤の一つ
トリフルリジン(Trifluridine)、別名トリフルオロチミジン(Trifluorothymidine、TFT)は、主に眼科で使用される抗ヘルペスウイルス薬である。グラクソ・スミスクラインに吸収されたグラクソ・ウェルカム社がViropticという商品名で販売していた。このブランドは現在、キング・ファーマシューティカルズが完全所有するモナーク・ファーマシューティカルズが所有している。
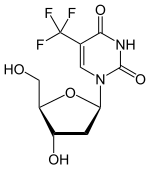 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Viroptic; Lonsurf (+tipiracil) |
| Drugs.com | monograph |
| ライセンス | EMA:リンク |
| 胎児危険度分類 |
|
| 法的規制 | |
| 投与経路 | Eye drops; tablets (+tipiracil) |
| 薬物動態データ | |
| 生物学的利用能 | Negligible (eye drops); ≥57% (oral) |
| 血漿タンパク結合 | >96% |
| 代謝 | Thymidine phosphorylase |
| 半減期 | 12 minutes (eye drops); 1.4–2.1 hrs (combination with tipiracil) |
| 排泄 | Mostly via urine |
| 識別 | |
| CAS番号 |
70-00-8 |
| ATCコード | S01AD02 (WHO) |
| PubChem | CID: 6256 |
| DrugBank |
DB00432 |
| ChemSpider |
6020 |
| UNII |
RMW9V5RW38 |
| KEGG |
D00391 |
| ChEBI |
CHEBI:75179 |
| ChEMBL |
CHEMBL1129 |
| 別名 | α,α,α-trifluorothymidine; 5-trifluromethyl-2′-deoxyuridine; FTD5-trifluoro-2′-deoxythymidine; TFT; CF3dUrd; FTD; F3TDR; F3Thd |
| 化学的データ | |
| 化学式 | C10H11F3N2O5 |
| 分子量 | 296.20 g·mol−1 |
| |
トリフルリジンは1980年に医療用として発売された[1]。日本では承認されていない。また、抗癌剤であるトリフルリジン・チピラシルの成分でもあり、この合剤は経口で服用される[2]。
参考資料
編集- ^ Long, Sarah S.; Pickering, Larry K.; Prober, Charles G. (2012) (英語). Principles and Practice of Pediatric Infectious Disease. Elsevier Health Sciences. p. 1502. ISBN 978-1437727029
- ^ “ロンサーフ配合錠T15/ロンサーフ配合錠T20 添付文書”. www.info.pmda.go.jp. 2021年9月20日閲覧。