ミトキサントロン
ミトキサントロン(Mitoxantrone)はアントラキノン系の癌化学療法剤の一つである。商品名ノバントロン。
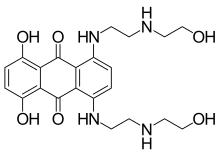 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Novantrone |
| Drugs.com | monograph |
| MedlinePlus | a608019 |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 投与経路 | Mainly intravenous |
| 薬物動態データ | |
| 生物学的利用能 | n/a |
| 血漿タンパク結合 | 78% |
| 代謝 | Hepatic (CYP2E1) |
| 半減期 | 75 hours |
| 排泄 | Renal |
| 識別 | |
| CAS番号 |
65271-80-9 |
| ATCコード | L01DB07 (WHO) |
| PubChem | CID: 4212 |
| IUPHAR/BPS | 7242 |
| DrugBank | DB01204 |
| ChemSpider |
4067 |
| UNII |
BZ114NVM5P |
| KEGG | D08224 |
| ChEBI | CHEBI:50729 |
| ChEMBL | CHEMBL58 |
| PDB ligand ID | MIX (PDBe, RCSB PDB) |
| 化学的データ | |
| 化学式 | C22H28N4O6 |
| 分子量 | 444.481 g/mol |
| |
効能・効果
編集ミトキサントロンは急性白血病(慢性骨髄性白血病の急性転化を含む)、悪性リンパ腫、乳癌、肝細胞癌への適応を持つ[1][2]。
ミトキサントロンとプレドニゾンの併用療法が転移性去勢抵抗性前立腺癌の第2選択治療として認められている。ドセタキセルとプレドニゾンの併用療法が生存率を改善し、無病生存期間を延長することが確かめられるまでは第1選択治療であった[3]。
ミトキサントロンは多発性硬化症(MS)の内二次性進行型MSの治療にも使われる。多発性硬化症を治癒させる治療法はなく、ミトキサントロンも多分に洩れないものの、二次性進行型MSの進行を遅らせて、再発寛解型MSと一次性進行型MSの再燃までの期間を延長することはできる[4]。
副作用
編集重大な副作用として、鬱血性心不全、心筋障害、心筋梗塞、貧血、白血球減少、血小板減少、出血、汎血球減少、間質性肺炎、ショック、アナフィラキシーがある[1]。
投与患者の5%以上に現れる副作用は上記の貧血、白血球減少、血小板減少のほか、肝機能検査値異常(AST(GOT)上昇、ALT(GPT)上昇、ALP上昇等)、血清ビリルビン上昇、悪心・嘔吐、食欲不振、口内炎、脱毛、発熱である。
そのほか、心障害や(遅発性の)免疫抑制が発現する。心筋症は不可逆性なので特に注意が必要である。心臓超音波検査や放射性核種血管造影での定期的モニタリングが推奨される。
心筋症のリスクがあるので、多発性硬化症患者へのミトキサントロンの生涯累積投与量(体表面積あたり)には限界がある[5]。
作用機序
編集ミトキサントロンはII 型トポイソメラーゼ阻害薬であり、正常細胞およびがん細胞の両方でDNA塩基間へのインターカレーションによってDNA合成とDNA修復を中断させる[7]。
関連項目
編集出典
編集- ^ a b “ノバントロン注10mg/ノバントロン注20mg 添付文書” (2016年9月). 2016年11月6日閲覧。
- ^ Parker C, Waters R, Leighton C, Hancock J, Sutton R, Moorman AV, Ancliff P, Morgan M, Masurekar A, Goulden N, Green N, Révész T, Darbyshire P, Love S, Saha V (2010). “Effect of mitoxantrone on outcome of children with first relapse of acute lymphoblastic leukaemia (ALL R3): an open-label randomised trial”. Lancet 376 (9757): 2009–2017. doi:10.1016/S0140-6736(10)62002-8. PMC 3010035. PMID 21131038.
- ^ Katzung, Bertram G. (2006). “Cancer Chemotherapy”. Basic and clinical pharmacology (10th ed.). New York: McGraw-Hill Medical Publishing Division. ISBN 0-07-145153-6. OCLC 157011367
- ^ Fox E (2006). “Management of worsening multiple sclerosis with mitoxantrone: a review”. Clin Ther 28 (4): 461–74. doi:10.1016/j.clinthera.2006.04.013. PMID 16750460.
- ^ “Mitoxantrone Hydrochloride (marketed as Novantrone and generics) - Healthcare Professional Sheet text version”. U.S. Food and Drug Administration. 2014年9月19日閲覧。
- ^ Wu, C. -C.; Li, Y. -C.; Wang, Y. -R.; Li, T. -K.; Chan, N. -L. (2013). “On the structural basis and design guidelines for type II topoisomerase-targeting anticancer drugs”. Nucleic Acids Research 41 (22): 10630–10640. doi:10.1093/nar/gkt828. PMID 24038465.
- ^ Mazerski J, Martelli S, Borowski E (1998). “The geometry of intercalation complex of antitumor mitoxantrone and ametantrone with DNA: molecular dynamics simulations.”. Acta Biochim. Pol. 45 (1): 1–11. PMID 9701490.
- ^ Baron M, Giorgi-Renault S, Renault J, et al. (1984). “Heterocycles with a quinone function.5.An abnormal reaction of butanedione with 1,2-diaminoanthraquinone - Crystalline structure obtained from naphto(2,3-f) quinoxaline-7,12 dione” (French). Can. J. Chem. 62 (3): 526–530. doi:10.1139/v84-087.