糖質コルチコイド受容体
糖質コルチコイド受容体またはグルココルチコイド受容体 (Glucocorticoid Receptor; GR) あるいはNR3C1(nuclear receptor subfamily 3, group C, member 1)はステロイド受容体(核内受容体)スーパーファミリーに属する分子である。リガンド非結合時においては細胞質に優位に存在する。ステロイドホルモンであるヒドロコルチゾンに対する受容体として働く一方、リガンド依存的に核内移行して転写因子としても働く。GRにはGRαとGRβの2つのスプライシングバリアントが存在する。
転写活性の発現
編集ステロイド系抗炎症薬を参照。
GRαとGRβ
編集GR遺伝子には9個のエキソンが存在し、3'末端側のエキソンの選択的スプライシングにより2種類のmRNAが産生される。それらが翻訳されてできたのがGRαとGRβである。
以下、ヒトのGR蛋白質について述べる。
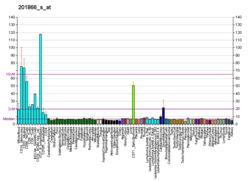
GRαは777アミノ酸残基からなる蛋白質であり、全身の組織に広く分布している。特に肝臓や腎臓、骨格筋、脳などで発現が高い。免疫制御や抗炎症作用、肺の成熟、糖新生、アポトーシスなどに関与している。その構造中にはN末端側からN末端ドメイン,DNA結合ドメイン,ヒンジ領域,リガンド結合ドメインが存在する。GRβはC末側のリガンド結合ドメインの一部が欠損しており、リガンド結合能を持たない。このため、GRβはドミナントネガティブ体として働くことが知られている。
翻訳後修飾
編集GRの機能はリン酸化、ユビキチン化などの翻訳後修飾により制御されている。
リン酸化
編集GRのリン酸化は大きく基底リン酸化(Basal Phosphorylation)と過剰リン酸化(Hyper Phosphorylation)に分けられる。過剰リン酸化はリガンド依存的に生じてGRの機能に影響を与えることから研究対象となることが多い。また、これらのリン酸化は細胞周期により制御されており、過剰リン酸化はS期に高く、G2/M期にはほとんど見られない。ヒトのGRの過剰リン酸化部位はN末端ドメインに5箇所存在し、全てSer残基である。
ユビキチン化
編集GRはリガンドが結合した後に翻訳後修飾としてリン酸化を受け、その後ユビキチン化を受けて分解を受けることが知られている。GRのプロテアソームによる分解はリガンドの結合によって生じた転写活性を制御するために存在する機構であると考えられている。
関連項目
編集出典
編集- ^ a b c GRCh38: Ensembl release 89: ENSG00000113580 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000024431 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference: