芳香族求核置換反応
芳香族求核置換反応(ほうこうぞくきゅうかくちかんはんのう)とは、化学反応のうち、ベンゼン環などの芳香環上にある置換基が、求核剤の攻撃を受けて置き換えられる反応のこと。一般にその形式は下式のように表され、基質と求核剤の種類により SNAr機構、SN1機構、SRN1機構、ベンザイン機構など、いくつかの反応機構が知られる。
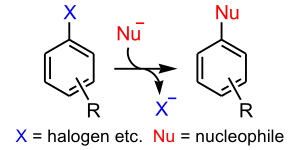
基質として主に用いられるのは芳香族ハロゲン化物である。ほか、芳香族ジアゾニウム化合物も反応性の高い基質である。ニトロ化合物が置換を受ける場合もある。
以下に、芳香族求核置換反応に知られる主な反応機構について解説する。脂肪族炭素上の求核置換反応は項目: 求核置換反応を参照のこと。
SNAr機構
編集SNAr機構は、ニトロ基などの電子求引基を持つ芳香族ハロゲン化物やピリミジンなど電子欠如型複素芳香環ハロゲン化物に見られる反応機構である。
- ハロゲンが結合している炭素(イプソ炭素)へ求核剤が攻撃し、付加体を作る。この付加体を「σ錯体」と呼ぶ。広義として「マイゼンハイマー錯体」と呼ぶこともある。
- σ錯体よりハロゲン化物イオンが脱離し、置換生成物を与える。
基質が持つ電子求引基は中間体の σ錯体の電荷を非局在化させて安定化するはたらきを持つ。ハロゲンの反応性は律速段階の場所によって異なり、求核剤の付加が律速である場合は F > Cl > Br, I と立体障害の小さな基質が有利であり、ハロゲン化物イオンの脱離が律速である場合は I > Br > Cl > F の順と、炭素-ハロゲン結合が弱い基質が有利となる。
このようにSNAr反応は付加-脱離という段階的な機構で進むと考えられていたが、原型的なSNAr反応は段階的ではなく協奏的に進行することが速度論的同位体効果と計算から示されている[1][2]。
SN1機構
編集SN1機構は、脂肪族の基質ではありふれた機構であるが、芳香族の場合はジアゾニウム化合物に限られる機構である。基質から窒素が脱離してアリールカチオンが生じ、求核剤を捕捉して置換生成物を与える。
この機構が稀である理由は、sp2炭素上のカチオンが、sp3炭素上のものに比べ不安定で生成しにくいためである。
ジアゾニウム化合物を基質とする人名反応のうち、シーマン反応の機構は SN1機構に近い。ザンドマイヤー反応はアリールラジカル、またはその銅錯体を経由すると考えられている。
SRN1機構
編集SRN1機構は、チオラート (RS−) など、還元性の高い求核剤を用いた場合に見られる機構である。連鎖反応が起こる点に特徴がある。各段階を順に追うと、
- Ar−X + Nu− → [Ar−X]−• + Nu•
- [Ar−X]−• → [Ar•] + X−
- [Ar•] + Nu− → [Ar−Nu]−•
- [Ar−Nu]−• + Ar−X → Ar−Nu + [Ar−X]−•
- まず、求核剤が還元剤としてはたらく。基質が 1電子還元を受け、アニオンラジカルに変わる。求核剤はラジカルとなって離れる。
- アニオンラジカルからハロゲン化物イオンが脱離し、アリールラジカルを与える。
- アリールラジカルと別の求核剤が結合し、新しいアニオンラジカルが生成する。
- そのアニオンラジカルが別の基質に電子を 1個与え、生成物となる。一方、ここで電子を与えられた基質は 2. の段階に戻り、(2. → 3. → 4. → 2. → ...) の反応サイクル(下図)が形成される。
SRN1機構において、ハロゲンの反応性の順番は、I > Br >> Cl であり、フッ化物はほとんど反応しない。
ベンザイン機構
編集フルオロベンゼンやクロロベンゼンなど、上記の反応機構において不活性な基質に強塩基を作用させるとベンザインが発生する。そこへ求核剤が付加すると、ハロゲンが置き換わった生成物が得られる。
例えば、液体アンモニア中においてクロロベンゼンに金属アミドを作用させるとアニリンに変わる。このとき、アミノ基が結合した炭素は、元々塩素が結合していた炭素、またはその隣(オルト位)の炭素ということになる。
身代わり求核置換反応
編集身代わり求核置換反応 (vicarious nucleophilic substitution、略称 VNS) と呼ばれる機構がある。炭素中心上に塩素などの脱離基と電子求引基を有するカルバニオン (Cl-CH--EWG) は、芳香族ニトロ化合物の水素と置き換わることができる。ニトロ基のオルト位にカルバニオンが付加したシグマ錯体からイプソ水素と脱離基が脱離し、再び芳香族化して置換生成物を与える。形式的には、求核剤上の脱離基が身代わりとなって脱離したことで、芳香環上のヒドリドを置換できたことになる[3]。
出典
編集- ^ Neumann, Constanze N.; Hooker, Jacob M.; Ritter, Tobias (2016). “Concerted nucleophilic aromatic substitution with 19F− and 18F−”. Nature 534 (7607): 369–373. doi:10.1038/nature17667. PMC 4911285. PMID 27281221.
- ^ Kwan, Eugene E.; Zeng, Yuwen; Besser, Harrison A.; Jacobsen, Eric N. (2018). “Concerted nucleophilic aromatic substitutions”. Nat. Chem.. doi:10.1038/s41557-018-0079-7.
- ^ Smith, M. B.; March, J. March's Advanced Organic Chemistry 6th ed. WILEY, 2007, chapter 10.
参考文献
編集- 鈴木仁美 著『有機反応II』、丸山和博 編、丸善、1984年。