リプレッサー
分子遺伝学においてリプレッサー(英: repressor)は、オペレーターまたは関連するサイレンサーに結合することで遺伝子の発現を阻害する、DNA結合タンパク質またはRNA結合タンパク質である。DNAに結合するリプレッサーはプロモーターへのRNAポリメラーゼの結合をブロックし、遺伝子のmRNAへの転写を防ぐ。RNAに結合するリプレッサーはmRNAに結合し、mRNAからタンパク質への翻訳を防ぐ。こうしてもたらされる遺伝子発現の低下は、抑制(リプレッション、repression)と呼ばれる。
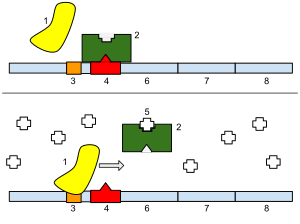
機能 編集
遺伝子発現を開始する分子であるインデューサーが存在する場合、インデューサーはリプレッサータンパク質と相互作用し、リプレッサーをオペレーターから除去する。その後、RNAポリメラーゼは遺伝子を転写する(遺伝子を発現する)ことができるようになる。この抑制機構はインデューサーの存在など特定の条件下でのみ転写を可能にし、一種のフィードバック機構を形成していることが多い。
コリプレッサーはリプレッサーに結合する分子で、リプレッサーがオペレーターへより強固に結合できるようにすることで転写を低下させる。コリプレッサーと結合することでオペレーターに結合するタイプのリプレッサーは、アポリプレッサー(aporepressor)または不活性リプレッサー(inactive repressor)と呼ばれている。アポリプレッサーの例としては、細菌の重要な代謝タンパク質であるトリプトファンリプレッサーが挙げられる。対照的に活性リプレッサー(active repressor)はオペレーターに直接結合し、転写を低下させる。
リプレッサーの例 編集
lacオペロンリプレッサー 編集
lacZYAオペロンはラクトースの分解に必要なタンパク質をコードする遺伝子を含んでいる。lacI遺伝子は一般に「lacリプレッサー」と呼ばれるタンパク質をコードし、lacオペロンのリプレッサーとして機能する。lacI遺伝子はlacZYAのすぐ上流に位置するが、転写はlacオペロンのプロモーターとは異なるlacIプロモーターから行われる。lacI遺伝子はLacIリプレッサータンパク質を合成し、LacIリプレッサータンパク質はオペレーター配列lacOに結合してlacZYAを抑制する[1]。
lacリプレッサーは恒常的に発現しており、通常はlacOに結合してRNAポリメラーゼによるlacオペロンの転写の開始を阻害している。リプレッサーはインデューサーであるアロラクトースの存在下でコンフォメーション変化を起こし、DNA結合強度が低下してlacO配列から解離する。その後、RNAポリメラーゼはlacオペロンのプロモーターに結合してlacZYA遺伝子の転写を開始できるようになる[1]。
metオペロンリプレッサー 編集
リプレッサータンパク質の他の例としては、メチオニンリプレッサーMetJがある。MetJはリボン-ヘリックス-ヘリックス(RHH)モチーフを介してDNAと相互作用する[2]。MetJは2つの単量体から構成されるホモ二量体である。各単量体のβリボンは共に逆平行βシートを形成し、Met boxと呼ばれるオペレーター配列にDNAの主溝側から結合する。結合したMetJ二量体は、オペレーター配列の相補鎖に結合した他のMetJ二量体とαヘリックスを介して相互作用する。
Met boxはAGACGTCTからなる回文配列で、DNAのどちらの鎖でも同じ配列が認識される。Met boxの中央に位置するCとGの間の接合部にはピリミジン-プリンステップが含まれており、ホスホジエステル骨格が屈曲して正の超らせんが形成される。タンパク質は、DNA二重らせんの形状がタンパク質の形状に沿うことで、認識部位を確認する。言い換えると、タンパク質は特定の塩基配列を認識するのではなく、DNAの構造パラメータを間接的に読み取ることで認識が行われる。
MetJ二量体には2つの補因子S-アデノシルメチオニン(SAM)結合部位が存在する。SAMはメチオニン生合成の産物である。MetJのSAM結合ポケットはDNA結合部位とは重複していない。SAMはMetJに結合してMetJのオペレーター部位への親和性を高め、メチオニン合成に関係する遺伝子の転写を停止させる。SAM濃度が低くなると、リプレッサーはオペレーター部位から解離し、より多くのメチオニンが合成されるようになる。
L-アラビノースオペロンリプレッサー 編集
L-アラビノースオペロンにはアラビノースを分解する酵素が含まれている。これらの酵素は、グルコース濃度が低いか存在しないときに代替的なエネルギー源としてアラビノースを分解する役割を果たす[3]。オペロンはリプレッサー遺伝子(araC)、4つの制御部位(araO2、araO1、araI1、araI2)、2つのプロモーター(Parac/ParaBAD)、3つの構造遺伝子(araBAD)から構成される。AraCは合成されると制御部位に結合してループを形成し、RNAポリメラーゼのプロモーター領域への結合と構造遺伝子の転写を防ぐリプレッサーとして機能する。
アラビノースもAraCも存在しない場合、ループ形成は開始されないが構造遺伝子の発現は低い状態である。アラビノースは存在しないがAraCが存在する場合、AraCは二量体を形成してaraO2とaraI1に結合し、ループ形成によってaraO2とaraI1を近接させる[4]。アラビノースとAraCの双方が存在する場合、AraCはアラビノースと結合し、アクチベーターとして機能する。AraCはアラビノースの結合に伴うコンフォメーション変化によってループを形成することができなくなり、線形となった遺伝子領域はaraBAD領域へのRNAポリメラーゼのリクルートを促進する[3]。
Flowing Locus C(エピジェネティックリプレッサー) 編集
シロイヌナズナArabidopsis thalianaのFlowering Locus C(FLC)オペロンは、開花のためのメリステムの発達に必要な遺伝子を抑制することで、開花を負に制御している。FLCの発現はFRIGIDAの存在によって調節されていることが示されており、温度の低下と負に相関して春化を防いでいる[5]。発現低下の程度は、季節の進行に伴う温度や露光時間の変化に依存している。FLCの発現がダウンレギュレーションされると、開花の可能性が出てくる。FLCの発現調節には、遺伝的な要因とヒストンのメチル化やDNAメチル化などのエピジェネティックな要因が関係している[6]。さらに、FLC遺伝子の負の転写因子として働くコファクターとなる遺伝子も多数存在する[7]。また、FLC遺伝子には種を超えて多数の相同な遺伝子が存在し、さまざまな気候での適応を可能にしている[8]。
出典 編集
- ^ a b Slonczewski, Joan (2009). Microbiology : an evolving science. John Watkins Foster (1st ed ed.). New York: W.W. Norton & Co. ISBN 978-0-393-97857-5. OCLC 185042615
- ^ Somers & Phillips (1992). “Crystal structure of the met repressor-operator complex at 2.8 A resolution reveals DNA recognition by beta-strands.”. Nature 359 (6394): 387–393. doi:10.1038/359387a0. PMID 1406951.
- ^ a b Voet, Donald (2011). Biochemistry. Voet, Judith G. (4th ed.). Hoboken, NJ: John Wiley & Sons. ISBN 978-0-470-57095-1. OCLC 690489261
- ^ Harmer, Tara; Wu, Martin; Schleif, Robert (2001-01-16). “The role of rigidity in DNA looping-unlooping by AraC” (英語). Proceedings of the National Academy of Sciences 98 (2): 427–431. Bibcode: 2001PNAS...98..427H. doi:10.1073/pnas.98.2.427. ISSN 0027-8424. PMC 14602. PMID 11209047.
- ^ Shindo, Chikako; Aranzana, Maria Jose; Lister, Clare; Baxter, Catherine; Nicholls, Colin; Nordborg, Magnus; Dean, Caroline (June 2005). “Role of FRIGIDA and FLOWERING LOCUS C in Determining Variation in Flowering Time of Arabidopsis”. Plant Physiology 138 (2): 1163–1173. doi:10.1104/pp.105.061309. ISSN 0032-0889. PMC 1150429. PMID 15908596.
- ^ Johanson, U.; West, J.; Lister, C.; Michaels, S.; Amasino, R.; Dean, C. (2000-10-13). “Molecular analysis of FRIGIDA, a major determinant of natural variation in Arabidopsis flowering time”. Science 290 (5490): 344–347. Bibcode: 2000Sci...290..344J. doi:10.1126/science.290.5490.344. ISSN 0036-8075. PMID 11030654.
- ^ Finnegan, E. Jean; Kovac, Kathryn A.; Jaligot, Estelle; Sheldon, Candice C.; Peacock, W. James; Dennis, Elizabeth S. (2005). “The downregulation of FLOWERING LOCUS C (FLC) expression in plants with low levels of DNA methylation and by vernalization occurs by distinct mechanisms” (英語). The Plant Journal 44 (3): 420–432. doi:10.1111/j.1365-313X.2005.02541.x. ISSN 1365-313X. PMID 16236152.
- ^ Sharma, Neha; Ruelens, Philip; D'hauw, Mariëlla; Maggen, Thomas; Dochy, Niklas; Torfs, Sanne; Kaufmann, Kerstin; Rohde, Antje et al. (February 2017). “A Flowering Locus C Homolog Is a Vernalization-Regulated Repressor in Brachypodium and Is Cold Regulated in Wheat1[OPEN”]. Plant Physiology 173 (2): 1301–1315. doi:10.1104/pp.16.01161. ISSN 0032-0889. PMC 5291021. PMID 28034954.
関連項目 編集
外部リンク 編集
- Repressor Proteins - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)