塩化ホルミウム(III)
塩化ホルミウム(III)(Holmium(III) chloride)は、化学式HoCl3の無機化合物である。主に研究に用いられる。純粋なホルミウムを作るのに用いることができる[2]。酸化ホルミウム(III)と同じ色の変化を見せ、自然光の下では黄色、蛍光の下では明るい桃色になる。
| 塩化ホルミウム(III) | |
|---|---|
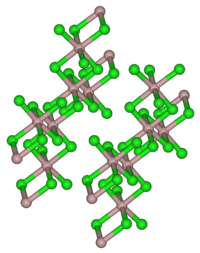
| |
別称 Holmium trichloride Holmiumchlorid | |
| 識別情報 | |
| CAS登録番号 | 10138-62-2 |
| PubChem | 24992 |
| UNII | CAR334HOLD |
| 特性 | |
| 化学式 | HoCl3 |
| モル質量 | 271.289 g/mol |
| 外観 | 黄色結晶 吸湿性 |
| 密度 | 3.7 g/cm3 |
| 融点 |
720 °C, 993 K, 1328 °F [1] |
| 沸点 |
1500 °C, 1773 K, 2732 °F ((分解)) |
| 水への溶解度 | 溶解 |
| 構造 | |
| 結晶構造 | 単斜晶系, mS16 |
| 空間群 | C12/m1, No. 12 |
| 関連する物質 | |
| その他の陰イオン | 酸化ホルミウム(III) |
| その他の陽イオン | 塩化ジスプロシウム(III), 酸化エルビウム(III) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
合成
編集塩化ホルミウム(III)合成の最も一般的な方法では、酸化ホルミウム(III)と塩化アンモニウムの混合物を200-250℃に加熱する[3]。
- Ho2O3 + 6 NH4Cl → 2 HoCl3 + 6 NH3 + 2 H2O
ホルミウムと塩酸の反応では、塩化ホルミウム(III)の六水和物が得られる[3]。
- 2 Ho + 6 HCl → 2 HoCl3 + 3 H2
- 2 Ho + 3 Cl2 → 2 HoCl3
性質
編集塩化ホルミウム(III)とその六水和物は、日光の下では明るい黄色の固体であり、水に可溶である。六水和物は、64℃で結晶水を遊離し始める[5]。単斜晶系で、塩化アルミニウム(III)のアナログである[3]。固相では、YCl3の層状構造を持つ[6]。
出典
編集- ^ Lide, David R., ed (2006). CRC Handbook of Chemistry and Physics (87th ed.). Boca Raton, FL: CRC Press. ISBN 0-8493-0487-3
- ^ Emsley, John (2003). Nature's building blocks: an A-Z guide to the elements (Reprinted with corrections ed.). Oxford: Oxford Univ. Press. ISBN 978-0-19-850340-8
- ^ a b c Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY.
- ^ Webelements: Holmium
- ^ Ans, Jan d'; Ans, Jan d' (1998). Elemente, anorganische Verbindungen und Materialien. Taschenbuch für Chemiker und Physiker / D'Ans (4., neubearb. u. rev. Aufl ed.). Ort nicht ermittelbar: Verlag nicht ermittelbar. ISBN 978-3-540-60035-0
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford. ISBN 0-19-855370-6