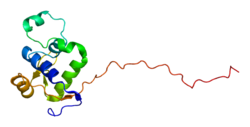
WRN
WRN(Werner syndrome ATP-dependent helicase)は、ヒトではWRN遺伝子にコードされる酵素である。RECQ3(DNA helicase, RecQ-like type 3)としても知られ、RecQヘリカーゼファミリーの一員である[5]。一般的に、ヘリカーゼは二本鎖DNAを巻き戻して分離する。こうした活性は、細胞分裂に備えてDNAをコピーする際(DNA複製)に必要である。転写と呼ばれる、タンパク質産生のための鋳型形成の際にもヘリカーゼは重要である。WRNタンパク質はDNA修復にも重要な役割を果たしていることが示唆されている。このタンパク質はDNAの構造と完全性の維持を助けている。
構造と機能 編集
WRNはRecQヘリカーゼファミリーの一員である。また、3'→5'エキソヌクレアーゼ活性を持つ唯一のRecQヘリカーゼである。エキソヌクレアーゼ活性によって、3'陥凹末端の分解や二本鎖DNA中のギャップからのDNA分解の開始などが行われる。WRNは相同組換え[6][7]や非相同末端結合[8]による二本鎖切断修復、塩基除去修復による一塩基損傷の修復[5][9][10]に重要であり、複製停止からの回復に効果的である[11]。WRNはテロメアの維持と複製、特にGリッチ配列の複製に重要である可能性がある[12]。
WRNはオリゴマーであり、DNAの巻き戻し時には単量体として作用する一方で、溶液中では二量体、DNAとの複合体形成時には四量体を形成し、また六量体を形成することも観察されている。WRNの拡散速度は核質では1.62 、核小体では0.12 と測定されている[13]。WRNのオルソログは、ショウジョウバエ、ツメガエル、C. elegansなど他の多数の生物にも存在する。WRNはゲノム安定性に重要であり、WRNに変異を有する細胞はDNA損傷やDNA切断に対する感受性が高くなる[14]。
WRNのN末端はヘリカーゼ活性とヌクレアーゼ活性の双方に関与しており、C末端は重要ながん抑制因子であるp53と相互作用する[15]。WRNはDNA修復、組換え、複製やDNA二次構造の解消時にエキソヌクレアーゼとして機能している可能性がある。WRNはホリデイジャンクションにおける分岐点移動に関与しており、その他のDNA複製中間体とも相互作用する[11]。WRNをコードするmRNAはヒトの大部分の組織で同定されている[15]。
翻訳後修飾 編集
WRNのセリン/スレオニン残基のリン酸化は、複製後DNA修復に重要なヘリカーゼ活性とエキソヌクレアーゼ活性を阻害する。これらの部位の脱リン酸化はWRNの触媒活性を亢進する。リン酸化は、SUMO化やアセチル化などの他の翻訳後修飾に影響を与えている可能性がある[12]。
臨床的意義 編集
ウェルナー症候群はWRN遺伝子の変異によって引き起こされる[15]。WRN遺伝子の原因となる変異として20種類以上が知られている。こうした変異の多くは、異常に短いWRNタンパク質を産生するものである。こうした短縮型タンパク質は、DNAと相互作用を行うための細胞核への移行が起こらないことが示唆されている[16]。また、こうした短縮型タンパク質は迅速に分解される可能性があり、細胞内のWRNタンパク質の喪失が引き起こされる。核内に正常なWRNタンパク質が存在しない場合、細胞はDNA複製、修復、転写を行うことができない[17]。これらの変異がウェルナー症候群でみられる早老の症状を引き起こす機構については現在も研究が行われている。
DNA修復経路における役割 編集
相同組換え修復 編集
WRNは相同組換えに活性を有する。WRN遺伝子に欠陥を有する細胞は有糸分裂時の自発的な組換えが23分の1に低下し、特に遺伝子変換型の組換えが減少する[18]。WRN遺伝子に欠陥を有する細胞は、野生型WRNを持つ細胞と比較して、X線に曝露した場合の染色体切断や小核形成が増加する[19]。WRN遺伝子に欠陥を有する細胞は、野生型細胞よりもガンマ線、紫外線、シクロブタン型ピリミジンダイマー、マイトマイシンCに対する感受性は高くならないが、I型、II型トポイソメラーゼ阻害剤に対する感受性が高くなる[20]。これらの知見は、WRNタンパク質が相同組換え修復や停止した複製フォークのプロセシングに関与していることを示唆している[21]。
非相同末端結合 編集
WRNは非相同末端結合(NHEJ)によるDNA修復にも重要な役割を果たしている。WRNは二本鎖切断部位にリクルートされ、そこでNHEJ経路において酵素的・非酵素的な機能を果たす。二本鎖切断部位ではKuと結合して標準的(典型的)NHEJ経路を促進し、その酵素機能によってDNA二本鎖切断をある程度の正確さで修復する。WRNはalt-NHEJまたはマイクロホモロジー媒介末端結合(MMEJ)と呼ばれるNHEJの代替的経路を阻害する。MMEJは二本鎖切断の不正確な修復機構である[8]。
塩基除去修復 編集
WRNはDNAの塩基除去修復(BER)にも関与している。WRNはBERの序盤の損傷検出段階でNEIL1と結合し、NEIL1による酸化損傷の除去を促進する[9]。NEIL1はDNAグリコシラーゼであり、活性酸素種(ROS)によって損傷した塩基を切除しすることでBERの第一段階を開始し、またNEIL1と関連したリアーゼ活性によってDNA鎖に切断が導入される[22]。NEIL1はROSによって損傷した塩基を認識して除去し、その後3'側と5'側ににリン酸基を残してβ,δ脱離によって無塩基部位を除去する。NEIL1は酸化ピリミジン、ホルムアミドピリミジン、メチル基が酸化されたチミン、チミングリコールの双方の立体異性体を認識する[23]。
WRNはPolλとの相互作用を介してもBERに関与する[10]。WRNはPolλの触媒ドメインに結合し、8-oxo-Gの反対側のギャップの埋め込みとその後の鎖置換合成を特異的に促進する。これによってWRNはMUTYHによって開始される8-oxo-G:Aミスペアの修復時のPolλによるロングパッチBERを促進する。
複製停止からの回復 編集
WRNは複製停止からの回復にも関与している。WRNに欠陥がある場合、複製の停止は二本鎖切断の蓄積と染色体断片化の増加を引き起こす[24]。WRNは、複製チェックポイントの中心的因子の1つであるRAD9-RAD1-HUS1(9.1.1)複合体と相互作用する[24]。この相互作用はWRNのN末端領域へのRAD1サブユニットの結合によって媒介され、核内のfociへのWRNの再局在と複製停止に応答したWRNのリン酸化に重要である。DNA損傷や複製フォークの停止が起こっていない場合、WRNは核小体に局在したままである[25]。WRNと9.1.1複合体との相互作用は、停止した複製フォークでの二本鎖切断の形成を防ぐ[24]。
がんにおけるWRNの欠乏 編集
限られた量のWRNを発現する細胞は、野生型細胞と比較して変異頻度が上昇する[26]。変異の増加はがんの発生の原因となる可能性がある。ウェルナー症候群の患者はWRN遺伝子にホモ接合型変異を抱えており、軟部肉腫、骨肉腫、甲状腺がんやメラノーマなどのがんの発生率が上昇する[27]。
WRNの変異は一般集団では稀である。WRNのヘテロ接合型機能喪失変異は約100万人に1人である。日本人集団では1000人あたり6人と比較的高いが、それでも低頻度である[28]。
がん細胞ではWRN遺伝子の変異による欠陥よりも、エピジェネティックな変化による発現の低下が広くみられ、下の図では630のヒト原発性腫瘍におけるWRN遺伝子のCpGアイランドの高メチル化の頻度を示している[29]。高メチル化はWRNの発現の低下を引き起こし、腫瘍形成時に広くみられる現象である[29]。
| がん | 頻度[29] |
|---|---|
| 大腸がん | 37.9% |
| 非小細胞性肺がん | 37.5% |
| 胃がん | 25% |
| 前立腺がん | 20% |
| 乳がん | 17.2% |
| 甲状腺がん | 12.5% |
| 非ホジキンリンパ腫 | 23.7% |
| 急性骨髄性白血病 | 4.8% |
| 軟骨肉腫 | 33.3% |
| 骨肉腫 | 11.1% |
相互作用 編集
WRNは次に挙げる因子と相互作用することが示されている。
出典 編集
- ^ a b c GRCh38: Ensembl release 89: ENSG00000165392 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000031583 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ a b Monnat RJ (October 2010). “Human RECQ helicases: roles in DNA metabolism, mutagenesis and cancer biology”. Semin. Cancer Biol. 20 (5): 329–39. doi:10.1016/j.semcancer.2010.10.002. PMC 3040982. PMID 20934517.
- ^ “Homologous recombination resolution defect in werner syndrome”. Mol. Cell. Biol. 22 (20): 6971–8. (2002). doi:10.1128/mcb.22.20.6971-6978.2002. PMC 139822. PMID 12242278.
- ^ “DNA2 cooperates with the WRN and BLM RecQ helicases to mediate long-range DNA end resection in human cells”. J. Biol. Chem. 289 (39): 27314–26. (2014). doi:10.1074/jbc.M114.578823. PMC 4175362. PMID 25122754.
- ^ a b “WRN regulates pathway choice between classical and alternative non-homologous end joining”. Nat Commun 7: 13785. (2016). Bibcode: 2016NatCo...713785S. doi:10.1038/ncomms13785. PMC 5150655. PMID 27922005.
- ^ a b “The human Werner syndrome protein stimulates repair of oxidative DNA base damage by the DNA glycosylase NEIL1”. J. Biol. Chem. 282 (36): 26591–602. (2007). doi:10.1074/jbc.M703343200. PMID 17611195.
- ^ a b “Involvement of Werner syndrome protein in MUTYH-mediated repair of oxidative DNA damage”. Nucleic Acids Res. 40 (17): 8449–59. (2012). doi:10.1093/nar/gks648. PMC 3458577. PMID 22753033.
- ^ a b “The Werner syndrome protein: linking the replication checkpoint response to genome stability”. Aging 3 (3): 311–8. (2011). doi:10.18632/aging.100293. PMC 3091524. PMID 21389352.
- ^ a b “Model of human aging: recent findings on Werner's and Hutchinson–Gilford progeria syndromes”. Clin Interv Aging 3 (3): 431–44. (2008). doi:10.2147/CIA.S1957. PMC 2682376. PMID 18982914.
- ^ Kristian Moss Bendtsen, Martin Borch Jensen, Alfred May, Lene JuelRasmussen, Ala Trusina, Vilhelm A. Bohr & Mogens H. Jensen (2014). “Dynamics of the DNA repair proteins WRN and BLM in the nucleoplasm and nucleoli”. European Biophysics Journal 43 (10–11): 509–16. doi:10.1007/s00249-014-0981-x. PMC 5576897. PMID 25119658.
- ^ “Roles of Werner syndrome protein in protection of genome integrity”. DNA Repair (Amst.) 9 (3): 331–44. (2010). doi:10.1016/j.dnarep.2009.12.011. PMC 2827637. PMID 20075015.
- ^ a b c Oshima J (2000). “The Werner syndrome protein: an update”. BioEssays 22 (10): 894–901. doi:10.1002/1521-1878(200010)22:10<894::AID-BIES4>3.0.CO;2-B. PMID 10984715.
- ^ “The spectrum of WRN mutations in Werner syndrome patients”. Hum. Mutat. 27 (6): 558–67. (2006). doi:10.1002/humu.20337. PMC 1868417. PMID 16673358.
- ^ Lebel M (2001). “Werner syndrome: genetic and molecular basis of a premature aging disorder”. Cell. Mol. Life Sci. 58 (7): 857–67. doi:10.1007/s00018-001-8398-y. PMID 11497235.
- ^ “Loss of Werner syndrome protein function promotes aberrant mitotic recombination”. Genes Dev. 15 (8): 933–8. (2001). doi:10.1101/gad.877001. PMC 312674. PMID 11316787.
- ^ “Correlation between senescence and DNA repair in cells from young and old individuals and in premature aging syndromes”. Mutat. Res. 316 (1): 37–48. (1994). doi:10.1016/0921-8734(94)90006-x. PMID 7507567.
- ^ “A deletion within the murine Werner syndrome helicase induces sensitivity to inhibitors of topoisomerase and loss of cellular proliferative capacity”. Proc. Natl. Acad. Sci. U.S.A. 95 (22): 13097–102. (1998). Bibcode: 1998PNAS...9513097L. doi:10.1073/pnas.95.22.13097. PMC 23722. PMID 9789047.
- ^ “Werner helicase relocates into nuclear foci in response to DNA damaging agents and co-localizes with RPA and Rad51”. Genes Cells 6 (5): 421–30. (2001). doi:10.1046/j.1365-2443.2001.00433.x. PMID 11380620.
- ^ “Inhibition of DNA glycosylases via small molecule purine analogs”. PLOS ONE 8 (12): e81667. (2013). Bibcode: 2013PLoSO...881667J. doi:10.1371/journal.pone.0081667. PMC 3857224. PMID 24349107.
- ^ “Variant base excision repair proteins: contributors to genomic instability”. Seminars in Cancer Biology 20 (5): 320–8. (Oct 2010). doi:10.1016/j.semcancer.2010.10.010. PMC 3254599. PMID 20955798.
- ^ a b c “The RAD9-RAD1-HUS1 (9.1.1) complex interacts with WRN and is crucial to regulate its response to replication fork stalling”. Oncogene 31 (23): 2809–23. (2012). doi:10.1038/onc.2011.468. PMC 3272477. PMID 22002307.
- ^ “Werner's syndrome protein (WRN) migrates Holliday junctions and co-localizes with RPA upon replication arrest”. EMBO Rep. 1 (1): 80–4. (2000). doi:10.1093/embo-reports/kvd004. PMC 1083680. PMID 11256630.
- ^ “The Werner syndrome exonuclease facilitates DNA degradation and high fidelity DNA polymerization by human DNA polymerase δ”. J. Biol. Chem. 287 (15): 12480–90. (2012). doi:10.1074/jbc.M111.332577. PMC 3320997. PMID 22351772.
- ^ “Excess of rare cancers in Werner syndrome (adult progeria)”. Cancer Epidemiol. Biomarkers Prev. 5 (4): 239–46. (1996). PMID 8722214.
- ^ “The Werner's Syndrome RecQ helicase/exonuclease at the nexus of cancer and aging”. Hawaii Med J 70 (3): 52–5. (2011). PMC 3071901. PMID 21365542.
- ^ a b c “Epigenetic inactivation of the premature aging Werner syndrome gene in human cancer”. Proc. Natl. Acad. Sci. U.S.A. 103 (23): 8822–7. (2006). Bibcode: 2006PNAS..103.8822A. doi:10.1073/pnas.0600645103. PMC 1466544. PMID 16723399.
- ^ “Colocalization, physical, and functional interaction between Werner and Bloom syndrome proteins”. J. Biol. Chem. 277 (24): 22035–44. (June 2002). doi:10.1074/jbc.M200914200. PMID 11919194.
- ^ “Substrate specificities and identification of putative substrates of ATM kinase family members”. J. Biol. Chem. 274 (53): 37538–43. (Dec 1999). doi:10.1074/jbc.274.53.37538. PMID 10608806.
- ^ “Werner protein is a target of DNA-dependent protein kinase in vivo and in vitro, and its catalytic activities are regulated by phosphorylation”. J. Biol. Chem. 277 (21): 18291–302. (May 2002). doi:10.1074/jbc.M111523200. PMID 11889123.
- ^ “Stimulation of flap endonuclease-1 by the Bloom's syndrome protein”. J. Biol. Chem. 279 (11): 9847–56. (March 2004). doi:10.1074/jbc.M309898200. PMID 14688284.
- ^ “Werner syndrome protein interacts with human flap endonuclease 1 and stimulates its cleavage activity”. EMBO J. 20 (20): 5791–801. (October 2001). doi:10.1093/emboj/20.20.5791. PMC 125684. PMID 11598021.
- ^ a b “Ku heterodimer binds to both ends of the Werner protein and functional interaction occurs at the Werner N-terminus”. Nucleic Acids Res. 30 (16): 3583–91. (August 2002). doi:10.1093/nar/gkf482. PMC 134248. PMID 12177300.
- ^ a b “Functional interaction between Ku and the werner syndrome protein in DNA end processing”. J. Biol. Chem. 275 (37): 28349–52. (September 2000). doi:10.1074/jbc.C000289200. PMID 10880505.
- ^ “The processing of Holliday junctions by BLM and WRN helicases is regulated by p53”. J. Biol. Chem. 277 (35): 31980–7. (August 2002). doi:10.1074/jbc.M204111200. PMID 12080066.
- ^ “p53 Modulates the exonuclease activity of Werner syndrome protein”. J. Biol. Chem. 276 (37): 35093–102. (September 2001). doi:10.1074/jbc.M103332200. PMID 11427532.
- ^ “Characterisation of the interaction between WRN, the helicase/exonuclease defective in progeroid Werner's syndrome, and an essential replication factor, PCNA”. Mech. Ageing Dev. 124 (2): 167–74. (February 2003). doi:10.1016/S0047-6374(02)00131-8. PMID 12633936.
- ^ “Characterization of the human and mouse WRN 3'-->5' exonuclease”. Nucleic Acids Res. 28 (12): 2396–405. (June 2000). doi:10.1093/nar/28.12.2396. PMC 102739. PMID 10871373.
- ^ “Telomere-binding protein TRF2 binds to and stimulates the Werner and Bloom syndrome helicases”. J. Biol. Chem. 277 (43): 41110–9. (October 2002). doi:10.1074/jbc.M205396200. PMID 12181313.
- ^ “A novel protein interacts with the Werner's syndrome gene product physically and functionally”. J. Biol. Chem. 276 (23): 20364–9. (June 2001). doi:10.1074/jbc.C100035200. PMID 11301316.
関連文献 編集
- “The Werner syndrome protein at the crossroads of DNA repair and apoptosis”. Mech Ageing Dev 125 (8): 521–8. (2004). doi:10.1016/j.mad.2004.06.004. PMID 15336909.
- “Pathways and functions of the Werner syndrome protein”. Mech Ageing Dev 126 (1): 79–86. (2005). doi:10.1016/j.mad.2004.09.011. PMID 15610765.
- Monnat RJ Jr; Saintigny Y (2004). “Werner syndrome protein--unwinding function to explain disease”. Sci Aging Knowledge Environ 2004 (13): re3. doi:10.1126/sageke.2004.13.re3. PMID 15056797.
- “Current advances in unraveling the function of the Werner syndrome protein”. Mutat Res 577 (1–2): 237–51. (2005). doi:10.1016/j.mrfmmm.2005.03.020. PMID 15946710.
- “The Werner syndrome protein has separable recombination and survival functions”. DNA Repair (Amst) 3 (5): 475–82. (2004). doi:10.1016/j.dnarep.2004.01.002. PMID 15084309.
- “WRN mutations in Werner syndrome”. Hum. Mutat. 13 (4): 271–9. (1999). doi:10.1002/(SICI)1098-1004(1999)13:4<271::AID-HUMU2>3.0.CO;2-Q. PMID 10220139.
- “The many substrates and functions of ATM”. Nat. Rev. Mol. Cell Biol. 1 (3): 179–86. (2001). doi:10.1038/35043058. PMID 11252893.
外部リンク 編集
- Werner Syndrome. University of Washington, Seattle. (February 2012). PMID 20301687. NBK1514 In GeneReviews [Internet]. Seattle WA: University of Washington, Seattle. (1993)
- GeneCard
- Werner Syndrome Mutational Database