マンノース
マンノース (英: mannose) は、アルドヘキソースに分類される単糖の一種である。
| D-(+)-Mannose | |
|---|---|

| |
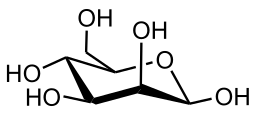
| |

| |
| 識別情報 | |
| CAS登録番号 | 3458-28-4 |
| PubChem | 18950 |
| J-GLOBAL ID | 200907049858861780 |
| KEGG | C00159 |
| MeSH | Mannose |
| 特性 | |
| 化学式 | C6H12O6 |
| モル質量 | 180.16 g mol−1 |
| 外観 | 無色固体 |
| 融点 |
132–133 °C |
| 比旋光度 [α]D | +29.3(α体、水中) −17.0(β体、c 4) +14.2(平衡混合物、水中)[1] |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
化学的性質 編集
化学式は C6H12O6、分子量は 180.16 g/mol。CAS登録番号は D-(+)-マンノースが [3458–28–4]、L-(−)-マンノースは [10030-80-5] である。融点は 132~133℃。単体としてD体が果実や果皮などに含まれるほか、多糖マンナンを構成しており,その加水分解によって大量に得られる。L体は天然には存在しない。マンノースのアルドン酸としてマンノン酸、ウロン酸としてマンヌロン酸、アルダル酸としてマンナル酸、アルジトールとしてマンニトールがある。また、ロブリー・ド・ブリュイン=ファン・エッケンシュタイン転位の平衡反応が起こり、マンノース、グルコース、フルクトースの混合物が得られる。
マンノースはグルコースの2位エピマーであるが、グルコースとは大きく性質が異なっている。
溶液中では6員環のマンノピラノースとして存在している。
| D-マンノース | ||
|---|---|---|
| 構造式 | ハース投影式 | |
| α-D-Mannofuranose <1 % |
β-D-Mannofuranose <1 % | |
| α-D-Mannopyranose 67 % |
β-D-Mannopyranose 33 % | |
代謝 編集
マンノースはヘキソキナーゼによってマンノース-6-リン酸に変えられ、次いでマンノース-6-リン酸イソメラーゼによって解糖系の中間体であるフルクトース-6-リン酸に変えられる。
マンノースは人間ではあまり代謝されない[2][3]。したがって、経口摂取した場合にはほとんど解糖系には入っていかない。
マンノースは糖タンパク質の糖鎖の重要な構成成分であるが、以前は糖鎖中のマンノースはグルコースから変換されると考えられていた。しかしながら近年、ラットにおいて経口摂取させたマンノースの87%が、腸で吸収された後、速やかに血中濃度が低下し(半減期30分)、ほぼ全ての器官で糖鎖合成に使われていることが明らかとなっている[4]。生体内で利用されるマンノースは微量で、90%は30-60分で尿中に排出され、残りの内99%は8時間以内に排出される。その間、血糖値に顕著な影響はない。
マンノースは多くのN-結合型糖鎖に存在する。C-マンノシル化もコラーゲン様部位によく見られる。
酵母で発現させた組み換え(リコンビナント)タンパク質は、ヒトにおけるものとは異なるマンノース修飾パターンを受けている[5]。このリコンビナントタンパク質と正常に生体内で作られるタンパク質との違いはワクチンの有効性に影響を与える可能性がある。
生成 編集
マンノースはマンニトールの酸化によって得られる。また、ロブリー・ド・ブリュイン=ファン・エッケンシュタイン転位によってグルコースから得られる。
D-マンノースは尿路感染症のための自然治療薬として販売されており、尿路においてバクテリアの接着を阻害することによって効果を発揮すると主張されている。
語源 編集
マンノースの名称は旧約聖書の出エジプト記に出てくるマナという食べ物に由来している。マナは、いくつかの木や灌木(例えばFraxinus ornus)の甘味分泌物である。
脚注 編集
- ^ Merck Index 14th ed., 5747.
- ^ Wood, F. C., Jr.; Cahill, G. F. Jr. (1963). “Mannose utilization in man”. J. Clin. Invest. 42: 1300-1312. doi:10.1172/JCI104814. PMC 289400. PMID 14057858.
- ^ Alton, G.; Kjaergaard, S.; Etchison, J. R.; Skovby, F.; Freeze, H. H. (1997). “Oral ingestion of mannose elevates blood mannose levels: a first step toward a potential therapy for carbohydrate-deficient glycoprotein syndrome type I”. Biochem. Mol. Med. 60 (2): 127-133. doi:10.1006/bmme.1997.2574. PMID 9169093.
- ^ Alton, G.; Hasilik, M.; Niehues, R.; Panneerselvam, K.; Etchison, J. R.; Fana, F.; Freeze, H. H. (1998). “Direct utilization of mannose for mammalian glycoprotein biosynthesis”. Glycobiology 8 (3): 285-295. PMID 9451038.
- ^ Vlahopoulos, S.; Gritzapis, A. D.; Perez, S. A.; Cacoullos, N.; Papamichail, M.; Baxevanis, C. N. (2009). “Mannose addition by yeast Pichia Pastoris on recombinant HER-2 protein inhibits recognition by the monoclonal antibody herceptin”. Vaccine 27 (34): 4704-4748. doi:10.1016/j.vaccine.2009.05.063. PMID 19520203.