メベンダゾール
メベンダゾール(Mebendazole、MBZ)は、#ベンズイミダゾール系駆虫薬の1つであり、スペクトラムが広い、すなわち体内に寄生した多種の寄生虫を殺すために用いることのできる医薬品である[2]。例えば、回虫症、蟯虫感染症、鉤虫感染症、メジナ虫症、エキノコックス症、ジアルジア症などの治療に使用できる[2]。しかし、日本では鞭虫症のみの治療薬として承認されている[3]。メベンダゾールは1971年から実用され始め[4]、WHO必須医薬品モデル・リストにも収載されている[5]。
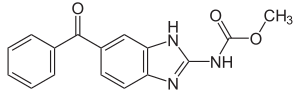 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Vermox[1] |
| Drugs.com | monograph |
| MedlinePlus | a682315 |
| 胎児危険度分類 | |
| 法的規制 | |
| 投与経路 | Oral |
| 薬物動態データ | |
| 生物学的利用能 | 2-10% |
| 血漿タンパク結合 | 95% |
| 代謝 | Hepatic (extensive) |
| 半減期 | 3-6 hours |
| 排泄 | Faeces, urine (5-10%) |
| 識別 | |
| CAS番号 |
31431-39-7 |
| ATCコード | P02CA01 (WHO) QP52AC09 (WHO) |
| PubChem | CID: 4030 |
| DrugBank |
DB00643 |
| ChemSpider |
3890 |
| UNII |
81G6I5V05I |
| KEGG |
D00368 |
| ChEBI |
CHEBI:6704 |
| ChEMBL |
CHEMBL685 |
| 化学的データ | |
| 化学式 | C16H13N3O3 |
| 分子量 | 295.293 g/mol |
| |
| 物理的データ | |
| 融点 | 288.5 °C (551.3 °F) |
ベンズイミダゾール系駆虫薬 編集
メベンダゾールは構造中にベンズイミダゾール骨格を持った、ベンズイミダゾール系の駆虫薬の1つである。ベンズイミダゾール系駆虫薬としては、他にアルベンダゾールやチアベンダゾールが知られる。一般にベンズイミダゾール系駆虫薬は、線虫の幼虫および成虫に有効であり、回虫と鞭虫の場合には、卵に対しても殺虫効果を持つ[6]。
作用機序 編集
メベンダゾールは寄生虫の微小管の合成を阻害し、虫の腸内の既存の細胞質微小管を破壊し、グルコースなどの栄養吸収を妨げ、緩やかに虫体を不動化し、死に至らしめる[6]。
効能・効果 編集
日本で正式に承認されている効能・効果は「鞭虫症」のみである[3]。
しかし実際のところ、メベンダゾールは、さまざまな寄生虫に有効な駆虫薬であり[2]、回虫、鉤虫、鞭虫、線虫、蟯虫などの感染症や、小腸内に留まる旋毛虫症の治療に使用される。寄生虫とその死骸は、数日掛けて便中に排出される[6]。ただし、メベンダゾールは消化管から吸収され難いので、消化管外に寄生した寄生虫には別の薬剤が用いられる[6]。 メベンダゾールは軽度から中等度の寄生虫感染症に単剤で使用される。殺虫効果が見られるまでの時間が比較的長く、重症例では寄生虫が消化管外に出て虫垂炎、胆管障害、腸穿孔などに繋がる危険がある。それらの危険を除くために、重症例の患者にはピペラジンを用いた方が望ましい。ピペラジンは寄生虫を麻痺させ、糞中に排出させる[7]。
メベンダゾールは、まれに包虫症の治療にも使用されるが、有効性は充分に証明されていない[8]。
副作用 編集
寄生虫はヒトと同じ真核生物であり、したがって寄生虫に危害を加える薬が、ヒトに害を与えないことは難しい。そのような中で、メベンダゾールの忍容性は比較的高いとされるものの[2]、さまざまな副作用の発生が知られている。
メベンダゾールの重大な副作用としては、ショック・アナフィラキシー様症状、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)が知られている[3]。また、高用量を投与すると、骨髄抑制が起こり[2]、危険な白血球減少および血小板減少、無顆粒球症が起こることがある。さらに、肝臓の細胞死を誘発し、血中における肝臓からの逸脱酵素の濃度上昇を起こすこともある。
この他にも、しばしば見られる副作用として、頭痛、嘔吐、耳鳴が知られている[2]。まれに、脱毛を引き起こす[9][10]。
妊産婦・授乳婦 編集
メベンダゾールは動物で催奇形性が報告されており、妊婦への安全性は確立していない[2]。アメリカ合衆国でのメベンダゾールの胎児危険度分類はCであり、動物実験では妊娠に異常を来たすことが判明しているものの、ヒトでは臨床試験が実施されていない。ヒトの母乳中に、投与したメベンダゾールが分泌されるか否かは不明である[9]。
薬物相互作用 編集
カルバマゼピンやフェニトインはメベンダゾールの血中濃度を低下させる。メベンダゾールは血中にほとんど吸収されないので、シメチジンは明瞭にはメベンダゾールの血中濃度を上昇させない[11][12]。これは類薬のアルベンダゾールとは対照的である。
高用量のメトロニダゾールの併用でスティーブンス・ジョンソン症候群や中毒性表皮壊死融解症が発生しうる[13]。
研究開発 編集
メベンダゾールには微小管の合成を阻害する作用が知られている[6]。いくつかの研究で、メベンダゾールが抗腫瘍活性を有することが示されている。メベンダゾールは有意に腫瘍細胞の成長や転移を阻害し、副腎皮質癌に対してin vitro とin vivo の両方で効果を示した[14]。メベンダゾールを肺癌系の細胞株を用いた実験では、有糸分裂を停止させ、カスパーゼ活性化とシトクロムc放出によってアポトーシスを誘導した[15]。 なお、ヒト肺癌細胞株に対しては、用量・時間依存的にアポトーシスを誘導した[16]。またメベンダゾールは、化学療法抵抗性の悪性黒色腫細胞に対して、Bcl-2を賦活化させてアポトーシスさせた[17]。
出典 編集
- ^ Ebadi, Manuchair (2008). Desk reference of clinical pharmacology (2 ed.). Boca Raton: CRC Press. p. 403. ISBN 9781420047448
- ^ a b c d e f g “Mebendazole”. The American Society of Health-System Pharmacists. 2015年8月18日閲覧。
- ^ a b c “メベンダゾール錠100 添付文書” (2011年3月). 2016年4月21日閲覧。
- ^ Mehlhorn, Heinz (2001). Encyclopedic reference of parasitology. 107 tables (2 ed.). Berlin [u.a.]: Springer. p. 259. ISBN 9783540668299
- ^ “WHO Model List of EssentialMedicines”. World Health. 2016年4月21日閲覧。
- ^ a b c d e Petri WA (2011). Goodman and Gilman's The Pharmacological Basis of Therapeutics, 12th ed.. McGraw-Hill. p. Chapter 42.. ISBN 978-0071624428
- ^ Martin AR; Doerge RF (1982). Wilson and Gisvold's Textbook of Organic Medicinal and Pharmaceutical Chemistry. Lippincott Williams & Wilkins. p. Chapter 4. ISBN 978-0397515837
- ^ “Mebendazole”. drugs.com. 2015年1月25日閲覧。
- ^ a b Finberg R, Fingeroth J in Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo (2012). Harrison's Principles of Internal Medicine, 18th ed.. McGraw-Hill. p. Chapter 217. ISBN 978-0071748896
- ^ Andersohn F, Konzen C, Garbe E (May 2007). “Systematic review: agranulocytosis induced by nonchemotherapy drugs”. Ann. Intern. Med. 146 (9): 657–65. doi:10.7326/0003-4819-146-9-200705010-00009. PMID 17470834.
- ^ “Drug Interactions”. Medicine chest. 2008年5月6日閲覧。
- ^ Luder PJ, Siffert B, Witassek F, Meister F, Bircher J; Siffert; Witassek; Meister; Bircher (1986). “Treatment of hydatid disease with high oral doses of mebendazole. Long-term follow-up of plasma mebendazole levels and drug interactions”. European journal of clinical pharmacology 31 (4): 443–448. doi:10.1007/bf00613522. PMID 3816925.
- ^ Chen, K. T.; Twu, S. J.; Chang, H. J.; Lin, R. S. (2003). “Outbreak of Stevens-Johnson Syndrome / Toxic Epidermal Necrolysis Associated with Mebendazole and Metronidazole Use Among Filipino Laborers in Taiwan”. American Journal of Public Health 93 (3): 489–492. doi:10.2105/ajph.93.3.489. PMC 1447769. PMID 12604501.
- ^ Martarelli D, Pompei P, Baldi C, Mazzoni G (April 2008). “Mebendazole inhibits growth of human adrenocortical carcinoma cell lines implanted in nude mice”. Cancer Chemother. Pharmacol. 61 (5): 809–17. doi:10.1007/s00280-007-0538-0. PMID 17581752.
- ^ Sasaki J, Ramesh R, Chada S, Gomyo Y, Roth JA, Mukhopadhyay T (November 2002). “The anthelmintic drug mebendazole induces mitotic arrest and apoptosis by depolymerizing tubulin in non-small cell lung cancer cells”. Mol. Cancer Ther. 1 (13): 1201–9. PMID 12479701.
- ^ Mukhopadhyay T, Sasaki J, Ramesh R, Roth JA (September 2002). “Mebendazole elicits a potent antitumor effect on human cancer cell lines both in vitro and in vivo”. Clin. Cancer Res. 8 (9): 2963–9. PMID 12231542.
- ^ Doudican N, Rodriguez A, Osman I, Orlow SJ (August 2008). “Mebendazole induces apoptosis via Bcl-2 inactivation in chemoresistant melanoma cells”. Mol. Cancer Res. 6 (8): 1308–15. doi:10.1158/1541-7786.MCR-07-2159. PMID 18667591.