エンハンサー
遺伝学においてエンハンサー(英: enhancer)は、特定の遺伝子の転写の可能性を高めるためにタンパク質(アクチベーター)が結合する、短い(50–1500塩基対)DNA領域である[1][2]。多くの場合、これらのエンハンサーに結合するタンパク質は転写因子と呼ばれる。エンハンサーはシスに作用し、遺伝子から最大で100万塩基対も離れている場合もあり、転写開始部位の上流に位置する場合も下流に位置する場合もある[2][3]。エンハンサーは原核生物と真核生物の双方に存在し[4]、ヒトのゲノム中には数十万個のエンハンサーが存在する[2]。

真核生物のエンハンサーが最初に発見されたのは1983年、免疫グロブリン重鎖の遺伝子においてである[5][6][7]。巨大なイントロンの内部に位置するこのエンハンサーによって、遺伝子再構成が起こっていないVhプロモーターは不活性であるのに対し、再構成が起こったVhプロモーターからの転写が活性化されることの説明が可能となった。
位置 編集
真核生物の細胞では、DNAのクロマチン構造は原核生物のDNAの超らせん構造を機能的に模倣するような形で折りたたまれる。そのため、エンハンサーDNAは配列上では遺伝子から遠くに位置していても、空間的にはプロモーターや遺伝子に近接していることがあり、基本転写因子やRNAポリメラーゼIIとの相互作用が可能となる[8]。同様の機構はサイレンサーにも当てはまる。サイレンサーはエンハンサーのアンタゴニストであり、リプレッサーと呼ばれる転写因子が結合した際に遺伝子の転写を抑制する。サイレンサーとエンハンサーは互いに近接して位置している場合や、同じ領域に位置し、その領域に結合する転写因子によってのみ両者が区別される場合もある。
エンハンサーは調節標的の遺伝子の上流に位置している場合も下流に位置している場合もある。さらに、エンハンサーは影響を与える転写開始部位に近接して位置している必要はなく、開始部位から数十万塩基対上流または下流に位置しているものもある[9]。エンハンサーはプロモーター領域に直接作用するのではなく、エンハンサー領域にはアクチベータータンパク質が結合する。これらのアクチベーターはメディエーター複合体と相互作用し、メディエーターはRNAポリメラーゼIIと基本転写因子をリクルートし、遺伝子の転写が開始される。エンハンサーは無関係な遺伝子のエクソン領域に存在することもあり[10][11][12]、他の染色体の遺伝子に作用することもある[13]。
ChIP-seqなどの技術を利用して、p300/CBPコアクチベーターファミリーなど特定の因子が結合するエンハンサーの位置の予測が行われている[14][15][16][17]。
哺乳類の転写におけるエンハンサー、転写因子、メディエーター複合体とDNAループの形成 編集
哺乳類における遺伝子発現は、遺伝子の転写開始部位の近傍に位置するコアプロモーターやpromoter-proximal element(プロモーター近位エレメント)など、多くのシスエレメントによって調節される。コアプロモーターは転写開始の指示に十分であるが、一般的にその基礎活性は低い[18]。他の重要なシス調節モジュールは転写開始部位から離れたDNA領域に位置している。そのようなものとしては、サイレンサー、インスレーター、テザリングエレメント(tethering element)などがある[19]。こうしたエレメントの中でも、エンハンサーとそこに結合する転写因子は遺伝子発現の調節に主要な役割を果たしている[20]。エンハンサーは遺伝子のプロモーターから離れたDNA領域に位置しているが遺伝子発現には大きな影響を与え、一部の遺伝子では活発なエンハンサーの存在によって発現が最大100倍にまで上昇する[21]。
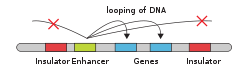
エンハンサーは、ゲノム中の主要な遺伝子調節エレメントである。エンハンサーは細胞種特異的な遺伝子発現プログラムを制御するが、その制御はDNAの長距離のループを形成することで特定のエンハンサーを標的遺伝子のプロモーターに物理的に近接させることによって行われることが多い[22]。エンハンサーのDNA領域とプロモーターの距離はは数十万塩基対にも及ぶが[2]、特定の組織では特定のエンハンサーのみが、そのエンハンサーが制御するプロモーターと近接している。大脳皮質の神経細胞での研究では、エンハンサーを標的プロモーターに近接させる24,937個のループが発見された[21]。複数のエンハンサーは、それぞれ標的遺伝子から数万から数十万ヌクレオチド離れた位置にあることが多いが、標的遺伝子のプロモーターへのループを形成し、互いに協調的に共通の標的遺伝子の発現を制御することができる[22]。
ループはコネクタータンパク質の二量体(CTCFやYY1の二量体など)によって安定化されており、二量体の一方はエンハンサー上の結合モチーフに、もう一方はプロモーター上の結合モチーフに固定されている[23]。細胞機能特異的ないくつかの転写因子(ヒトの細胞内には約1,600種類の転写因子が存在する[24])は一般的にはエンハンサー上の特定のモチーフに結合し[25]、こうしたエンハンサー結合転写因子の小さな組み合わせがDNAのループによってプロモーター近傍にもたらされることによって、標的遺伝子の転写レベルは制御される。メディエーター(通常約26個のタンパク質が相互作用する構造で構成される複合体)は、エンハンサーに結合した転写因子からの調節シグナルを、プロモーターに結合したRNAポリメラーゼIIに直接伝達する[26]。
エンハンサーが活性化している場合、一般的にはDNAの双方の鎖からRNAポリメラーゼによる双方向への転写が行われ、2種類のエンハンサーRNA(eRNA)が産生される[27]。不活性なエンハンサーには、不活性な転写因子が結合している場合がある。転写因子のリン酸化は転写因子を活性化する場合があり、それによって転写因子が結合しているエンハンサーが活性化されることがある[28]。活性化されたエンハンサーは、標的遺伝子のmRNAの転写を活性化する前に自身のeRNAの転写を開始する[29]。
仮説 編集
発生生物学において 編集
細胞や組織の発生、分化と成長には、正確に調節された遺伝子発現パターンが必要となる。エンハンサーはシス調節エレメントとして、特定の細胞で転写を活性化したり抑制したりすることで、発生過程の時間的・空間的制御を行う。発生中の組織では、転写因子や他のDNA結合タンパク質の組み合わせによって、その組織でどの遺伝子が発現するかの制御が行われる。エンハンサーによって、時間的・空間的に異なる過程で同じ遺伝子を利用することが可能となる[31]。
同定と特徴づけ 編集
伝統的に、エンハンサーはレポーター遺伝子を用いたエンハンサートラップによって同定されてきた。キイロショウジョウバエDrosophila melanogasterなどの遺伝的追跡が可能なモデルでは、P因子トランスポゾンを用いてlacZ遺伝子などのレポーターコンストラクトをゲノムにランダムに組み込むことができる。レポーターがエンハンサーの近傍に組み込まれた場合には、レポーターの発現はエンハンサーが駆動する発現パターンを反映したものとなる。そのため、LacZの発現と活性によるハエの染色と、組み込み部位の周囲の配列のクローニングにより、エンハンサー配列を同定することができる[32]。
ゲノミクスとエピゲノミクス技術の発展により、シス調節モジュール(CRM)の発見の様相は劇的に変化している。次世代シーケンシング(NGS)技術によって機能的CRMの発見のためのハイスループットなアッセイが可能となったことで、転写因子結合部位モチーフの大規模ライブラリや、アノテーションと検証が行われたCRMのコレクション、多くの細胞種での広範囲にわたるエピジェネティックなデータなど、利用可能なデータは大幅に増加し、計算によるCRMの正確な発見は達成可能な目標となっている。NGSベースのアプローチの例としてはDNase-Seqと呼ばれるものがあり、CRMが含まれる可能性のある、ヌクレオソームを含まない領域や開いたクロマチン構造の領域の同定が可能である。ATAC-seqなどのより近年の技術では、より少ない出発物質での解析が可能である。ヌクレオソームを含まない領域はDamメチラーゼを発現させることでin vivoで同定することができ、細胞種特異的エンハンサーの同定をより良く制御できるようになった[33]。計算的手法には、比較ゲノミクス、既知または予測された転写因子結合部位のクラスタリング、既知のCRMで学習した教師付き機械学習アプローチなどがある。これらの手法はいずれもCRMの発見に有効であることが証明されているが、それぞれに考慮すべき点や限界があり、またそれぞれ多かれ少なかれ偽陽性の同定が生じる[34]。比較ゲノミクスの手法では、非コード領域の配列保存性がエンハンサーの指標となる。複数の生物種の配列がアラインメントされ、計算によって保存領域が同定される[35]。その後、同定された配列はGFPやlacZなどのレポーター遺伝子に付加され、胚に注入することでエンハンサーによるin vivoでの遺伝子発現パターンが決定される。レポーターのmRNAの発現はin situハイブリダイゼーションによって可視化することができ、翻訳やタンパク質のフォールディングなどの複雑な過程の影響を受けることなく、より直接的にエンハンサー活性を測定することが可能となる。発生に重要なエンハンサーの配列は保存されていることを示す十分な証拠があるものの、他の研究では、一次配列の保存性がほとんどない場合でもエンハンサーの機能が保存されている場合があることが示されている。例えば、ヒトのRETエンハンサーはゼブラフィッシュのものと比較して配列はほとんど保存されていないが、両者の配列をそれぞれ付加したレポーター遺伝子をゼブラフィッシュに導入した場合に駆動される発現パターンはほぼ同じである[35]。同様に、高度に多様化した昆虫(約3億5000万年前に分岐したと考えられる)では、いくつかの重要な遺伝子の類似した遺伝子発現パターンは、類似した構成のCRMによって制御されているものの、これらのCRMにはBLASTなどの標準的な配列アラインメント法で検出できるほどの配列保存性はみられなかった[36]。
昆虫の分節 編集
キイロショウジョウバエの胚の初期の分節を決定するエンハンサーは、発生に関するエンハンサーの中で最もよく特徴づけられている。ハエの初期胚ではギャップ遺伝子転写因子が、ペアルール遺伝子など多数の分節遺伝子の活性化や抑制を担う。ギャップ遺伝子は、母性効果を担う他の転写因子とともに、ハエの前後軸に沿ってブロック状に発現し、その結果、転写因子がさまざまな組み合わせで発現しているさまざまな領域が形成される。ペアルール遺伝子を発現する細胞は非発現細胞によって互いに隔てられ、ストライプ状に位置する。異なるペアルール遺伝子が形成する発現ストライプはそれぞれずれているため、ペアルール遺伝子の発現のユニークな組み合わせによって前後軸に沿った空間的ドメインが形成され、14個のセグメントが設定される。ペアルール遺伝子even-skipped(eve)のストライプ2での鋭い発現を駆動する480 bpのエンハンサーはよく特徴づけられている。このエンハンサーには、母性効果転写因子やギャップ遺伝子転写因子が結合する12個の異なる結合部位が同定されている。活性部位や抑制部位は配列上で重複している。eveは、このエンハンサー配列のアクチベーターが高濃度で存在しリプレッサーが低濃度で存在する、狭いストライプ状の領域でのみ発現する。胚の他の6つのストライプでのeveの発現は、他のエンハンサー領域によって駆動される[37]。
脊椎動物のパターン形成 編集
動物の発生において、体軸の決定は重要な段階である。マウスの胚発生において、TGF-βスーパーファミリーに属するリガンドであるNodalは、初期胚の前後軸と左右軸の双方のパターン形成に関与する重要な因子である。Nodal遺伝子には、PEE(Proximal Epiblast Enhancer)とASE(Asymmetric Enhancer)という2つのエンハンサーが含まれる。PEEはNodal遺伝子の上流に位置し、原始線条の結節へ分化する部分(原始結節とも呼ばれる)でのNodalの発現を駆動する[38]。PEEはWntシグナルと未知のシグナルとの組み合わせに応答してNodalの発現を駆動する。LEF/TCF転写因子ファミリーが結節内の細胞のTCF結合部位に結合すると考えられる。Nodalの結節からの拡散によって濃度勾配が形成され、胚の前後軸のパターンが確立される[39]。ASEはイントロンに位置するエンハンサーで、フォークヘッドドメイン転写因子Fox1が結合する。発生初期には、Fox1によって駆動されるNodalの発現は臓側内胚葉(visceral endoderm)を確立する。より後の段階では、ASEへのFox1の結合は側板中胚葉の左側でのNodalの発現を駆動し、中胚葉での非対称な器官の発生に必要な左右非対称性を確立する[40]。
原腸形成の際の3つの胚葉の確立は、動物の発生に重要な他の段階である。三胚葉にはそれぞれ、分化と発生を促進する特有の遺伝子発現パターンが存在する。初期発生において、内胚葉はGata4の発現によって特定され、Gata4は後に腸の形態形成を指揮する。初期胚において、Gata4の発現は他のフォークヘッド転写因子、FoxA2が結合するイントロン性エンハンサーによって制御されている。まずエンハンサーは胚全体で幅広く遺伝子発現を駆動するが、発現はすぐに内胚葉に限定されるようになる。そのため、他のリプレッサーが抑制に関与している可能性が示唆される。より後の段階では、同じエンハンサーによって胃と膵臓になる組織に発現が限定される。腸の発生の中間段階での内胚葉でのGata4の発現の維持は、さらに他のエンハンサーが担っている[41]。
複数のエンハンサーによる発生の頑健性の促進 編集
重要な発生過程に関与する遺伝子の一部には、重複する機能を持つ複数のエンハンサーが存在する。"Secondary enhancer"や"shadow enhancer"と呼ばれるエンハンサーは、"primary enhancer"から数千塩基対も離れた場所に位置している場合がある。この場合、"primary"という語は最初に発見されたエンハンサーを指し、それらは調節する遺伝子に近接して存在していることが多い。どちらのエンハンサーはほぼ同一なパターンの遺伝子発現を駆動するが、近年の研究では、ショウジョウバエがこうした複数のエンハンサーによって温度上昇などの環境変化を生存していることが示されている。高温で生育した場合、単一のエンハンサーでは発現の完全なパターンの駆動に失敗することがあるが、双方のエンハンサーが存在する場合には正常な遺伝子発現が行われることが示されている[42]。
発生機構の進化 編集
トゲウオPitx1遺伝子 編集
近年、イトヨの形態変化におけるエンハンサーの役割の研究が行われている。トゲウオ類は海水と淡水の双方の環境に存在するが、トゲウオの多くの淡水個体群は、腹鰭(四肢動物の後肢と相同な付属器官)を完全に失っている。
Pitx1は、脊椎動物で後肢の発生に関与するホメオボックス遺伝子である。予備的な遺伝的解析により、この遺伝子の発現の変化がトゲウオでの腹鰭の喪失を担っていることが示されている。Pitx1の淡水型アレルのみを発現する魚は腹鰭を持たず、海水型アレルを発現する魚は腹鰭を持つ。より詳細な特徴づけにより、約500塩基対のエンハンサー配列が腹鰭芽でのPitx1の発現の活性化を担っていることが示された。このエンハンサーは、染色体脆弱部位(DNAが壊れやすく、不正確なDNA修復のために変異が生じやすい領域)の近傍に位置している。淡水個体群では腹鰭の棘でPitx1の発現を駆動するエンハンサーの欠損が何度にもわたって独立に生じており、このエンハンサーを持たない淡水魚では腹鰭の棘の発生が行われない[43]。
ショウジョウバエの翅パターンの進化 編集
色素沈着のパターンは、異なる動物種の間で最も顕著で容易に評価できる差異の1つである。ショウジョウバエの翅の色素沈着は、色素沈着の複雑な表現型の発生の研究に特に適したシステムであることが示されている。ミズタマショウジョウバエDrosophila guttiferaの翅には、12個の暗いvein-associated spot(翅脈と結合した色素斑)と4個のより明るい灰色のintervein shade(翅脈間のパッチ)が存在する。このspotは黒いメラニンを産生する遺伝子産物をコードするyellow遺伝子の発現によって形成される。近年の研究では、yellow遺伝子の2つのエンハンサーが正確にこのパターンの遺伝子発現を引き起こすことが明らかにされた。すなわち、vein spotエンハンサーは12個のspotでレポーター遺伝子の発現を駆動し、もう1つのintervein shadeエンハンサーは4か所のshadeで発現を駆動した。色素沈着が生じたすべての場所でwinglessが発現しており、winglessによってこれら2つのエンハンサーは活性化されていた。複雑な色素沈着の表現型の進化において、yellow色素遺伝子はWinglessシグナルに反応するエンハンサーを進化させ、winglessは新たな場所での発現を進化させることで、新たな翅のパターンが生み出されていた[44]。
炎症とがん 編集
一般的に各細胞には、数百の特殊なクラスのエンハンサーが数kbのDNA配列にわたって並んでいるスーパーエンハンサーと呼ばれる領域が存在する[45]。こうしたエンハンサーには、配列特異的に遺伝子発現を誘導する転写因子の結合部位が多数含まれており、細胞分化に関与する遺伝子発現を調節している[46]。炎症時には、転写因子NF-κBはクロマチンの再編成を促進し、高占有率のエンハンサーからコファクターを選択的に再分配することで、細胞のアイデンティティの維持に関わる遺伝子の発現を抑制する。同時に、NF-κBによって駆動される再編成と再分配は、炎症による細胞機能の変化を誘導する他のエンハンサーを活性化する[47][48]。その結果、炎症は細胞を再プログラムし、組織の他の部分や免疫系との相互作用を変化させる[49][50]。がんではNF-κB活性を制御するタンパク質の調節異常が生じ、悪性細胞は局所組織との相互作用への依存度を低下させ、免疫系による監視を妨げることが可能となっている[51][52]。
脚注 編集
- ^ “Going the distance: a current view of enhancer action”. Science 281 (5373): 60–3. (July 1998). doi:10.1126/science.281.5373.60. PMID 9679020.
- ^ a b c d “Enhancers: five essential questions”. Nature Reviews. Genetics 14 (4): 288–95. (April 2013). doi:10.1038/nrg3458. PMC 4445073. PMID 23503198.
- ^ “Transcriptional regulatory elements in the human genome”. Annual Review of Genomics and Human Genetics 7: 29–59. (2006). doi:10.1146/annurev.genom.7.080505.115623. PMID 16719718.
- ^ “Distant activation of transcription: mechanisms of enhancer action”. Molecular and Cellular Biology 32 (24): 4892–7. (December 2012). doi:10.1128/MCB.01127-12. PMC 3510544. PMID 23045397.
- ^ “Transcriptional enhancer elements in the mouse immunoglobulin heavy chain locus”. Science 221 (4611): 663–5. (August 1983). doi:10.1126/science.6306772. PMID 6306772.
- ^ “A lymphocyte-specific cellular enhancer is located downstream of the joining region in immunoglobulin heavy chain genes”. Cell 33 (3): 729–40. (July 1983). doi:10.1016/0092-8674(83)90015-6. PMID 6409418.
- ^ “A tissue-specific transcription enhancer element is located in the major intron of a rearranged immunoglobulin heavy chain gene”. Cell 33 (3): 717–28. (July 1983). doi:10.1016/0092-8674(83)90014-4. PMID 6409417.
- ^ “Transcriptional regulatory elements in the human genome”. Annual Review of Genomics and Human Genetics 7 (1): 29–59. (2006-01-01). doi:10.1146/annurev.genom.7.080505.115623. PMID 16719718.
- ^ “Obesity-associated variants within FTO form long-range functional connections with IRX3”. Nature 507 (7492): 371–5. (March 2014). doi:10.1038/nature13138. PMC 4113484. PMID 24646999.
- ^ “Exonic remnants of whole-genome duplication reveal cis-regulatory function of coding exons”. Nucleic Acids Research 38 (4): 1071–85. (March 2010). doi:10.1093/nar/gkp1124. PMC 2831330. PMID 19969543.
- ^ “Coding exons function as tissue-specific enhancers of nearby genes”. Genome Research 22 (6): 1059–68. (June 2012). doi:10.1101/gr.133546.111. PMC 3371700. PMID 22442009.
- ^ “De novo genesis of enhancers in vertebrates”. PLOS Biology 9 (11): e1001188. (November 2011). doi:10.1371/journal.pbio.1001188. PMC 3206014. PMID 22069375.
- ^ “Interchromosomal associations between alternatively expressed loci”. Nature 435 (7042): 637–45. (June 2005). doi:10.1038/nature03574. PMID 15880101.
- ^ “Genome-wide mapping of HATs and HDACs reveals distinct functions in active and inactive genes”. Cell 138 (5): 1019–31. (September 2009). doi:10.1016/j.cell.2009.06.049. PMC 2750862. PMID 19698979.
- ^ “Histone modifications at human enhancers reflect global cell-type-specific gene expression”. Nature 459 (7243): 108–12. (May 2009). doi:10.1038/nature07829. PMC 2910248. PMID 19295514.
- ^ “ChIP-seq accurately predicts tissue-specific activity of enhancers”. Nature 457 (7231): 854–8. (February 2009). doi:10.1038/nature07730. PMC 2745234. PMID 19212405.
- ^ “ChIP-seq accurately predicts tissue-specific activity of enhancers”. Nature 457 (7231): 854–8. (February 2009). doi:10.1038/nature07730. PMC 2745234. PMID 19212405.
- ^ “Eukaryotic core promoters and the functional basis of transcription initiation”. Nat Rev Mol Cell Biol 19 (10): 621–637. (October 2018). doi:10.1038/s41580-018-0028-8. PMC 6205604. PMID 29946135.
- ^ “The Why of YY1: Mechanisms of Transcriptional Regulation by Yin Yang 1”. Front Cell Dev Biol 8: 592164. (2020). doi:10.3389/fcell.2020.592164. PMC 7554316. PMID 33102493.
- ^ “Transcription factors: from enhancer binding to developmental control”. Nat Rev Genet 13 (9): 613–26. (September 2012). doi:10.1038/nrg3207. PMID 22868264.
- ^ a b “Three-dimensional genome restructuring across timescales of activity-induced neuronal gene expression”. Nat Neurosci 23 (6): 707–717. (June 2020). doi:10.1038/s41593-020-0634-6. PMC 7558717. PMID 32451484.
- ^ a b “Long-range enhancer-promoter contacts in gene expression control”. Nat Rev Genet 20 (8): 437–455. (August 2019). doi:10.1038/s41576-019-0128-0. PMID 31086298.
- ^ “YY1 Is a Structural Regulator of Enhancer-Promoter Loops”. Cell 171 (7): 1573–1588.e28. (December 2017). doi:10.1016/j.cell.2017.11.008. PMC 5785279. PMID 29224777.
- ^ “The Human Transcription Factors”. Cell 172 (4): 650–665. (February 2018). doi:10.1016/j.cell.2018.01.029. PMID 29425488.
- ^ “Positional specificity of different transcription factor classes within enhancers”. Proc Natl Acad Sci U S A 115 (30): E7222–E7230. (July 2018). doi:10.1073/pnas.1804663115. PMC 6065035. PMID 29987030.
- ^ “The Mediator complex: a central integrator of transcription”. Nat Rev Mol Cell Biol 16 (3): 155–66. (March 2015). doi:10.1038/nrm3951. PMC 4963239. PMID 25693131.
- ^ “The degree of enhancer or promoter activity is reflected by the levels and directionality of eRNA transcription”. Genes Dev 32 (1): 42–57. (January 2018). doi:10.1101/gad.308619.117. PMC 5828394. PMID 29378788.
- ^ “MAP kinase phosphorylation-dependent activation of Elk-1 leads to activation of the co-activator p300”. EMBO J 22 (2): 281–91. (January 2003). doi:10.1093/emboj/cdg028. PMC 140103. PMID 12514134.
- ^ “Enhancer RNAs predict enhancer-gene regulatory links and are critical for enhancer function in neuronal systems”. Nucleic Acids Res 48 (17): 9550–9570. (September 2020). doi:10.1093/nar/gkaa671. PMC 7515708. PMID 32810208.
- ^ Arnosti, David N.; Kulkarni, Meghana M. (2005-04-01). “Transcriptional enhancers: Intelligent enhanceosomes or flexible billboards?”. Journal of Cellular Biochemistry 94 (5): 890–898. doi:10.1002/jcb.20352. ISSN 0730-2312. PMID 15696541.
- ^ “Regulation of eukaryotic gene expression by the untranslated gene regions and other non-coding elements”. Cellular and Molecular Life Sciences 69 (21): 3613–34. (November 2012). doi:10.1007/s00018-012-0990-9. PMC 3474909. PMID 22538991.
- ^ “Studying Drosophila embryogenesis with P-lacZ enhancer trap lines”. Roux's Archives of Developmental Biology 201 (4): 194–220. (June 1992). doi:10.1007/BF00188752. PMID 28305845.
- ^ “CATaDa reveals global remodelling of chromatin accessibility during stem cell differentiation in vivo”. eLife 7. (February 2018). doi:10.7554/eLife.32341. PMC 5826290. PMID 29481322.
- ^ “Identifying transcriptional cis-regulatory modules in animal genomes”. Wiley Interdisciplinary Reviews: Developmental Biology 4 (2): 59–84. (2014). doi:10.1002/wdev.168. PMC 4339228. PMID 25704908.
- ^ a b “Enhancer identification through comparative genomics”. Seminars in Cell & Developmental Biology 18 (1): 140–52. (February 2007). doi:10.1016/j.semcdb.2006.12.014. PMC 1855162. PMID 17276707.
- ^ Kazemian, Majid; Suryamohan, Kushal; Chen, Jia-Yu; Zhang, Yinan; Samee, Md Abul Hassan; Halfon, Marc S.; Sinha, Saurabh (2014-09). “Evidence for deep regulatory similarities in early developmental programs across highly diverged insects”. Genome Biology and Evolution 6 (9): 2301–2320. doi:10.1093/gbe/evu184. ISSN 1759-6653. PMC 4217690. PMID 25173756.
- ^ “Dissecting the regulatory switches of development: lessons from enhancer evolution in Drosophila”. Development 137 (1): 5–13. (January 2010). doi:10.1242/dev.036160. PMC 2796927. PMID 20023155.
- ^ “Asymmetric and node-specific nodal expression patterns are controlled by two distinct cis-acting regulatory elements”. Genes & Development 13 (12): 1575–88. (June 1999). doi:10.1101/gad.13.12.1575. PMC 316799. PMID 10385626.
- ^ “Nodal cis-regulatory elements reveal epiblast and primitive endoderm heterogeneity in the peri-implantation mouse embryo”. Developmental Biology 349 (2): 350–62. (January 2011). doi:10.1016/j.ydbio.2010.10.036. PMID 21047506.
- ^ “The Foxh1-dependent autoregulatory enhancer controls the level of Nodal signals in the mouse embryo”. Development 129 (14): 3455–68. (July 2002). PMID 12091315.
- ^ “Direct transcriptional regulation of Gata4 during early endoderm specification is controlled by FoxA2 binding to an intronic enhancer”. Developmental Biology 346 (2): 346–55. (October 2010). doi:10.1016/j.ydbio.2010.07.032. PMC 2945415. PMID 20692247.
- ^ “Shadow enhancers foster robustness of Drosophila gastrulation”. Current Biology 20 (17): 1562–7. (September 2010). doi:10.1016/j.cub.2010.07.043. PMC 4257487. PMID 20797865.
- ^ “Adaptive evolution of pelvic reduction in sticklebacks by recurrent deletion of a Pitx1 enhancer”. Science 327 (5963): 302–5. (January 2010). doi:10.1126/science.1182213. PMC 3109066. PMID 20007865.
- ^ “Generation of a novel wing colour pattern by the Wingless morphogen”. Nature 464 (7292): 1143–8. (April 2010). doi:10.1038/nature08896. PMID 20376004.
- ^ “Master transcription factors and mediator establish super-enhancers at key cell identity genes”. Cell 153 (2): 307–19. (April 2013). doi:10.1016/j.cell.2013.03.035. PMC 3653129. PMID 23582322.
- ^ “Chromatin stretch enhancer states drive cell-specific gene regulation and harbor human disease risk variants”. Proceedings of the National Academy of Sciences of the United States of America 110 (44): 17921–6. (October 2013). doi:10.1073/pnas.1317023110. PMC 3816444. PMID 24127591.
- ^ “NF-κB directs dynamic super enhancer formation in inflammation and atherogenesis”. Molecular Cell 56 (2): 219–231. (October 2014). doi:10.1016/j.molcel.2014.08.024. PMC 4224636. PMID 25263595.
- ^ “Acute TNF-induced repression of cell identity genes is mediated by NFκB-directed redistribution of cofactors from super-enhancers”. Genome Research 25 (9): 1281–94. (September 2015). doi:10.1101/gr.188300.114. PMC 4561488. PMID 26113076.
- ^ “Late-phase synthesis of IκBα insulates the TLR4-activated canonical NF-κB pathway from noncanonical NF-κB signaling in macrophages”. Science Signaling 9 (457): ra120. (December 2016). doi:10.1126/scisignal.aaf1129. PMC 5260935. PMID 27923915.
- ^ “Super-enhancers delineate disease-associated regulatory nodes in T cells”. Nature 520 (7548): 558–62. (April 2015). doi:10.1038/nature14154. PMC 4409450. PMID 25686607.
- ^ “Dynamic aberrant NF-κB spurs tumorigenesis: a new model encompassing the microenvironment”. Cytokine & Growth Factor Reviews 26 (4): 389–403. (August 2015). doi:10.1016/j.cytogfr.2015.06.001. PMC 4526340. PMID 26119834.
- ^ “Brd4 maintains constitutively active NF-κB in cancer cells by binding to acetylated RelA”. Oncogene 33 (18): 2395–404. (May 2014). doi:10.1038/onc.2013.179. PMC 3913736. PMID 23686307.
関連項目 編集
外部リンク 編集
- エンハンサー - 脳科学辞典
- Enhancer Elements,Genetic - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)
- TFSEARCH
- JASPAR
- ENCODE threads explorer Enhancer discovery and characterization. Nature