クマリン
クマリン (coumarin) は桜の葉に代表される植物の芳香成分の一種。ラクトンの一種で、芳香族化合物である。バニラに似た芳香があり、苦く、芳香性の刺激的な味がする。桜湯や天然のオオシマザクラの塩蔵葉を用いた桜餅の香りはこれらに含まれるクマリンなどによるものである。
| クマリン | |
|---|---|
 クマリンの構造式
| |
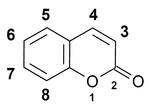 クマリン骨格の番号
| |
2H-クロメン-2-オン(系統名) | |
別称 1-benzopyran-2-one クマリン(慣用名) | |
| 識別情報 | |
| CAS登録番号 | 91-64-5 |
| PubChem | 323 |
| ChemSpider | 13848793 |
| UNII | A4VZ22K1WT |
| J-GLOBAL ID | 200907007165179824 |
| EC番号 | 202-086-7 |
| DrugBank | DB04665 |
| KEGG | C05851 |
| ChEBI | |
| ChEMBL | CHEMBL6466 |
| RTECS番号 | GN4200000 |
| 3DMet | B00867 |
| |
| |
| 特性 | |
| 化学式 | C9H6O2 |
| モル質量 | 146.14 g mol−1 |
| 外観 | 無色または白色結晶 |
| 匂い | pleasant, like vanillabeans |
| 密度 | 0.935 g/cm3 (20 °C (68 °F)) |
| 融点 |
71 °C, 344 K, 160 °F |
| 沸点 |
301.71 °C, 575 K, 575 °F |
| 水への溶解度 | 0.17 g/100 mL |
| 溶解度 | エーテル, ジエチルエーテル, クロロフォルム, 油, ピリジンに易溶 エタノールに可溶 |
| log POW | 1.39 |
| 蒸気圧 | 1.3 hPa (106 °C (223 °F)) |
| 構造 | |
| 結晶構造 | 斜方晶 |
| 危険性 | |
| 安全データシート(外部リンク) | Sigma-Aldrich |
| NFPA 704 | |
| 引火点 | 150 °C (302 °F; 423 K) |
| 半数致死量 LD50 | 293 mg/kg (rat, oral) |
| 関連する物質 | |
| 関連物質 | Chromone |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
クマリンは、シナモンの香り成分のシンナムアルデヒドやコーヒーの香り成分であるコーヒー酸とともに天然の香り成分として知られている。
分離と合成 編集
当初は中南米に育つマメ科のクマル(Dipteryx odorata、トンカともいう。クマリンの語源でもある)という樹木から得られる種子(トンカマメ)から分離されていたが、1876年にウィリアム・パーキンがサリチルアルデヒドと無水酢酸の反応(パーキン反応)[1]により合成に成功[2]。現在では香料、軽油識別剤、医薬品原料として用いられている。
化学的性質 編集
常温では無色の結晶または薄片状の固体。アルコール、エーテル、クロロホルムおよび揮発油に可溶。水に微溶。可燃性。紫外線のブラックライトを照射すると、黄緑色の蛍光を発する。
存在 編集
生きている葉の中ではクマリン酸(o-クマル酸)配糖体の形で糖分子と結びついて液胞内に隔離されているので匂いはしないが、これを含むサクラやヒヨドリバナなどの葉や花を半乾きにしたり破砕、塩蔵するなどすると、死んだ細胞の中で液胞内のクマリン酸配糖体と液胞外の酵素が接触し、加水分解によりクマリン酸が分離、さらに閉環反応が起こってクマリンが生成し、芳香を発するようになる。
食品添加物としては認められていないが、インターネットショッピングや業務用販売などで桜葉や桜葉パウダーが食品素材として流通している。
生合成 編集
- フェニルアラニン → E-桂皮酸
- 桂皮酸 → o-クマル酸, (2-クマル酸, trans-2-hydroxycinnamate)
- 2-クマル酸 → β-D-グルコシル 2-クマル酸, (β-D-Glucosyl 2-coumarate, trans-β-D-glucosyl 2-hydroxycinnamate)
- β-D-グルコシル 2-クマル酸 → β-D-グルコシル 2-クマリン酸, (β-D-glucosyl 2-coumarinate, cis-β-D-glucosyl 2-hydroxycinnamate)
- β-D-グルコシル 2-クマリン酸 → 2-クマリン酸, (coumarinic acidであって、クマリン酸とも表記されるcoumalic acidとは別のものである。)
- 2-クマリン酸 → クマリン (2位の水酸基とカルボキシ基が分子内エステルであるラクトンを形成して環化する)
これらの反応は全て以下の一連の酵素群により触媒されておこる。
- フェニルアラニンアンモニアリアーゼ
- 桂皮酸 2-ヒドロキシラーゼ (EC 1.14.13.14)
- イソメラーゼ (反応)
- β-グルコシダーゼ (β-D-グルコシル 2-クマリン酸グルコハイドラーゼ)(反応)
毒性 編集
通常量では問題ないが過量摂取では肝毒性や腎毒性が懸念されるため、日常継続的に大量摂取することは好ましくない[4][5][6]。
用途 編集
香料 編集
フランスのウビガン (Houbigant) 社が人工合成のクマリンを元に1882年に香水を調合することに成功し、「フジェール・ロワイヤル (Fougere Royale)」と名付けて発売し、人工合成材料による香水の製造が始まる。
タバコにも香料として用いられるが、発がん性が生じる。タバコ会社B&W社の研究開発部門副社長ジェフリー・ワイガンドが自社製品への添加をやめさせようとしたが、代替品が見つからず、本当に科学的根拠があるのかもわからないと豪語する営業畑出身の社長サンダファーはクマリン不使用を検討しなかったことで揉めた。このことを題材に1999年、映画『インサイダー』が作られた。
軽油識別剤 編集
日本においては、クマリンは、軽油引取税の脱税防止のため、1990年(平成2年)3月から識別剤として灯油及びA重油(軽油周辺油種と呼ばれる)に、1 ppmの濃度で添加されている。添加は石油元売業者の製油所から出荷される際に行われ、軽油に灯油などを不正に混合しても、ブラックライトを当てると蛍光反応が出て、識別が可能となる。
イギリスにおいても1984年(昭和59年)から、灯油にクマリンを添加している(イギリスの濃度は2 ppm)。
医薬品原料 編集
誘導体のワルファリン、クマテトラリル、フマリンはビタミンKと拮抗して抗凝血作用を示すため、抗凝固剤や殺鼠剤の製造原料として用いられる[7][8]。
脚注 編集
- ^ 熊野谿従, 桑田勉「パーキン反応に依るクマリンの合成 (第1報)」『有機合成化学協会誌』第11巻第10号、有機合成化学協会、1953年、388-390頁、doi:10.5059/yukigoseikyokaishi.11.388、ISSN 00379980。
- ^ 桜の香り 大阪市立科学館 (PDF)
- ^ 高橋佳孝、大谷一郎、魚住順、萩野耕司、五十嵐良造「クマリンのアレロパシー発現に及ぼす土壌条件の影響」『日本草地学会誌』第40巻第2号、1994年、223–226頁、doi:10.14941/grass.40.223、2022年4月9日閲覧。
- ^ “シナモン”. 国立健康・栄養研究所. 2021年7月18日閲覧。
- ^ “シナモン”. 厚生労働省『「統合医療」に係る 情報発信等推進事業』. 2021年7月17日閲覧。
- ^ “ドイツのBfRがシナモン中のクマリンについて警告(061020)”. 国立健康・栄養研究所. 2022年11月7日閲覧。
- ^ “Coumarin”. PubChem, National Library of Medicine, US National Institutes of Health (2019年4月4日). 2019年4月13日閲覧。
- ^ “Coumarins and indandiones”. Drugs.com (2016年). 2016年12月24日閲覧。
