プレノール
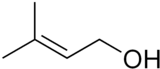
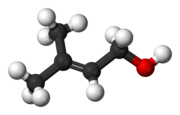
プレノール(Prenol)は、天然に精製するアルコールである。IUPAC名は、3-メチル-2-ブテン-1-オールという。最も単純なテルペンの1つで、無色透明の精油であり、水には適度に溶け、ほとんどの有機溶媒と任意の割合で混ざる。果物のような香りを持ち、香水に使われることもある。
| プレノール | |
|---|---|
| |
| |
3-Methyl-2-buten-1-ol | |
別称 3,3-Dimethylallyl alcohol | |
| 識別情報 | |
| CAS登録番号 | 556-82-1 |
| PubChem | 11173 |
| ChemSpider | 10700 |
| EC番号 | 209-141-4 |
| |
| |
| 特性[1] | |
| 化学式 | C5H10O |
| モル質量 | 86.132 g/mol |
| 密度 | 0.848 g/cm3 |
| 融点 |
−59 °C (calculated) |
| 沸点 |
約142 °C |
| 水への溶解度 | 17 g/100 ml (20 °C) |
| log POW | 0.91 |
| 危険性 | |
| GHSピクトグラム |  
|
| GHSシグナルワード | 警告(WARNING) |
| Hフレーズ | H226, H302 |
| Pフレーズ | P210, P233, P240, P241, P242, P243, P264, P270, P301+312, P303+361+353, P330, P370+378, P403+235, P501 |
| EU Index | not listed |
| 引火点 | 43.3 °C (110 °F) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
天然には、柑橘類、クランベリー、コケモモ、スグリ、ブドウ、ラズベリー、ブラックベリー、トマト、精白パン、ホップ油、コーヒー、キイチゴ、クラウドベリー、パッションフルーツ等に含まれる[1]。また、ドイツのBASFや日本のクラレによって、医薬品や香料の中間体として工業生産されている。2001年の世界全体での生産量は6,000トンから13,000トンであった[1]。
工業生産 編集
プレノールは、工業的にはホルムアルデヒドとイソブテンを反応させ、得られたイソプレノール(3-メチル-3-ブテン-1-オール)を異性化することで生産される[1][2]。
ポリプレノール 編集
プレノールは、次の一般式で表されるイソプレノイドアルコールの構成単位となる。
- H–[CH2CCH3=CHCH2]n–OH
繰り返されるC5H8単位はイソプレンと呼ばれ、このような構造の化合物は「イソプレノール」と呼ばれることもあるが[3]、プレノールの異性体であるイソプレノールとは別のものである。最も単純なイソプレノイドアルコールはゲラニオール(n=2)であり、ファルネソール(n=3)、ゲラニルゲラニオール(n=4)と続く。
アルコールと結合するイソプレン単位が飽和されたものはドリコールと呼ばれる。ドリコールは、多糖合成の際に糖を運搬する。細胞膜の防御、細胞タンパク質の安定化、免疫系の維持にも重要な役割を果たす。
プレノールは、少なくとも5単位以上ある時には、脱水反応によって重合し、重合体はポリプレノールと呼ばれる。ポリプレノールは、100単位程度まで大きくなれる。長鎖のイソプレノイドアルコールは、「テルペノール」とも呼ばれ、タンパク質、カロテノイド、脂溶性のビタミンA、ビタミンE、ビタミンK等のアシル化に重要な役割を果たす。
ポリプレノールは、細胞代謝においても重要である。摂取されたポリプレノールは、肝臓でドリコールに代謝され、ドリコールリン酸回路に入る。ポリプレノールの薬理活性は、慢性炎症性や腫瘍等によってドリコールが欠乏するのを補う効果に由来する[4]。
出典 編集
- ^ a b c d 3-Methyl-2-buten-1-ol, SIDS Initial Assessment Report, Geneva: United Nations Environment Programme, (May 2005).
- ^ See, eg, Kogan, S. B.; Kaliya, M.; Froumin, N. (2006), “Liquid phase isomerization of isoprenol into prenol in hydrogen environment”, Appl. Catal. A: Gen. 297 (2): 231–36, doi:10.1016/j.apcata.2005.09.010.
- ^ See, eg, Goodfellow, Robert D.; Huang, Yung-Sheng; Radtke, Harold E., Jr. (1972), “Isoprenol biosynthesis in the fly, Sarcophaga bullata”, Insect Biochem. 2 (8): 467–75, doi:10.1016/0020-1790(72)90027-3.
- ^ Edlund, C.; Söderberg, M.; Kristensson, K. (1994), “Isoprenoids in aging and neurodegeneration”, Neurochem. Int. 25 (1): 35–38, doi:10.1016/0197-0186(94)90050-7, PMID 7950967.
- ^ Company Announcement – Report on Opening of Tomsk Production Facility, Solagran Ltd., (2008-03-27) 2009年8月31日閲覧。.