モルヒネ
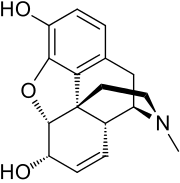
モルヒネ(莫児比涅[1]、蘭: morfine、英: morphine、英語発音: [ˈmɔːrfiːn])は、ベンジルイソキノリン型アルカロイドの一種で、チロシンから生合成されるオピオイド系の化合物である。ケシを原料とする。脳内や脊髄に作用し、痛みを脳に伝える神経の活動を抑制し、鎮痛作用を示す。
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 | |
| 法的規制 | |
| 投与経路 | 吸入, 経口, 皮下注射, 筋肉内注射, 静注 |
| 薬物動態データ | |
| 生物学的利用能 | 〜25% (経口); 100% (静注); |
| 血漿タンパク結合 | 30–40% |
| 代謝 | 肝臓 90% |
| 半減期 | 2–3 時間 |
| 排泄 | 腎臓 90%, 胆汁 10% |
| 識別 | |
| CAS番号 | 57-27-2 |
| ATCコード | N02AA01 (WHO) |
| PubChem | CID: 5288826 |
| DrugBank | APRD00215 |
| ChemSpider | 4450907 |
| KEGG | D08233 |
| 化学的データ | |
| 化学式 | C17H19NO3 |
| 分子量 | 285.4 |
| |
きわめて強力な鎮痛作用を持ち、日本では薬機法に定められた、重要な処方箋医薬品である。とくに持続する疼痛である鈍痛に効果が高く、一般的な鎮痛薬が効きにくい内臓痛をはじめ、各種がん性疼痛や手術後の術後痛にも適応する。有効限界がないのも特徴で、より強い痛みに対しては用量を増やすことによる対応が可能である[2]。
その一方で適切に使わねば強い中毒性・常習性を持つため(医療の鎮痛目的には使用方法が確立されており、適切に使えば依存することはない)、毒薬(薬機法)・麻薬(麻向法)として規制されている。
医療用途
編集医療用途においては、麻薬施用者免許を取得した医師・歯科医師・獣医師の処方で、手術によって起こる痛みを止めるための麻酔や、癌性疼痛、神経障害性疼痛や外傷による強い慢性疼痛、各種の疾病による疼痛に対して、痛みを緩和する目的で使用される。「モルフィン」、「モヒ」とも呼ぶ。薬剤の剤形としては錠剤、散剤、液剤、坐剤、注射剤があり、それぞれ実情に応じて使用される。味は苦い。同種のコデインは麻薬施用者免許のない医師等でも処方でき、咳止めとして普通に処方される。また、咳止めシロップ薬などにも低濃度のコデインが含まれているが指定第二類医薬品のため処方箋なしに薬局で購入、服用できる唯一のオピオイド薬である[3]。風邪を引いた際に飲む咳止めに含まれるので、多数の国民が服用経験があると考えられる。慢性疼痛患者に処方投与する場合、その患者に対してどういった鎮痛薬を用いるのが適切かを確かめるために、医師等は「ドラッグチャレンジテスト」を実施することがある。これは、麻薬であるオピオイドを含む各種の鎮痛薬を、患者には何の医薬品を使用しているかを知らせずに投与して患者自身による痛みの評価尺度であるVASやNRSなどを参考にしながら適切な薬品の種類を決める方法である。この結果モルヒネが効く場合にはじめてモルヒネの処方を開始し、VASやNRSなどに応じて最適な用量を決定していく。
作用機序
編集モルヒネはδ、κ、μのいずれのオピオイド受容体にも親和性を持つが、主に中枢神経系(CNS)と末梢神経系(PNS)内にあるμオピオイド受容体に結合することによって鎮痛効果を発揮する。 モルヒネがオピオイド受容体(またはモルヒネ
モルヒネをはじめとするオピオイド鎮痛薬を使用した場合、具体的な割合は調査によってばらつきがあるものの比較的高い頻度で便秘が見られるが[7]、この背景にはオピオイドが腸管にあるオピオイドμ受容体に作用して腸内の蠕動運動を抑制しているためだと長らく考えられてきた[8][9]。しかし、近年では大腸に内在するタンパク質の一種であるアクアポリン3の発現増加に伴い水分の吸収が促進されることも便秘の一因であると示唆する研究がある[10]。
代謝
編集経口投与されたモルヒネは胃腸管から吸収されると主に肝臓で代謝され、約44-55%がモルヒネ-3-グルクロニド(M3G)に、約9-10%は強力な鎮静・鎮痛作用を持つモルヒネ-6-グルクロニド(M6G)に変換される[7][11]。なお、M6Gは投与経路を問わず鎮痛効果に大きく寄与する[12]一方で、M3Gはオピオイド受容体への親和性が低く鎮痛作用はない[13]がTLR4受容体との相互作用によってオピオイド誘発性痛覚過敏(オピオイド投与による痛みの感受性増加)など副作用の原因となる[14][15]。つまり、モルヒネを使用した際の鎮痛効果や多幸感は、主にモルヒネ・モルヒネの代謝物であるM6G・それらの媒介となるオピオイド受容体、この3つの相互作用によるものである。
副作用
編集モルヒネの副作用には、薬物依存性、耐性のほか、悪心嘔吐、血圧低下、便秘、眠気、呼吸抑制がある[7]。便秘の発現が48–90%[16][17]、悪心嘔吐は40–50%の症例でみられる。[要出典]眠気はモルヒネ投与開始から7日の間で頻繁にみられ、時間経過と共に改善することがほとんどである[7]。
多くの場合、M3GとM6Gは腎臓から排泄される。腎機能障害を有する患者にモルヒネを使用すると、これらが蓄積するために腎機能障害患者へのモルヒネは非推奨であり、とりわけ高度な腎機能障害を有する患者に対しては使用すべきではない[7][18]。また、ブプレノルフィンはμオピオイド受容体に対する親和性がモルヒネよりも強いため、ブプレノルフィンを投与した場合には、モルヒネとブプレノルフィンの間でμオピオイド受容体への結合が競合するので総合的に鎮痛効果が弱まる可能性がある[7]。
毒性
編集毒としてみた場合、非常に強い塩酸モルヒネを例にとると、ヒト(経口)のLD50:120-500mg/kgである。マウス皮下注 (LD50):456mg/kg、マウス静注 (LD50):258 mg/kg。乳児・ 小児では感受性が高い。数量にすると、ヒトに対し6-25gであり、数分から2時間程度で死亡する。
法的分類
編集国際的には、麻薬に関する単一条約の、スケジュールIに指定されている。
歴史
編集1804年、ドイツの薬剤師フリードリヒ・ゼルチュルナーによって初めて分離された(この物質は、史上初めて薬用植物から分離されたアルカロイドとなった)。ゼルチュルナーは、この薬が「夢のように痛みを取り除いてくれる」ということから、ギリシア神話に登場する、ケシの花に囲まれて眠るという夢の神モルペウス (Morpheus) にちなんでモルフィウム (morphium) と名づけ、効用の研究・宣伝に当たった。
1805年には鎮静催眠薬として精神医学にも導入された[19]。
しかし、1853年の皮下注射針の開発までは、モルヒネは普及しなかった。鎮痛のために用いられ、また、アヘンやアルコールの中毒(依存症)の治療として用いられた。南北戦争ではモルヒネは広く使用され、軍人病(モルヒネ依存症)による40万人を超える被害者を生み出した。また普仏戦争において、同様のことが西欧で起こった。
モルヒネの依存症を克服する目的で、モルヒネを原料とするヘロインが1898年に発売された。
脚注
編集- ^ 金沢庄三郎 編「モルヒネ」『広辞林』(新訂)三省堂、1934年、1812頁。
- ^ “モルヒネ”. www.interq.or.jp. 2020年1月8日閲覧。
- ^ “【薬食審】乱用防止へ販売数量制限‐一般薬配合7成分を指定”. 薬事日報. (2014年2月17日) 2021年11月12日閲覧。
- ^ Murphy PB, Bechmann S, Barrett MJ (2022年6月20日). “Morphine” (英語). StatPearls. 2023年3月13日閲覧。
- ^ 船山信次『毒の科学 毒と人間のかかわり』(第4版)ナツメ社、2015年4月10日、105頁。ISBN 4816354093。
- ^ “麻酔薬および麻酔関連薬使用ガイドライン 第 3 版 XI ペイン” (pdf). 公益社団法人日本麻酔科学会. 2023年3月13日閲覧。
- ^ a b c d e f “がん診療ガイドライン│がん疼痛薬物療法│薬理学的知識”. 一般社団法人日本癌治療学会. 2023年3月14日閲覧。
- ^ Kaufman PN, Krevsky B, Malmud LS, Maurer AH, Somers MB, Siegel JA, Fisher RS (1988-06). “Role of opiate receptors in the regulation of colonic transit” (英語). Gastroenterology 94 (6): 1351-1356. doi:10.1016/0016-5085(88)90673-7. PMID 2834257 2023年3月15日閲覧。.
- ^ Brock C, Olesen SS, Olesen AE, Frøkjaer JB, Andresen T, Drewes AM (2012-10-01). “Opioid-induced bowel dysfunction: pathophysiology and management” (英語). Drugs 72 (12): 1847-1865. doi:10.2165/11634970-000000000-00000. PMID 22950533 2023年3月15日閲覧。.
- ^ Risako Kon, Nobutomo Ikarashi, Akio Hayakawa, Yusuke Haga, Aika Fueki, Yoshiki Kusunoki, Masataka Tajima, Wataru Ochiai, Yoshiaki Machida, Kiyoshi Sugiyama (2015-06). “Morphine-Induced Constipation Develops With Increased Aquaporin-3 Expression in the Colon via Increased Serotonin Secretion” (英語). Toxicological Sciences 145 (2): 337-347. doi:10.1093/toxsci/kfv055. PMID 25766885 2023年3月15日閲覧。.
- ^ Christrup LL (1997-01). “Morphine metabolites” (英語). Acta Anaesthesiologica Scandinavica 41 (1): 116-122. doi:10.1111/j.1399-6576.1997.tb04625.x. PMID 9061094 2023年3月13日閲覧。.
- ^ Klimas R, Mikus G (2014-12). “Morphine-6-glucuronide is responsible for the analgesic effect after morphine administration: a quantitative review of morphine, morphine-6-glucuronide, and morphine-3-glucuronide” (英語). British Journal of Anaesthesia 113 (6): 935–944. doi:10.1093/bja/aeu186. PMID 24985077 2023年3月13日閲覧。.
- ^ Smith MT. (2000-07). “Neuroexcitatory effects of morphine and hydromorphone: evidence implicating the 3-glucuronide metabolites” (英語). Clinical and Experimental Pharmacology and Physiology 27 (7): 524-528. doi:10.1046/j.1440-1681.2000.03290.x. PMID 10874511 2023年3月13日閲覧。.
- ^ Due MR, Piekarz AD, Wilson N, Feldman P, Ripsch MS, Chavez S, Yin H, Khanna R, White FA. (2012-08-16). “Neuroexcitatory effects of morphine-3-glucuronide are dependent on Toll-like receptor 4 signaling” (英語). Journal of Neuroinflammation 9 (200). doi:10.1186/1742-2094-9-200. PMID 22898544 2023年3月13日閲覧。.
- ^ Lewis SS, Hutchinson MR, Rezvani N, Loram LC, Zhang Y, Maier SF, Rice KC, Watkins LR. (2010-01-20). “Evidence that intrathecal morphine-3-glucuronide may cause pain enhancement via toll-like receptor 4/MD-2 and interleukin-1beta” (英語). Neuroscience 165 (2): 569-583. doi:10.1016/j.neuroscience.2009.10.011. PMID 19833175 2023年3月16日閲覧。.
- ^ Tokoro A, Imai H, Fumita S, Harada T, Noriyuki T, Gamoh M, Akashi Y, Sato H, Kizawa Y (2019-08). “Incidence of opioid-induced constipation in Japanese patients with cancer pain: A prospective observational cohort study” (英語). Cancer Medicine 8 (10): 4883-4891. doi:10.1002/cam4.2341. PMID 31231974 2023年3月14日閲覧。.
- ^ 林 隼輔、須田奈美、川久保孝、下山直人「オピオイド誘発性の便秘および嘔気・嘔吐に対するオピオイド受容体拮抗薬ナルデメジンの効果」(pdf)『医療薬学』第45巻第12号、2019年12月10日、667-673頁、doi:10.5649/jjphcs.45.667、2023年3月14日閲覧。
- ^ “医療用麻薬適正使用ガイダンス” (pdf). 厚生労働省医薬・生活衛生局・監視指導・麻薬対策課. 2023年3月16日閲覧。
- ^ Francisco López-Muñoz; Ronaldo Ucha-Udabe; Cecilio Alamo (2005). “The history of barbiturates a century after their clinical introduction”. Neuropsychiatr Dis Treat (4): 329–43. PMC 2424120. PMID 18568113.
関連項目
編集- デソモルヒネ
- コノトキシン
- ブロンプトン・カクテル
- 『人間失格』 - 主人公の大庭葉蔵が絶望の果てに酒の替わりに知り中毒に陥る。
- L.A.ノワール - 推理ゲーム。風紀犯罪課の捜査でモルヒネの事件を扱う。
外部リンク
編集- “医療用麻薬(モルヒネなど)をはじめて使用するとき” (PDF). 日本緩和医療学会. 2023年3月17日時点のオリジナルよりアーカイブ。2019年4月10日閲覧。