オピオイド
オピオイド(Opioid)は、ケシから採取されるアルカロイドや、そこから合成された化合物、また、体内に存在する内因性の化合物を指す。鎮痛、陶酔作用があり、また薬剤の高用量の摂取では昏睡、呼吸抑制を引き起こす[2]。医療においては手術や、がんの疼痛の管理のような強い痛みの管理に不可欠となっている。このようなアルカロイド(オピエート)やその半合成化合物には、モルヒネ、ジアセチルモルヒネ、コデイン、オキシコドンなどが含まれ、合成オピオイドにはフェンタニル、メサドン、ペチジンなどがある[2]。これらは本来的な意味で麻薬(narcotic)である[2]。オピオイドとは「オピウム(アヘン)類縁物質」という意味であり、これらが結合するオピオイド受容体に結合する物質(元来、生体内にもある)として命名された。内因性のオピオイドにはエンドルフィン、エンケファリンなどがある。
| オピオイド | |
|---|---|
| Drug class | |
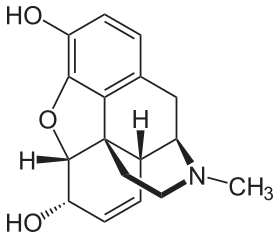 | |
| クラス識別子 | |
| 効用 | 疼痛緩和 |
| ATC code | N02A |
| 作用様式 | オピオイド受容体 |
| External links | |
| MeSH | D000701 |
| In Wikidata | |
オピオイド薬の使用には、オピオイド依存症や、離脱症状、また過剰摂取による死亡の危険性がある。そのため多くの国で規制物質となっている。
半合成のものはアメリカでは一般的に流通しており、弱い順にコデイン、バイコディン(合剤である商品名)、オキシコドンの3種がある[3]。いずれも処方箋があれば簡単に入手できる。
アメリカでは、2015年内には2.4億件のオピオイドが処方されており(米国の全成人に対して1処方に相当する)[4]、薬物中毒死の43%までも、オピオイド医薬品の過剰摂取で占めている[5]。2014年にもアメリカ神経学会は頭痛、腰痛、線維筋痛症などの慢性の疼痛では、オピオイドの使用は危険性の方がはるかに上回るという声明を行っている[6]。死亡は止まらず、2017年にはアメリカで「オピオイド危機」と呼ばれる公衆衛生上の非常事態が宣言された[7]。一方で、用途でも言及されているように末期がんなど重いがん患者には、オピオイドを使用できるようにするべきだという点で、専門家の意見はほぼ一致しているとされる[8]。
OECD25カ国を対象とした調査では、オピオイド関連死亡(ORD)の平均は2011年から2016年にかけて20%以上増加しており、その要素としてOECDは疼痛管理目的の処方、および過剰処方の増加を挙げている[4]。そのためOECDは根拠に基づく臨床ガイドラインや、処方サーベイランス強化などにより、処方規制の改善が必要だと勧告している[4]。オピオイド乱用は医療サービスへの大きな負担である[4]。
定義 編集
オピオイドとは、ケシ(Opium poppy)から採取されるアルカロイドや、それから合成された化合物、また体内に存在する内因性の化合物を指す[2]。
オピオイドは、鎮痛や陶酔といった共通した作用を持つ[2]。ケシから採取されるアルカロイドや、それから合成された化合物は、高用量を摂取した場合に、昏睡、呼吸抑制を引き起こす[2]。
一般的に、「オピオイド」は「麻薬性鎮痛薬」を指す用語であるが、“麻薬=オピオイド”というわけではない[9](後述)。
麻薬 編集
麻薬(narcotic)とは、通常は麻薬性鎮痛薬として、この記事にて説明しているオピオイドや、またはさらにその狭義のオピエートを含めて指す用語である[2]。しかし、そうした薬理学的な定義と関わりなく、一般用語あるいは法律上において、コカインや大麻などを含めた違法薬物を指して用いられている場合がある[2]。そのため、世界保健機関の薬物に関する文書では、麻薬の語ではなく、より具体的な意味を持つオピオイドの語を用いている[2]。
現在では「麻薬」という用語は社会的用語であり、薬理学的あるいは分子生物学的用語である「オピオイド」とは意味が異なる[9]。「麻薬及び向精神薬取締法」で「麻薬」に指定されている薬剤が麻薬であり、オピオイド受容体とは関係しないものもある[9]。例えば、オピオイドではない「ケタミン」は麻薬に指定されているので、「麻薬性非オピオイド鎮痛薬」になる[9]。
合成・半合成オピオイド 編集
ケシのアルカロイド(オピエート)やその半合成化合物には、モルヒネ、ジアセチルモルヒネ(ヘロイン)、コデイン、オキシコドンなどが含まれる。また合成オピオイドにはフェンタニル、メサドン、ペチジンなどがある[2]。
内因性オピオイド 編集
生体内で産生されるのオピオイドはペプチド(オピオイドペプチド)であり、作用するオピオイド受容体サブタイプの違いによってエンドルフィン類(μ受容体)、エンケファリン類(δ受容体)、ダイノルフィン類(κ受容体)の3つに分類される。
非麻薬性オピオイド(鎮痛薬) 編集
合成オピオイドのうち、鎮痛作用を有するものは「非麻薬性オピオイド(鎮痛薬)」と称され、その代表は以下の通り:。
- トラマドール - トラマール、ワントラム、トラムセット配合錠(アセトアミノフェン配合)[10]- 劇薬。医療用麻薬としての規制外[11]。
- ブプレノルフィン - ノルスパン、レペタン - 劇薬、向精神薬、習慣性医薬品
- ペンタゾシン - ソセゴン、ペルタゾン - 劇薬、向精神薬、習慣性医薬品
オピオイドのうち、鎮痛作用を有するものの構造にはN,N-Dialkyl-3,3-dialkyl-3-phenylpropanamineという共通点があり、モルヒネ則と呼ばれている。
用途 編集
手術侵襲に対する鎮痛と過剰なストレス反応の制御、がん末期のような強い痛みに対する鎮痛手段として広く用いられており、医学の進歩した現代においても最も強力な鎮痛薬であるとともに、麻酔臨床では必要不可欠な薬剤である。
手術の麻酔で使用されるオピオイドは、日本ではモルヒネ、フェンタニル、レミフェンタニルである。欧米では、このほかにアルフェンタニルやスフェンタニルも使用されている。
副作用 編集
依存症 編集
オピオイド依存症であるかは、当初の想定よりも使用量が増加し離脱症状を呈する、薬物の使用が制御できない、またそれらによって引き起こされた機能的な状態が重症であるなどの、いくつかの診断基準を満たすかに基づいて診断されうる。
2008年のレビューでは、依存率は全体として3.3%であり、アルコールや薬物依存の既往歴のある場合に5%、そうでない場合に0.2%であった[12]。アメリカでは、2000年以降にジアセチルモルヒネ(ヘロイン)を乱用した者の75%が、処方薬のオピオイドによって乱用を開始している[13]。オピオイド使用障害は、意図しない過剰摂取による死亡だけでなく、自殺と関連しておりアメリカでのオピオイドの使用が深刻化した結果、自殺率も上昇してきた[14]。
依存症の治療は、半減期の長いオピオイドであるメタドンや、より新しいものではオピオイド受容体に作用するブプレノルフィンに置換して漸減するのが標準的である。活性成分イボガインを含む幻覚剤であるイボガを用いた治療は、標準的でない治療法として実施している施設がある。
離脱症状 編集
オピオイドによる離脱症候群には、渇望、不安、不快、あくび、発汗、立毛(鳥肌)、流涙、鼻漏、不眠、吐き気や嘔吐、下痢、痙攣、筋肉痛、また発熱が含まれる[2]。
モルヒネやジアセチルモルヒネ(ヘロイン)などの短時間作用型の薬物では、離脱症状は最後の摂取から8~12時間以内に発症し、48~72時間でピークに達し、7~10日後にかけて消えていく[2]。メサドンなどの長時間作用型の薬剤では、離脱症状の発症は1~3日であることもあり、一般的により軽度の症状が長く続く[2]。
遷延性離脱として、上記のような急性の離脱症状に続き、数週間から数か月にわたってあまり明確ではない症状が生じることがある[2]。
ガイドライン 編集
2014年には、アメリカ神経学会がオピオイドによる死亡の増加から声明を出しており[15]、頭痛、腰痛、線維筋痛症などの慢性疼痛状態では、薬剤使用の利益を危険性の方がはるかに上回るとした[6]。これは最良の方法を挙げており、処方を行う前に処方データ監視プログラム(PDMP)を確認することや、1日にモルヒネに換算して80~120mgに相当する場合には、疼痛管理の専門家に相談することが含まれている[6]。死亡の増加によりアメリカ疾病予防管理センター (CDC) は2016年にガイドラインを公開しており、それは慢性疼痛では運動や認知行動療法のような非薬物療法や他の薬物療法を推奨し、オピオイドは最小有効量で使用して定期的に痛みが改善しているか観察することが必要であるとしている[16]。その後、CDCのガイドラインでオピオイドの使用削減を勧告した執筆者たちは2019年のニューイングランド・ジャーナル・オブ・メディスンで、使用削減の結果が患者に「深刻な危害」をもたらしているようだと警告し、CDCは2016年のガイドラインを見直し、オピオイド使用削減の呼びかけを訂正した[17]。
薬理学 編集
作用機序 編集
オピオイドとオピオイドレセプターの結合によりGタンパク質を介して神経細胞の過分極が生じて神経伝達系が抑制されると考えられている。しかし、その神経回路などについては不明な点が多い。Gタンパク質はそれぞれのレセプターに関与するイオンチャネルに作用すると考えられているが、その詳細は明らかになっていない。
薬物動態 編集
モルヒネ、フェンタニル、レミフェンタニルの薬物動態における特性を示す。
| モルヒネ | フェンタニル | レミフェンタニル | |
|---|---|---|---|
| pKa | 8.0 | 8.4 | 7.1 |
| ph7.4におけるイオン化率 | 77 | >90 | 33? |
| 脂溶性(オクタノール/水分配係数) | 1.4 | 813 | 17.9 |
| 血漿蛋白結合率(%) | 20〜40 | 84 | 80? |
| 定常状態での分布容量(Vdss)(L/kg) | 3〜5 | 3〜5 | 0.2〜0.3 |
| クリアランス(mL/min/Kg) | 15〜30 | 10〜20 | 30〜40 |
フェンタニルは、脂溶性が高いために定常状態における分布容積が大きいことが特徴で、血中濃度の低下には再分布が大きな意味をもつ。レミフェンタニルはエステル構造を有し、血中あるいは組織中のエステラーゼにより速やかに分解される。生体に投与されたモルヒネの約60%は肝臓で、残りは腎臓で代謝される。肝臓で代謝されたモルヒネはモルヒネ3グルクロナイド(M3G)とモルヒネ6グルクロナイド(M6G)になる。 M3Gには鎮痛作用はないが、M6Gの鎮痛作用はモルヒネよりも強いと言われている。腎不全患者ではM6Gの排出が遅れて著しい呼吸抑制をきたす可能性がある。
フェンタニルは肝臓で速やかに代謝されるが、その代謝産物にはほとんど鎮痛作用がない。レミフェンタニルは投与中止とともに速やかに血中濃度が低下するため、術後呼吸抑制の心配が少ない。そのため超短時間作用性オピオイドとして有用であるが、投与中止により速やかに鎮痛効果が消失するので、術後の疼痛対策が必須である[18]。
薬理作用 編集
- 鎮痛作用
- 鎮痛のメカニズムに関しては不明な点が多いが、解明されつつある。オピオイドは、脊髄後角において一次知覚神経線維末端からのサブスタンスPやグルタミン酸のような神経伝達物質の放出を抑制し、脊髄後角に存在する侵害ニューロンの興奮を抑制する。このような作用以外に、オピオイドが中脳水道周囲灰白質に作用することにより下行抑制系(ノルアドレナリン作動性およびセロトニン作動性)が活性化されることによる脊髄後角における鎮痛作用を示す機序もある。さらに、視床、大脳皮質のレベルにおいても鎮痛作用が現れる。 このように、オピオイドの鎮痛作用は中枢神経系内の1ヶ所における作用では説明できない。さらに、末梢神経におけるオピオイドの鎮痛作用も報告されている。 薬剤の種類によって鎮痛作用の力価には差がある。鎮痛作用力価の比の目安をモルヒネ:1とすると、フェンタニル:100、スフェンタニル:500 、アルフェンタニル:1 、レミフェンタニル:500 である。 鎮痛作用は個人差が大きい。また鎮痛効果と呼吸抑制や鎮静作用も必ずしも並行しない。参考値を表にまとめる。+の数がアゴニストの強さ、-の数がアンタゴニストの強さである。
物質名 μ親和性 κ親和性 同効果(mg) 最大効果(min) 持続時間(hr) モルヒネ +++ + 10 20~30 3~4 フェンタニル +++ 0 0.1 3~5 0.5~1.0 レミフェンタニル +++ 0 0.1 1.5~2.0 0.1~0.2 ペチジン ++ + 80 5~7 2~3 ブプレノルフィン +++ - 0.3 30 6~8 ペンタゾシン -- ++ 60 15~30 2~3 ブトルファノール - ++ 2 15~30 2~3 トラマドール ++ - 100 15 4~6 ナロキソン --- - ? ? ?
- 中枢作用
- オピオイドには鎮静作用があり、吸入麻酔薬と併用すると吸入麻酔薬のMACを減少させる効果がある。しかし、単独では大量に投与しても完全な意識消失は起こりにくい。 この作用にはドーパミン系が関与している可能性がある。動眼神経 Edinger–Westphal核に対する大脳皮質からの抑制が解除されて、縮瞳を起こす。 オピオイドは長期使用によって耐性、依存性、習慣性を生じることがある。オピオイドの副作用として掻痒感をきたすことがある。その機序は明らかにされていないが、延髄あるいは脊髄における作用の可能性がある。
- 通常の鎮痛量では傾眠傾向になるものの健忘作用はないとされている。深い鎮痛効果と無呼吸に至るほどの高用量を投与しても必ずしも入眠するとは限らない。オピオイド単独による麻酔導入は不可能と考えられている。
- ヒスタミン遊離作用のないフェンタニルでも掻痒感を生じ、その掻痒感は抗ヒスタミン薬で抑制されず、ナロキソンによって抑制されることからオピオイド自体の脳幹レベルでの作用と考えられている。
- 呼吸器系
- 上気道、下気道における反射を抑制する。鎮咳作用もあり、気管挿管時の反射、咳嗽を抑制することができる。一方、非麻酔時の鎮痛目的使用では、その呼吸抑制作用が問題になることが多い。オピオイドは脳幹の延髄に存在する呼吸中枢に作用して、用量に依存して呼吸抑制を起こし、血中の二酸化炭素濃度の上昇を起こしたり、低酸素による換気促進作用を減弱させる。高齢、腎不全、肝障害などがあると、呼吸抑制が著しく現れることがあるので注意が必要である。呼吸数の減少が典型的であるが、呼吸リズムが不規則になることもある。意識があるときも呼吸する意思が抑制されて窒息をおこす恐れがある。そのためオピオイド投与時は効果が最大になる時間まで呼吸が止まらないことを確認する必要がある(呼吸抑制は濃度依存の作用であるため)。
- モルヒネにはヒスタミン遊離作用があるため気管支喘息の患者には使いにくい。それ以外のオピオイドも咳嗽抑制、呼吸抑制があることから気管支喘息患者への使用には注意が必要である。
- 心血管作用
- オピオイドは、循環抑制作用が少ないので、心疾患を有する患者の麻酔や心臓外科手術の麻酔に対して安全に用いることができる。また、オピオイドを投与することによって、心筋虚血によって生じる梗塞巣の容積を減少させることができるという報告がある。脳幹の迷走神経を刺激することにより除脈を引き起こすことがあるが、アトロピンの投与によって拮抗することができる。
- また、モルヒネは肥満細胞からのヒスタミン遊離をひきおこし、ヒスタミンの血管拡張作用による低血圧を生じる。これを予防するためには、H1受容体拮抗薬(ジフェンヒドラミン、クロルフェニラミンなど)とH2 受容体拮抗薬(シメチジン、ラニチジンなど)の両者を投与する必要がある。
- 消化器系
- 中枢、および消化管自体のオピオイド受容体に作用し、下部食道括約筋を弛緩させ、消化管蠕動運動を抑制する。そのため、モルヒネの長期投与では便秘が起こることが多い。
- オッディ括約筋の収縮をおこし、胆道内圧の上昇を引き起こすため、胆道系疾患の疼痛には使いにくい。
- 延髄のCTZに作用し悪心、嘔吐を起こす。
- 泌尿器系
- 尿管、膀胱の排尿筋や尿道括約筋を収縮させ、尿意促迫や尿閉をおこす。前立腺肥大症の患者では注意が必要である。
- 内分泌系
- 筋硬直
- オピオイドの投与により、骨格筋の強直を起こすことがある。呼吸筋の強直を生じると、換気不全を起こして補助呼吸を要する場合がある。声門の閉鎖からマスク換気が不可能になることもある。骨格筋の強直を生じるメカニズムは不明であるが、オピオイドによって誘発される大脳基底核のGABA系やドパミン系の変化が関与するとの報告がある。オピオイドは神経筋接合部には作用しないので、筋弛緩薬を投与するとオピオイドによる骨格筋の強直は生じない。麻酔中に筋が硬くなるのは、麻酔が浅い場合もあるしオピオイドの副作用であることもある。
- 抗ストレス作用
- 生体に手術侵襲のような強力なストレスが加わると、交感神経系の活性化による高血圧、頻脈とともに下垂体前葉から副腎皮質刺激ホルモン(ACTH)、成長ホルモン(GH)、下垂体後葉からバゾプレッシン、副腎皮質からコルチゾールが分泌され、血糖の上昇を生じる。このような生体の神経、内分泌系を介するストレス反応が過剰に起こると、周術期合併症の誘因となる可能性がある。現在全身麻酔に用いられている吸入麻酔薬や静脈麻酔薬は、意識消失作用は強いが、鎮痛作用および抗ストレス作用は不十分である。モルヒネやフェンタニルは手術侵襲によって引き起こされる内分泌反応を抑制する。
薬物相互作用 編集
オピオイドにベンゾジアゼピン系の薬物が加わることで、呼吸抑制作用が増強され、意図しない死亡事故が生じやすい[19]。
薬力学的相互作用 編集
アメリカの処方記録によれば、2000年代に、オキシコドンや、アセトアミノフェンとヒドロコドンの合剤であるVicodinのようなオピオイドと、アルプラゾラムやロラゼパム、またクロナゼパムのようなベンゾジアゼピン系の薬剤の処方はそれぞれ増加した[19]。2010年には、検視官から提出された死亡診断書など死因ファイルの調査によって、22,134例の医薬品による死亡のうち16,651例(75%)がオピオイドが関与したものであり、そのほぼ30%はベンゾジアゼピンが組み合わさったものであった[5]。このような相互作用による中毒死は、1999年には13%であり、2011年には31%であった[20]。
フェノチアジン誘導体、バルビツール酸誘導体、ベンゾジアゼピン系薬剤のような中枢神経抑制薬のほか、アルコール、ワルファリンのような抗凝固薬など、抑制作用を増強させる薬剤の併用によって抑制作用が増強される可能性がある[21]。
薬物動態学的相互作用 編集
オキシコドンでは、CYP2D6を阻害する薬剤によって血中濃度が高まる可能性がある[21]。フェンタニルはCYP3A4を阻害する[21]。
オピオイド受容体 編集
オピオイド受容体はμ(ミュー)、κ(カッパ)、δ(デルタ)、σ(シグマ)、ε(イプシロン)の5つが知られている。σはナロキソンによって拮抗されないため、特異的オピオイド受容体とは考えられなくなりつつある。εは内因性オピオイドであるβエンドルフィンと結合性が高い以外あまりわかっていない。2007年現在、μ、κ、δの3つが特異的オピオイド受容体と考えられ、特にμとκが臨床医学では重要視されている。薬理学的にはμには2つ、κには3つのサブタイプが知られている。静脈麻酔ではμ1が鎮痛、μ2が呼吸抑制を担っていると考えられてμ1の特異的アゴニストが開発できれば非常に扱いやすい鎮痛薬になると考えられている。
- μ1受容体
- 主に脊髄より上位中枢に作用し鎮痛作用に関わるとされている。鎮静作用やプロラクチン放出作用も知られている。μ受容体の遺伝子としての実体はOprm1、もしくはMOR1と呼ばれる単一のものであるが、選択的スプライシングによって多数のバリアントが生じることが知られている。
- μ2受容体
- 主に脊髄に作用し、鎮痛作用に関わるとされている。μ2受容体のその他の作用としては呼吸抑制、徐脈、血圧低下、多幸感、悪心、腸蠕動抑制、オッディ括約筋収縮、排尿障害、筋硬直、縮瞳などがあげられる。
- κ受容体
- 主に脊髄に作用して鎮痛作用に関わるとされている。その他の作用としては鎮静や不快感、幻覚やせん妄、ADH分泌低下が知られている。内因性オピオイドのダイノルフィン類と親和性が高いことが知られている。κ受容体の遺伝子としての実体はOprk1、もしくはKORと呼ばれるものである。
- δ受容体
- 主に脊髄に作用して鎮痛作用に関わるとされている。その他の作用としては掻痒感がある。内因性オピオイドのエンケファリン類と親和性が高いことが知られている。δ受容体の遺伝子としての実体はOprd1、もしくはDORと呼ばれるものである
- σ受容体
- オピオイドレセプターであるが鎮痛作用はなく他のオピオイドレセプターと異なる作用をもつ。呼吸促進、頻脈、血圧上昇、散瞳といった作用が知られている。
医療大麻との併用 編集
医療大麻は、低用量でオピオイドの鎮痛効果を増強する[22][23][24][25]。1999年から2010年の、アメリカの全50州の死亡証明書の分析により、州ごとの医療大麻の合法化に伴って、その州のオピオイド系鎮痛薬の過剰摂取による死亡者数は低下している[26]。共に鎮痛作用は主な作用である[26]。
様々な調査があり、医療大麻にアクセスできたことで67%がオピオイドをやめることができ、29%は使用量を減らしたとか、別の調査では30%がすべての薬をやめることができた[27]。
オピオイド乱用 編集
オピオイド乱用率は、欧州においては一般市民の間で1%未満であった[4]。しかし刑務所人口においては平均30%に上昇していた[4]。
またオピオイド乱用者においては、アルコールやその他の薬物の多剤乱用が一般的である[4]。これは他の薬物との相互作用において、よりオピオイド関連死を招くことを意味する[4]。
過剰摂取による死亡 編集
オピオイドは、作用量と有毒域が近いため薬事法における劇薬に指定されている。
アメリカでは、医薬品のオピオイドによる死亡は、他の医薬品や違法薬物を抜いて最多であり、2010年の死因ファイルによる38,329例の中毒死のうち16,651(43%)を占めている[5]。オピオイド系鎮痛薬による中毒死は、アメリカでは1999年から2011年とを比較するとおよそ4倍に増加した[20]。1999年から、2010年では、男性2.65倍に増加したのに対して、女性4倍となっている[29]。
処方薬による死亡の4倍の増加は、将来のジアセチルモルヒネ(ヘロイン)による死亡につながるのではと懸念されたが、2009年まで増加は見られなかった[30]。しかし、2010年と2011年に薬物過剰摂取死の最多であったオキシコドンを、2012年に急増したジアセチルモルヒネ(ヘロイン)が上回った[31]。
2016年8月、アメリカ食品医薬品局(FDA)は、極度の眠気、呼吸抑制、昏睡および死亡につながることがあるオピオイドとベンゾジアゼピンの併用について、それら医薬品に、最も強い枠内警告を追加した[32]。
2019年12月8日、ラッパーのジュース・ワールドがオピオイドの過剰摂取により死亡した。
オピオイド危機 編集
| ジアセチルモルヒネ(ヘロイン) | オピオイド | 10,863 | 23.1% |
| コカイン | 精神刺激薬 | 5,856 | 12.4% |
| オキシコドン | オピオイド | 5,417 | 11.5% |
| アルプラゾラム | ベンゾジアゼピン | 4,217 | 9.0% |
| フェンタニル | オピオイド | 4,200 | 8.9% |
| モルヒネ | オピオイド | 4,022 | 8.5% |
| メタンフェタミン | 精神刺激薬 | 3,728 | 7.9% |
| メサドン | オピオイド | 3,495 | 7.4% |
| ヒドロコドン | オピオイド | 3,274 | 7.0% |
| ジアゼパム | ベンゾジアゼピン | 1,729 | 3.7% |
2017年にトランプ大統領は、オピオイド危機について国家非常事態の宣言を予定し[33]、これは公衆衛生上の非常事態の宣言となった[7]。中国をオピオイドおよびオピオイド関連の違法物質の主な供給源と主張し[34]、2023年には「主要な麻薬供給国」に認定した[35]。
これはアメリカでのみ強く起こった事態である[36]。1990年代半ばにオキシコドン(オキシコンチン)は、38人での研究だけに基づいて依存が発生しない、革新的な薬として広く販売されるようになったが、実際の日常ではまだ痛みが完全に消えていない人々はより多く用い、また薬物への欲求を増大させるものであった[36]。しかし、製薬産業は医師への豪華な接待や、病院の待合室で再生されるビデオを通じて積極的にマーケティングし、医師もしばしば時間のかかる痛みの原因の特定よりも痛みを感じさせなくする方が簡単であった[36]。1999年から2011年ではオキシコドンの処方量は6倍となり、次第に世界の81%をアメリカ合衆国で消費するようになった[36]。依存者は勿論薬物の売人達もニーズの変化に従ってクリニックからクリニックへと痛みを訴えては処方箋を入手しようと試み、安易に処方を行う医師達はろくな診察もせず彼らに処方箋を書く。更に医師には処方箋のために受け取る賄賂や医薬品を転売することでも大きな収入をもたらし、この危機は犯罪や暴力の大きな動乱を起こさないため、目立たず静かに進行していった[36]。
こうして薬の販売が増えて利益を上げる製薬産業、手間いらずで患者を満足させ患者数の増加と処方箋を書くための賄賂や転売で儲ける医師、合法な処方箋による麻薬の入手が可能となった依存者と売人の需要が噛み合ったサイクルが完成し瞬く間にオピオイドはアメリカ中に蔓延した。監視を逃れるため越境してメキシコで薬を入手したり、ついには現金ではなく麻薬目当てに薬局に強盗が押し入る事態も起きた。
医師は問題に気づき、処方箋監視プログラムの導入もあって2010年からの5年間で処方量は18%減少し、依存者はストリートのジアセチルモルヒネ(ヘロイン)に向かうことになるが、そこへ登場したのはジアセチルモルヒネ(ヘロイン)よりも50倍強い効力を持つ、中国から密輸されるフェンタニルであった[36]。上述の通り、オピオイドは作用量と致死量が近く、量を間違えると死亡しうる。
こうした死亡を減らす取り組みには職業訓練を行う一方で、監督下注射施設を用意することであり、カナダでは35%の死亡の減少、全国的に展開するスイスでは半減している(ハーム・リダクション)[36]。これを実施するためにはアメリカは薬物戦争を終わらせなければならず、そのための準備はまだない[36]。
過剰摂取の対策として鎮痛効果を維持しつつ依存性が少ないオピオイド化合物の研究が行われている[37]。
裁判 編集
オピオイドの乱用問題が拡大すると、アメリカ国内では数千件もの裁判が提起された。2019年にはアメリカの製薬会社パーデュー・ファーマが、2022年にはアイルランドの製薬会社エンドー・インターナショナルが、訴訟に対処するため破産法の適用を申請している[38]。
リガンド 編集
アゴニスト 編集
パーシャルアゴニスト 編集
- オピオイドレセプターのパーシャルアゴニスト(部分作動薬)を弱オピオイドという。弱オピオイドは鎮痛効果に天井効果があることが知られている。天井効果とは投与量を増やしても鎮痛効果はある一定以上増えることはない。分子的メカニズムは不明ではあるが副作用のみが増えることが知られている。パーシャルアゴニストとしてはペンタゾシン(ペンタジン、ソセゴン)、ブプレノルフィン(レペタン)、トラマドール(トラマール)などが有名である。またκ選択的アゴニストにナルフラフィン(レミッチ)、ナルブフィン(セダペイン)がある。
アゴニストアンタゴニスト 編集
- μ受容体にはアゴニストとしてκ受容体にはアンタゴニストとして作用する、あるいはその逆に作用する物質である。ペンタゾシン、ブトルファノール(スタドール)はμ受容体には作用を示さず、κ受容体に対して作用を示す。すなわちμアゴニスト存在下ではμアンタゴニスト、κアゴニストと考えることができる。しかし近年はアゴニストアンタゴニストという概念を作ること自体に疑問の声もあがっている。なお、ペンタゾシンやブトルファノールはμ作用がないことから呼吸抑制や便秘といった作用も少ないと考えられている。こういった理由からソセゴンは病棟で鎮痛薬としてよく用いられる。
アンタゴニスト 編集
麻薬拮抗薬 編集
オピオイド受容体のアンタゴニストであるナロキソンが麻薬拮抗薬として臨床的に使用されている。
ナロキソンによるオピオイドの副作用の治療 編集
オピオイドの副作用(呼吸抑制、悪心・嘔吐・掻痒感、尿閉、骨格筋の強直など)は、ナロキソンの投与によって軽減することができる。静脈注射後、1~2分で作用が現れ、30~60分持続する。作用時間が短いため、モルヒネのように作用時間の長いものに対して使用する時は、ナロキソンの効果が消失したあとに再びオピオイドの副作用が現れる(renarconization)ことがあり、注意が必要である。ナロキソンの副作用として、血圧上昇、頻脈、肺水腫がある。
脚注 編集
- ^ Ogura, Takahiro; Egan, Talmage D. (2013). “Chapter 15 – Opioid Agonists and Antagonists”. Pharmacology and physiology for anesthesia : foundations and clinical application. Philadelphia, PA: Elsevier/Saunders. ISBN 978-1-4377-1679-5
- ^ a b c d e f g h i j k l m n 世界保健機関 (1994) (pdf). Lexicon of alchol and drug term. World Health Organization. pp. 47, 49-50. ISBN 92-4-154468-6 (HTML版 introductionが省略されている)
- ^ 「オキシコドン」は、"警戒"するべき薬だった
- ^ a b c d e f g h Addressing Problematic Opioid Use in OECD Countries, OECD, (2019), doi:10.1787/a18286f0-en, ISBN 9789264934207
- ^ a b c Jones, Christopher M.; Mack, Karin A.; Paulozzi, Leonard J. (February 2013). “Pharmaceutical Overdose Deaths, United States, 2010”. JAMA 309 (7): 657. doi:10.1001/jama.2013.272. PMID 23423407.
- ^ a b c Kristina Fiore (2014年9月30日). “AAN Warns Against Opioids in Chronic Noncancer Pain”. MedPage Today 2015年5月15日閲覧。
- ^ a b Axel Bugge (2017年10月28日). “アングル:米国の「オピオイド危機」、欧州にも波及の恐れ”. ロイター 2017年12月5日閲覧。
- ^ “アメリカが苦戦する新オピオイド危機”. ニューズウィーク日本版(2023年6月27日号). CCCメディアハウス. (2023-6-27). p. 44.
- ^ a b c d オピオイド 日本ペインクリニック学会
- ^ トラムセット配合錠基本情報 日経メディカル
- ^ トラマドール:トラマール,ワントラム おくする110番
- ^ DA Fishbain, B Cole, J Lewis, HL Rosomoff, RS Rosomoff. (2008年). “What percentage of chronic nonmalignant pain patients exposed to chronic opioid analgesic therapy develop abuse/addiction and/or aberrant drug-related behaviors? A structured evidence-based review”. PUbMed Health. 2016年8月15日閲覧。
- ^ Rudd RA, Paulozzi LJ, Bauer MJ, et al. (2014). “Increases in heroin overdose deaths - 28 States, 2010 to 2012”. MMWR. Morbidity and Mortality Weekly Report 63 (39): 849–54. PMID 25275328.
- ^ Bohnert ASB, Ilgen MA (January 2019). “Understanding Links among Opioid Use, Overdose, and Suicide”. N. Engl. J. Med. (1): 71–79. doi:10.1056/NEJMra1802148. PMID 30601750.
- ^ Katz, J. A.; Swerdloff, M. A.; Brass, S. D.; Argoff, C. E.; Markman, J.; Backonja, M.; Katz, N.; Franklin, G. M. (2015). “Opioids for chronic noncancer pain: A position paper of the American Academy of Neurology”. Neurology 84 (14): 1503–1505. doi:10.1212/WNL.0000000000001485. ISSN 0028-3878.
- ^ “Guideline Information for Providers”. アメリカ疾病予防管理センター:CDC (2016年7月14日). 2016年8月15日閲覧。
- ^ “アメリカが苦戦する新オピオイド危機”. ニューズウィーク日本版(2023年6月27日号). CCCメディアハウス. (2023-6-27). p. 45.
- ^ 古家仁 (2011/05/01). 標準麻酔科学第6版. 医学書院
- ^ a b John Fauber, Kristina Fiore (2014年2月25日). “Killing Pain: Benzo 'Boost' Can Be Deadly”. MedPage Today 2014年3月11日閲覧。
- ^ a b Rebecca Cooney (2014年10月1日). “Graying the dragon”. The Lancet United States of Health Blog 2015年5月15日閲覧。
- ^ a b c (編集)日本緩和医療学会、緩和医療ガイドライン作成委員会「2章背景知識 4-1-10 オピオイドの与える影響/薬物相互作用」『がん疼痛の薬物療法に関するガイドライン』(第1版;2010年)金原出版、2010年6月20日。ISBN 978-4-307-10149-3。
- ^ “麻薬系鎮痛剤治療にカンナビスを併用することにより疼痛緩和改善の可能性/カリフォルニア大学サンフランシスコ校”. がん医療情報リファレンス (2012年1月12日). 2016年8月15日閲覧。
- ^ “Adding Cannabis to Opiates Treatment May Increase Pain Relief”. University of California San Francisco Medical Center (2012年12月6日). 2016年8月15日閲覧。
- ^ Abrams, D I; Couey, P; Shade, S B; Kelly, M E; Benowitz, N L (2011). “Cannabinoid–Opioid Interaction in Chronic Pain” (pdf). Clinical Pharmacology & Therapeutics 90 (6): 844–851. doi:10.1038/clpt.2011.188. PMID 22048225.
- ^ Megan Brooks (2011年12月13日). “Cannabis Augments Analgesic Effect of Opioids”. Medscape 2016年8月15日閲覧。
- ^ a b Bachhuber, Marcus A.; Saloner, Brendan; Cunningham, Chinazo O.; Barry, Colleen L. (2014-08). “Medical Cannabis Laws and Opioid Analgesic Overdose Mortality in the United States, 1999-2010”. JAMA Internal Medicine. doi:10.1001/jamainternmed.2014.4005. PMID 25154332.
- ^ Russ Belville (2017年11月3日). “Study: 2 out of 3 Pain Patients Quit Opioids with Marijuana”. HuffPost 2018年2月25日閲覧。
- ^ Robert S., Gable. “Acute Toxicity of Drugs Versus Regulatory Status”. In Jeffeson M. Fish. Drugs and society : U.S. public policy. Rowman & Littlefield. pp. 149-162. ISBN 0-7425-4245-9
- ^ “[www.cdc.gov Prescription Painkiller Overdoses - A Growing Epidemic, Especially Among Women]”. CDC (2013年7月). 2016年8月15日閲覧。
- ^ Martins, Silvia S.; Sampson, Laura; Cerdá, Magdalena; et al. (2015). “Worldwide Prevalence and Trends in Unintentional Drug Overdose: A Systematic Review of the Literature”. American Journal of Public Health 105 (11): e29–e49. doi:10.2105/AJPH.2015.302843. PMC 4605170. PMID 26451760.
- ^ a b Warner M, Trinidad JP, Bastian BA, Minino AM, Hedegaard H (2016). “Drugs Most Frequently Involved in Drug Overdose Deaths: United States, 2010-2014” (pdf). Natl Vital Stat Rep (10): 1–15. PMID 27996932.
- ^ "FDA requires strong warnings for opioid analgesics, prescription opioid cough products, and benzodiazepine labeling related to serious risks and death from combined use" (Press release). アメリカ食品医薬品局(FDA). 31 August 2016. 2017年5月10日閲覧。
- ^ “トランプ米大統領、鎮痛剤の乱用「国家的な不名誉」”. BBC. (2017年10月27日) 2017年12月5日閲覧。
- ^ “米国、オピオイド需要減らすためさらなる措置が可能=中国外務省”. ロイター (2019年8月26日). 2023年9月18日閲覧。
- ^ “外交部「米国は中国の麻薬撲滅努力にとやかく言う資格はない」”. CRJ (2023年9月18日). 2023年9月18日閲覧。
- ^ a b c d e f g h Andrew Sullivan (2018年2月20日). “The Poison We Pick”. New York. 2018年2月18日閲覧。
- ^ 新しいオピオイド鎮痛薬の開発 - 和歌山県立医科大学医学部薬理学講座
- ^ “医薬品エンドーが米破産法の適用申請、オピオイド訴訟に対応”. ロイター (2022年8月17日). 2022年8月17日閲覧。
参考文献 編集
- 病態生理に基づく臨床薬理学 ISBN 4895924610
- 麻酔科必修マニュアル 羊土社 ISBN 4897063442
- STEP 麻酔科 海馬書房 ISBN 4907704275
- イヤーノート内科外科等編 2007年版 メディックメディア ISBN 9784896321500
- 麻酔科シークレット メディカルサイエンスインターナショナル ISBN 9784895923224
- 麻酔科レジデントマニュアル ISBN 4906472443
- 麻酔科研修チェックノート 改訂第2版 ISBN 9784758105682
- 麻酔科研修の素朴な疑問に答えます ISBN 4895924440
- 麻酔の研修ハンドブック 小栗顕二編著 金芳堂 1999 ISBN 4765309762
- 「DOPESICK アメリカを蝕むオピオイド危機」ベス・メイシー光文社 2020年 ISBN 9784334962388
関連項目 編集
外部リンク 編集
- 『がん疼痛の薬物療法に関するガイドライン 2010年版』日本緩和医療学会、緩和医療ガイドライン作成委員会・編集