グルタミン酸
グルタミン酸(グルタミンさん、英: glutamic acid, glutamate)は、アミノ酸のひとつで、2-アミノペンタン二酸のこと。2-アミノグルタル酸とも呼ばれる。Glu あるいは E の略号で表される。小麦グルテンの加水分解物から初めて発見されたことからこの名がついた。英語に準じ、グルタメートと呼ぶこともある。
| グルタミン酸 | |
|---|---|
| |

| |

| |
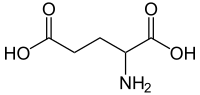
Glutamic acid | |
別称 2-Aminopentanedioic acid 2-Aminoglutaric acid | |
| 識別情報 | |
| CAS登録番号 | 617-65-2 56-86-0 (L-異性体) 6893-26-1 (D-異性体) |
| PubChem | 611 |
| ChemSpider | 591 |
| UNII | 61LJO5I15S |
| 日化辞番号 | J9.171E |
| EC番号 | 210-522-2 |
| E番号 | E620 (調味料) |
| KEGG | C00302 C00025 (L-グルタミン酸) C00217 (D-グルタミン酸) |
| ChEMBL | CHEMBL276389 |
| 1369 | |
| |
| |
| 特性 | |
| 化学式 | C5H9NO4 |
| モル質量 | 147.13 g mol−1 |
| 外観 | 白色結晶性粉末 |
| 密度 | 1.4601 (20 °C) |
| 融点 |
199 °C(分解) |
| 水への溶解度 | soluble |
| 危険性 | |
| GHSピクトグラム | 
|
| Hフレーズ | H301, H315, H335 |
| EU Index | |
| NFPA 704 | |
| 関連する物質 | |
| 関連物質 | α-ケトグルタル酸 アンモニア グルタミン グルタミン酸ナトリウム |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
酸性極性側鎖アミノ酸に分類される。タンパク質構成アミノ酸のひとつで、非必須アミノ酸。動物の体内では神経伝達物質としても機能しており、グルタミン酸受容体を介して神経伝達が行われる、興奮性の神経伝達物質である。
グルタミン酸が多くつながると、納豆の粘性物質であるポリグルタミン酸になる。
致死量はLD50=20グラム/キログラムであり、体重50キログラムのヒトなら1,000グラム=1キログラムである。
生合成 編集
クエン酸回路の一員である2-オキソグルタル酸が、グルタミン酸トランスフェラーゼの作用により他のアミノ酸からアミノ基転移を受けることで合成される。
あるいは、グルタミン酸デヒドロゲナーゼ (EC 1.4.1.3) による、グルタミン酸の2-オキソグルタル酸とアンモニアへの分解反応の逆反応により合成される。
- L-glutamate + H2O + NAD(P)+ → 2-oxoglutarate + NH3 + NAD(P)H + H+
存在 編集
コンブ、チーズ、緑茶などに大量に含まれるほか、シイタケ、トマト、魚介類などにも比較的多く含まれていることが知られている。
利用 編集
主に、食品添加物であるL-グルタミン酸ナトリウム(グルタミン酸ソーダ、mono sodium glutamate、MSGあるいはグル曹とも呼ばれる)の中間原料として製造、利用される。グルタミン酸そのものは酸味を持つため、そのナトリウム塩であるグルタミン酸ナトリウムが調味料(うま味調味料)として利用されている。L-グルタミン酸ナトリウムを主成分とする調味料として、日本では味の素などがよく知られている。
昆布等からのグルタミン酸の抽出には水に含まれるミネラルが悪影響を及ぼすので軟水の使用が望ましい[1][信頼性要検証][2][信頼性要検証][3]という話がよくある。多数の硬度の違う水を用いた研究によると、昆布からのグルタミン酸ナトリウムの抽出量における硬度の影響は否定されている[4]。同研究では、カルシウムの影響で粘性が上がるので、グルタミン酸の量が関係なくとも昆布だしを取るにはカルシウムが多い水は向かないとしている[4]。
製法 編集
現在ではグルタミン酸は工業的に生産されている。2005年には世界で約 170 万トン、年率で3 - 4 %の増産が見込まれていた[5]。用途によっていくつかの製法が併存するが、アミノ酸発酵によるものが最も生産量が多い。
加水分解法 編集
グルテン、大豆蛋白などの植物性タンパク質に、塩酸を加えて高温のもとで加水分解すると、グルタミン酸の塩酸塩が得られる。かつては小麦粉グルテンを使っての製造が行われていたが、現在は用いられない。
抽出法 編集
テンサイから甜菜糖を作る過程で出る廃糖蜜には、約3%程度の遊離グルタミン酸が含まれるので、ステファン法によって抽出すれば利用可能であり、1930年代には工業化されたが、コストが高いことと、廃棄物が多く出ることから、現在は用いられない。
化学合成法 編集
アクリロニトリルを原料に、ホルミル化、シアノアミン化、加水分解によってグルタミン酸のラセミ体が得られる[5]。3つの反応行程が必要で、需要の多いL-グルタミン酸だけを生産できず、これをさらに分離する行程が必要になる。また、異物混入事故による健康被害、発がん物質、製造過程で発生する公害など、化学合成物を食品添加物として利用することへの不安を払拭できず[5]需要拡大には至らなかった。
酵素促進合成法 編集
生合成にも使われているグルタミン酸デヒドロゲナーゼや、アミノトランスフェラーゼ、グルタミン酸合成酵素などの酵素と補酵素の作用によって、それぞれ異なる原料から製造する方法もある。
アミノ酸発酵法 編集
細菌、酵母などの微生物のアミノ酸代謝を人為的な変換により過剰に産生させ体外に排出蓄積させる技術をアミノ酸発酵という。1955年、協和発酵(現・協和発酵バイオ)の田中 勝宣、中山 清、木下祝郎、鵜高重三(日本学士院賞受賞)[6]がグルタミン酸生産菌を発見し、発酵法による工業的な生産技術を翌1956年に世界に先駆けて軌道に載せた[7]。原料の糖蜜、粗糖、糖液の調達コストの兼ね合いから生産のほとんどは海外で行われている。
出典 編集
- ^ 軟水と硬水について 株式会社コスモライフ
- ^ 硬水・軟水で料理の味が変わる 味博士の研究所
- ^ 軟水、硬水はどのように使い分けされているのでしょうか。日本ミネラルウォーター協会
- ^ a b 鈴野弘子、豊田美穂、石田裕「ミネラルウォーター類の使用が昆布だし汁に及ぼす影響」『日本食生活学会誌』第18巻第4号、日本食生活学会、2008年、376-381頁、CRID 1390001205198484736、doi:10.2740/jisdh.18.376、ISSN 1346-9770。
- ^ a b c 中森茂「アミノ酸発酵技術の系統化調査」『平成19年度技術の系統化調査報告』、国立科学博物館、2008年、53-91頁、NDLJP:11546646、2024年1月22日閲覧“国立国会図書館デジタルコレクション”
- ^ “日本学士院賞 「醱酵によるアミノ酸類の生成に関する研究」” (PDF). 日本学士院. 2022年5月8日閲覧。
- ^ アミノ酸発酵 - 日本大百科全書(ニッポニカ) コトバンク
