気管支喘息
気管支喘息(きかんしぜんそく、英語: bronchial asthma)または喘息(ぜんそく、英語: asthma)は、慢性の気道炎症(2型炎症が主体の表現型が典型的であるが、それ以外にも多様な表現型が存在する)、気流制限(典型例では、通常、可逆性あり)、気道過敏性の亢進を病態の基盤に有し、発作性に、呼吸困難、喘鳴[1]、咳などの呼吸器症状の増悪をきたす症候群である。なお、末梢気道病変の喘息で聴かれる喘鳴は主として呼気性喘鳴(Wheezing)である[2]。
| 気管支喘息 | |
|---|---|
 | |
| 呼気の流量の最大値を計測するピークフローメーター | |
| 概要 | |
| 診療科 | 呼吸器学, 免疫学 |
| 分類および外部参照情報 | |
| ICD-10 | J45 |
| ICD-9-CM | 493 |
| OMIM | 600807 |
| DiseasesDB | 1006 |
| MedlinePlus | 000141 |
| eMedicine | article/806890 |
| Patient UK | 気管支喘息 |
| MeSH | D001249 |
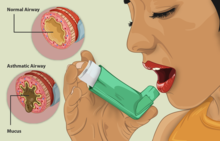
喘息は東洋医学では哮喘と称される(哮は発作性の喘鳴を伴う呼吸疾患で、喘は保迫するが喘鳴は伴わない呼吸疾患である。双方は同時に見られることが多いため、はっきりと区別することは難しい。虚証・実証に区別はされるが、気機〈昇降出入〉の失調で起こる)。
なお、鬱血性心不全により喘鳴、呼吸困難といった喘息類似の症状がみられることがあるが、喘息とは異なる病態である。
喘息をはじめとするアレルギーが関与する疾患の治療に関して、欧米の医師と日本の医師との認識の違いの大きさを指摘し、改善可能な点が多々残されていると主張する医師もいる。
歴史
編集喘息を指す英単語 asthma はギリシャ語の「aazein」という"鋭い咳"を意味する言葉に由来する[3]。この言葉は紀元前8世紀のイーリアスに登場するのが最初とされている。紀元前4世紀にヒポクラテスはこの病気が仕立て屋、漁師、金細工師に多いこと、気候と関係していること、遺伝的要因がある可能性があることを記載した。2世紀にガレノスは喘息が気管支の狭窄・閉塞によるものであることを記し、基本病態についての考察が始まった。
その後喘息についてさまざまな考察、文献が発表されたが、このころまで喘息という言葉は今日でいう喘息のみならず呼吸困難をきたすさまざまな病気が含まれていた。今日でいう喘息についての病態にせまるには17世紀まで待たねばならない。17世紀にイタリアのベルナルディーノ・ラマツィーニは喘息と有機塵との関連を指摘し、またイングランドのジョン・フロイヤー (医師)は1698年、A Treatise of the Asthmaにおいて気道閉塞の可逆性について記載した。1860年にはイギリスのソルターは著書On asthma:its pathology and treatmentの中で気道閉塞の可逆性と気道過敏性について述べ、またその後19世紀末から20世紀初頭にはアドレナリンやエフェドリンが開発され、気管支拡張薬が喘息の治療として使用されるようになった。この頃まで喘息の基本病態は可逆性のある気管支収縮であると考えられていた。
1960年代に入り喘息の基本病態が気道の慢性炎症であることが指摘され始め、1990年にイギリス胸部疾患学会(BTS)の発表した喘息ガイドライン、および1991年にアメリカ国立衛生研究所 (NIH) の発表した喘息ガイドラインにおいて「喘息は慢性の気道炎症である」ことにコンセンサスが得られた。これによりステロイド吸入により気道の炎症を抑え、発作を予防するという喘息の治療戦略が完成し、治療成績が改善した。しかし、吸入ステロイドの普及率は、国・地域によって差があり、殊に、日本は欧米先進諸国に比し、吸入ステロイドの普及率は低い。
症状
編集煙、排気ガスなどの刺激物、アレルゲン、気道感染、急激な寒暖差、運動、ストレスなどの種々の刺激が引き金となり、気管支平滑筋、気道粘膜の浮腫、気道分泌亢進などにより気道の狭窄・閉塞が起こる。気道狭窄によって、喘鳴(ぜんめい:喉のゼーゼー、ヒューヒューという音)、息切れ、咳、痰(たん)などの症状を認める。喘息発作時にはこれらの症状が激しく発現し、呼吸困難や過呼吸、酸欠、体力の激しい消耗などを伴い、時には死に至ることもある。
発症因子
編集大気汚染
編集煙(粒子状物質)への曝露は強い発症因子であることが判明している。
- たばこ たばこの煙(副流煙)は喘息の発症、憎悪の原因となる[4][5]。
- 野焼き 秋田県において、米の収穫後の野焼きの時期に喘息患者が急増することが報告されている[6]。
- ばい煙 工場やディーゼル車の排出するばい煙は四日市ぜんそくの主因であり、四大公害の一つに数えられる。
- 線香 線香の煙と喘息の発症数には有意な相関があることが示されている[7]。
- 粉塵 火山灰などの粉塵は喘息の憎悪要因である[8]。
ヨーロッパにおいては、大気汚染と新生児アレルギー感作の増大の関連は結論されていない[9]。
食習慣
編集野菜と果物の摂取はそれぞれ、喘息のリスクと重症度を下げるようである[10]。小児の野菜と果物の消費量に応じて、喘息のリスクが下がる関係が見られ、妊娠期の母親の消費量はその子のリスクに無関係であった[11]。一方、妊娠初期にアブラナ科の野菜(ブロッコリー、カリフラワー、キャベツ、クレソンなど)を摂取すると幼児の喘息症状の発生率軽減するというデータもある[12]。22研究中17が野菜と果物は喘息やアレルギーの予後を良好にしているという関係が見られた[13]。20か国29施設が参加した国際研究でも、野菜と果物の消費量が発症率に関係することが見いだされた[14]。 牛乳の消費と喘息の増加には関連があるが、単純な因果関係では説明できず、一部の喘息の人々では粘液産生を促している可能性がある[15]。
動物との接触
編集猫への曝露は、喘息のリスクに対してわずかに予防的、逆に、犬への曝露はリスクをわずかに増加させており、追加の研究が必要だとされた[16]。BCGワクチンの予防接種による喘息の予防効果は一時的である[17]。
環境緑化
編集分類
編集分類法も複数存在するが、代表的なものの一つに、幼児期に発症することの多いアトピー型と40歳以上の成人発症に多くみられる非アトピー型の2型の表現型に分類する方法がある。喘息はIgE型の免疫不全症であるため、アトピー性皮膚炎などと合併してくることが多くみられる。
アトピー型喘息(アレルギー性喘息)
編集吸入アレルゲンに対して遅発性喘息反応が起こることがある。曝露後、数時間から数日間気道過敏性が亢進するのだが、詳細な機序は不明である。過敏性肺炎とは異なりI型アレルギーである。
非アトピー型喘息
編集小児喘息
編集小児喘息は成長とともに寛解する場合が多いが、成人喘息に移行する場合もある。小児期に喘鳴が認められる場合はウイルス感染、アレルギー、異物の可能性がある。重要な鑑別疾患としてはRSウイルスによる細気管支炎があるが、細気管支炎では一日中喘鳴が聴取されるが、気管支喘息はヒューヒュー、あるいはゼイゼイとした喘鳴が夜間に多い。小児喘息の診断には、他疾患の除外が必要である。2歳から3歳のころ頻繁に喘鳴を繰り返す 幼児は小児喘息に移行するリスクが高いと考えられている。
- major criteria
-
- 医師によって診断された両親いずれかの喘息の既往。
- 医師によって診断されたアトピー性皮膚炎
- minor criteria
-
- 医師によって診断されたアレルギー性鼻炎。
- 上気道感染と関連しない喘鳴。
- 4%以上の好酸球の増加
major criteriaひとつまたはminor criteria2つで小児喘息の確率は76%である。逆に満たさなければ5%の確率となる。
小児喘息のガイドラインとしてはJPGL2005が知られている。春先や秋口などが発作の好発時期である。3歳から5歳の発症が多い。β2刺激薬の吸入とステロイドの全身投与が基本となる。アミノフィリンは嘔吐といった副作用をはじめ、血中濃度の調整が難しく、安全性、簡便性を考慮すると消極的になる。吸入は吸入器(定量噴露吸入器とドライパウダー吸入器)とネブライザーによる吸入が知られている。吸入薬の量は小児であろうが成人であろうが変化がないのが一般的である。これは成長するほど上手に吸入できる傾向があるため、末梢気道に達する薬物量が増えるためである。ネブライザー治療に影響を与える因子としては呼吸パターン、口呼吸か鼻呼吸か、気道狭窄病変の程度、人工気道の存在などがあげられている。
小児喘息の治療の目標とは軽いスポーツを含め、日常生活を普通に行うこと、昼夜を通じて症状がないこと、β2刺激薬の頓用の減少、学校の欠席の防止、肺機能障害の予防、PEFの安定化とされている。
小児分野では年齢により薬剤の選択も異なり専門性の高い分野であるがJPGLにてかつてよりは簡略化されている。大まかに述べると2歳未満の乳児喘息、2歳から5歳、6歳から15歳という区分で分けられている。アトピー性が多いためDSCGを積極的に使うこと、吸入技術の問題で吸入ステロイドの適応が若干異なる。ラーメンやうどんが食べられるようならば、原理的には吸入は可能であり、吸入をサポートするスペーサーも各種販売されている。
乳児喘息では中等度でも専門医の下で治療を行うこと、2歳から5歳では軽症持続型の段階ではICSは考慮に過ぎない、6歳以上では軽症持続型以上ならばICSが原則となるといった差がある。
日本で増加する小児喘息に関しても、安全かつ有効な標準化ダニアレルゲンを用いた減感作療法をすることで、小児喘息患者の肺機能の改善,成長,維持を助けて健康な成人を育てることが厚生医療行政の急務であると主張している医師もいる。
咳喘息 (cough variant asthma)
編集咳喘息は厳密には喘息とは異なる疾患として扱われる。喘息と同様気道に炎症が起こり、気道が狭くなることで咳が出る。主な特徴は[19][20]、
- 喘息特有の喘鳴は無い
- 呼吸困難も無い
- たんの無い乾いた咳が8週間以上続く(慢性咳嗽)
- 夜~明け方、季節の変わり目に悪化する
一般的な風邪薬や咳止めは効果が無く、気管支喘息で用いる気管支拡張薬、吸入ステロイド薬の吸入(後述)が有効とされる。 症状は、慢性(8週間以上)に発作性の咳が持続することが特徴的である。交感神経β2受容体作動薬(β2刺激剤)の吸入により臨床症状が改善するため、治療的診断として有用である。典型的な喘息と異なり、通常、胸部聴診にて狭窄音は聴取されず、閉塞性換気障害や気道可逆性等、異常所見が認められないため、確定診断に難渋し、ドクターショッピングを引き起こすことも多い。 喘息と同様の病態(慢性の気道炎症、気道過敏性の亢進等)が基盤にあることが判明しており、これらの評価が可能な専門医療機関等を受診することが望まれる。通常、咳喘息における気道炎症や気道過敏性亢進の程度は、喘息に比し軽微であることから、喘息の前段階として認識されることもあり、軽症喘息におけるコントローラーに準じた定期的薬物療法が導入されることが多いが、重症の咳喘息症例も存在し、重症喘息と同等の治療を要することもある。咳喘息を無治療で放置すると、約3割が典型的な喘息に移行するとされる。
気管支喘息治療薬は「長期管理薬」(コントローラー)と「発作治療薬」(リリーバー)に大別される。発作が起きないように予防的に長期管理薬を使用し、急性発作が起きた時に発作治療薬で発作を止める。発作治療薬を使う頻度が多いほど喘息の状態は悪いと考えられ、長期管理薬をいかに用いて発作治療薬の使用量を抑えるかということが治療の一つの目標となる。
長期管理薬では吸入ステロイド薬が最も重要な基本薬剤であり、これにより気管支喘息の本体である気道の炎症を抑えることが気管支喘息治療の根幹である。重症度に応じて吸入ステロイドの増量、経口ステロイド、長時間作動型β2刺激薬(吸入薬・貼り薬)、抗アレルギー薬、抗コリン剤などを併用する。長期管理薬を使用しても発作が起こった場合は、発作治療薬を使用する。発作治療薬には短時間作動型β2刺激薬、ステロイド剤の点滴などが使われる。
1997年、β2刺激薬であるベロテックエロゾル(臭化水素酸フェノテロール)の乱用による死亡者増加が日本において大きな問題となった。これはβ2刺激薬の副作用によるものとは言えず、β2刺激薬の吸入により一時的に症状が改善するために大発作に至る発作でも病院の受診が遅れたことが主因と考えられている。
アスピリン喘息
編集喘息患者の何割かが獲得するアセチルサリチル酸(アスピリン)などの非ステロイド系抗炎症薬 (NSAIDs)、特にシクロオキシゲナーゼ阻害薬(主にCOX1阻害薬)に対する過敏体質であり、アレルギーによるものではない。NSAIDsの服用から数分から1時間後に鼻汁過多、鼻閉、喘息発作が起こる。このように症状が、上気道、下気道に及ぶことから、近年、non-steroidal anti-inflammatory drugs exacerbated respiratory disease (NERD) と呼称されるようになった。成人女性に好発し、小児では稀である。
アトピー型、非アトピー型喘息患者のいずれにおいても認められ、中等症以上の症例が多く、急性増悪時には、しばしば、重度の呼吸器症状をきたす。病歴から診断可能な例もあるが、確定診断のためにアスピリン負荷試験を要することが少なくない。成人喘息患者の約21%は誘発試験でアスピリン喘息を起こしたとの報告がある[21]。
COX1阻害によるプロスタグランジンの阻害とそれに伴うロイコトリエン (LT) 代謝経路に傾くことによる代謝異常が病態の基盤にあるため、COX2阻害薬投与においては発生率が低下する。しかし、COX2阻害薬も他のNSAIDsと同様、添付文書上、喘息患者には禁忌とされている。
病態の特徴の一つにロイコトリエンの過剰産生があり、そのためロイコトリエン拮抗薬が用いられることが多い。好酸球性副鼻腔炎の合併率が極めて高く、鼻茸や嗅覚低下を合併することが多い。他臓器の好酸球性疾患の合併もみられる。
アスピリン喘息の急性増悪ではコハク酸エステル型ステロイド(コハク酸ヒドロコルチゾン(ソル・コーテフTM)、ソル・メドロール、水溶性プレドニンなど)の急速静注は喘息の増悪を誘発することがある(ステロイド自体やコハク酸残基が誘因になった報告があり、リン酸塩は安全とされる。溶解液中安定剤パラベンはしばしば誘因になる)。1時間以上かけて点滴を行えば比較的安全とされている。リン酸エステル型ステロイド薬(デカドロン、リンデロン、ハイドロコートンなど)を1時間以上かけて点滴投与する。
おおよそ気管支喘息の10%がアスピリン喘息(アスピリン不耐症)とも言われ、総ての酸性NSAIDsは原則禁である。アセトアミノフェンやCOX2阻害剤は比較的安心とも言うが原則禁で基本は冷罨法である。アセトアミノフェンは少量ならば使用可能とする意見もある。塩基性NSAIDs(ソランタール®等)葛根湯、地竜は使用可能とされる。症状発現の程度は様々で数分でショック状態に陥る強い発作もあれば風邪がダラダラ長引いて治らないと訴える場合もある。またその使用時に常に症状発現するとは限らないことが診断を難しくしている。NSAIDsやβブロッカーの点眼液でも発作が出現することもある。
運動誘発性喘息
編集健常者では運動によって気道の径が変化することはないが、喘息患者の場合は運動によって気管収縮が誘発される。特に、運動によって臨床的な症状が出現する場合を運動誘発性喘息という。運動が刺激因子となり、肥満細胞からのロイコトリエン産生が増加する病態が基盤にあるため、ロイコトリエン拮抗薬が効果的である。インタール吸入にもその誘発予防効果がある。
病態生理学
編集臨床医にとっては、いくつかの呼吸器症状が喘息と診断するための情報となるが、これらの臨床症状は必ずしも喘息のみに特異的ではない。発作性の喘鳴、咳、息切れ、胸部の圧迫感(時間により程度が変化し、気管支拡張薬にて改善する)などが喘息を疑う所見としている。
病理学者は組織学的に定義を行っており、好酸球の浸潤や気道壁の肥厚、リモデリングによって特徴づけられる持続性の炎症と喘鳴としている。
生理学者は機序によってその都度定義を行っており、多くの異なる刺激に反応して、過剰な気管支平滑筋収縮を引き起こす気道過敏性の状態を気管支喘息と定めている。生理学的な定義のうち特に重要なのが、運動誘発性喘息や吸入アレルゲンによる喘息、アスピリン喘息である。上記、歴史の項に述べられているようにいずれの定義でも再発性の気道過敏性と慢性炎症といった病態生理学に統合されると考えられている。慢性気道炎症によって気道過敏症となり、増悪因子により気道狭窄がおこり喘息症状が起こるとされている。
喘息患者にβ1受容体選択性の高くないβブロッカーを用いる場合、重篤な気管支収縮が起こる可能性がある。
疫学
編集2004年の試算で全世界に3億人の喘息患者がおり、年間255,000人が喘息で死亡している[22]。また喘息死の80%以上は低所得国から中低所得国で発生しており、今後10年間で喘息死はさらに20%増えるだろうと予測されている。喘息の有症率は1% - 18%程度と国によって報告にばらつきがあるが、多少強引にまとめると先進国で5% - 10%程度、発展途上国では1% - 4%程度である。
日本では1996年の統計で喘息の累積有症率(現症と既往の合計)は乳幼児5.1%、小児6.4%、成人3.0%(16歳から30歳では6.2%)である[23]。1960年代は小児、成人とも有症率は1%程度であったものが近年増加の傾向にあり、10年の経過で1.5倍から2倍程度増加している[24]。日本における喘息による死亡者数と人口10万人あたりの死亡率は1995年には7,253人 (5.8%)、2000年には4,473人 (3.6%)、2001年には4,014人 (3.2%)、2002年には3,771人 (3.0%)、2003年には3,701人 (2.9%)、2004年には3,283人 (2.6%) と、年々低下傾向にある(厚生労働省人口動態統計より)。死亡者の約半数は、重度の発作を軽発作だと思い適切な治療が遅れたあるいはされなかった事が原因であるといわれている。
検査
編集- 理学所見
- 特に、急性増悪時には、胸部聴診にて、呼気時優位に狭窄音が聴取される。狭窄音には、笛声音(wheeze「ウィーズ」, piping rale)、rhonchi等がある。急性増悪時には、呼気延長を認め、さらに、進行すると、陥没呼吸等、努力呼吸を呈するようになり、呼吸数増多(英: tachypnea)やチアノーゼを伴うこともある。最重症の急性増悪においては、意識障害や、呼吸音が減弱して喘鳴が聴取されなくなるsilent chestに至ることがあるが、極めて危険で緊急の処置を要する状態である。理学所見は気候や時間帯による影響も受ける。
- 気道可逆性試験
- 気道閉塞の可逆性は喘息に特異性が高いが、気道閉塞の可逆性はないと考えられていた慢性閉塞性肺疾患(COPD)でも気道閉塞の可逆性が存在する症例があることが示されている。米国胸部疾患学会の基準では、β2刺激薬吸入前後、1秒量が200ml以上かつ12%以上改善した場合、気道可逆性ありと診断する。あるいは2週間から3週間のステロイド内服・吸入前後で評価することも可能である。ただし検査時に喘息発作が起きていない場合、気道の可逆性を証明できないこともあるため自宅にピークフローメーターを持って帰ってもらい、ピークフロー値に20%以上の日内変動がみられた場合も気道可逆性ありと診断できる。
- スパイロメトリー
- スパイロメーターを用いた呼吸機能検査。喘息では気道の狭窄により呼気の排出速度が低下する。(FEV1.0<75%)
- 広域周波オシレーション法
- 音響スピーカーなどによる工学的な空気振動(オシレーション波)を,安静換気している被験者に伝搬させ,口腔内の気流と圧を測定する。
- 血液ガス分析
- 非発作時には異常を認めないことが多い。喘息発作時には酸素分圧は正常ないし低下、人体の防御反応として呼吸回数上昇による低酸素状態からの回復が図られるため、過呼吸を反映して二酸化炭素分圧が低下することがある。また、その反対に、気管支狭窄・閉塞が高度な場合、肺胞低換気を反映して二酸化炭素分圧はむしろ上昇する。この場合、低酸素状態を伴う場合が多い。
- 胸部X線写真
- 特に、喘息急性増悪時に肺過膨張を認めることはあるが、それ以外は、異常を認めないことが多い。喘鳴や気道狭窄をきたす他の疾患(腫瘍や肺炎、慢性閉塞性肺疾患など)や鬱血性心不全の除外、無気肺、気胸、縦隔気腫などの併発に留意することが重要である。
- 血液検査
- 末梢血中好酸球の増加や血清中の非特異的IgE値の上昇がみられれば、本疾患の補助診断となりうる。また、アレルゲンを調べるために、血清中のアレルゲン特異的IgE抗体の測定や、皮膚テスト(プリックテスト等)が行われる。
- 病理学的所見
- 気管支壁に好酸球浸潤と平滑筋肥大が認められる。
- アスピリン喘息では鼻茸など、特異的鼻粘膜所見を確認することが、有力な診断の補助となる。
- 専門的検査(専門的医療機関以外では施行されていない)
- 呼気中の一酸化窒素 (NO) 濃度は、気道炎症と相関し、非侵襲的かつ簡便に測定することが可能である。2013年より、一部の測定機器による呼気中NO濃度測定の保険適応が認められるようになったが、測定器具と試薬が高価であり保険点数では採算が取れない検査であるために、実施できる医療機関は限定される。呼気中NO濃度は、鼻炎、気道感染、喫煙などの要因によっても影響を受けることに留意すべきである。そのほか、気道炎症を評価する手法として、極めて限られたごく一部の専門施設において、呼気凝縮液中の種々のバイオマーカーの測定が施行されている。呼気凝縮液は、非侵襲的に、かつ比較的簡便に採取することが可能である。
- 気道過敏性の亢進は、喘息の病態の根幹を成し、その評価は極めて重要である。いくつかの評価方法があるが、いずれも、被験者に気道を刺激する物質を低濃度より吸入負荷し徐々に負荷量を漸増して喘息の病態を生じさせ、1秒量や呼吸抵抗などの指標が有意に変化するまでに要した負荷総量により、気道過敏性を評価する。負荷物質として、メサコリンが選択されることが多い。日本では、主に標準法とアストグラフ法が施行されており、評価のために用いる指標等が異なる。
治療
編集薬物療法
編集抗炎症薬
編集- 経口ステロイド薬
- 1950年代にコルチコステロイドが精製されるとすぐに喘息の治療に用いられた経歴がある。気管支拡張薬で反応しなかった重度の喘息でも極めて有効であったが、長期にわたって全身投与を行うと多くの有害な副作用が出現するため、緊急時の短期間投与のみが行われる。例外としてはステロイド依存性喘息であり、やむをえず、長期ステロイド全身投与を行う。民間療法でステロイドの有害性を過度に強調する情報があるが、これらは吸入ステロイドをはじめとする治療ができる以前の報告である。
- 吸入ステロイド薬 (ICS)
- 喘息長期管理薬の第一選択として用いられるが、ICS/LABA合剤の一つであるBudesonide/Formoterolは発作治療薬としても使われることがある(SMART療法)。バイオアベイラビリティ(吸収されて血流中に残り、全身に分布する量)が低い薬剤が用いられるため、全身性の副作用(高血圧、肥満、骨粗しょう症、身長の伸びの抑制など)はほとんどないと考えられている。薬物量においても、全身投与ではmg単位必要であるのに対して、吸入ではμg単位で治療が可能である。嗄声、口腔内カンジダなどの副作用は起こりえるが、吸入直後に入念なうがいをして喉と口腔内から薬剤を洗い流すことで防ぐことができる。ICSを低用量から高用量へ増量するよりも低用量ICSにLABAやLTRAあるいはLAMAを併用した方がコントロールが良くなる傾向がある。このような報告や吸入薬は全身影響が少ないこともあり、合剤が販売されるようになっている。ICS/LABA合剤として、アドエア、シムビコート、ブデホル、レルベア、フルティフォーム、アテキュラがあり、ICS/LABA/LAMA合剤において、エナジア、テリルジーに気管支喘息の適応がある。気管支喘息において、これらの合剤は、リスクを上げることなく発作を減らすことが報告されている[25]
- 吸入器には定量噴露吸入器 (pMDI) と自己吸気によるドライパウダー吸入器 (DPI) が存在する。フルタイドディスカス・ロタディスク、パルミコート・タービュヘイラー、アズマネックスツイストヘラー、アニュイティエリプタといったドライパウダー製剤、キュバール(ベクロメタゾン)、オルベスコ(シクレソニド)、フルタイド・エアーといったガス噴霧製剤(エアロゾル)がある。またドライパウダー製剤・ガス噴霧製剤などが上手に吸入できない小児などのために、デポ・メドロール(酢酸メチルプレドニゾロン)、パルミコートにはネブライザーで吸入できる吸入液がある。ガイドラインに基づく治療をしている場合はLABA、LAMAと併用を行う場合が多いため、ICS/LABA合剤あるいはICS/LABA/LAMA合剤は、携帯する薬品、吸入回数が減ることで利便性が高い。
- ロイコトリエン受容体拮抗薬(LTRA)
- 代表的な経口喘息治療薬。軽症や吸入ステロイド薬の使用が困難である症例においては単独で使用されることが多い。中等症〜重症では一般的には吸入ステロイド薬の併用薬として使用される。リモデリング予防・改善効果、運動誘発性喘息、アスピリン喘息、鼻閉を伴うアレルギー性鼻炎や月経困難症および子宮内膜症の合併では特に使用を推奨されている。好酸球性多発血管炎性肉芽腫症(チャーグストラウス症候群)発症のリスクの可能性が指摘されたが、否定的な報告もある。代表的なLTRAには、プランルカスト(商品名オノンなど)、モンテルカスト(商品名シングレアなど)がある。効果発現は薬剤によってことなるが、プランルカストでは2週間、モンテルカストでは1日で自覚症状が改善するというデータがある。アトピー性が多い小児では好まれる。プランルカストは小児の場合は1歳以上に適応があり、カプセル (112.5mg) とドライシロップ (10%) の製剤が知られており7mg/Kg/dayで最大量は450mg/dayである。朝夕に分服する。モンテルカストはチュアブル錠 (5mg) が6歳以上15歳未満、細粒 (4mg) が1歳以上6歳未満の適応があり、1日1回1錠を就寝前に投与される。特に小児ではJPGL2008ですべてのステップで第一に推奨されている薬剤である。ただしロイコトリエンが関与しない喘息もあり、約60%の患者に効果がみられる。
- ケミカルメディエーター遊離抑制薬
- クロモグリク酸吸入液(DSCG、インタール等)は肥満細胞の脱顆粒を抑制する薬である。直前に1回吸入するだけで運動や抗原吸入によって引き起こされる気管支収縮を軽減できる。しかし、その効果は吸入ステロイドに劣り、また発作の治療に用いることもできない。非アトピー性が多い成人の喘息では用いる機会はかなり少ないものの、アトピー性が多い小児喘息では比較的効果があり有害な副作用がないということもあり小児科では非常に好まれる薬物である。クロモグリク酸吸入液は (20mg/2ml) で1回1Aで一日3回から4回、電動式ネブライザーを用いて治療を行う。
- 抗アレルギー薬
- スプラタミド、ケタスなどといった化学伝達物質阻害剤、ケトチフェン、アゼラスチンといった抗ヒスタミン剤なども処方されることがある。one airway one diseaseという考え方が提唱されており、喘息とアレルギー性鼻炎や副鼻腔炎を同時に治療すると効果的と考えられている。
気管支拡張薬
編集- β2刺激薬
- 短時間作用型 (SABA) の吸入薬は急性増悪時にリリーバーとして用いられる。長時間作用型の製剤 (LABA) はコントローラーとして用いられるが、単独使用は推奨されない。前述の通り、ICS/LABA合剤の一つであるBudesonide/Formoterolはコントローラーとしてのみならずリリーバーとしても使われることがあり(SMART療法)、GINAの喘息急性増悪時治療ガイドラインに記載されている。
- 短時間作用型吸入薬 (SABA)
- サルブタモール(サルタノール・インヘラーやベネトリンなど)、プロカテロール(メプチン・エアーなど)、フェノテロール(ベロテック・エロゾルなど)など。即効性はあるものの、効果はすぐに減弱するため、コントローラーとしては用いられない。
- 長時間作用型吸入薬 (LABA)
- 単剤として、サルメテロール(セレベント・ディスカスなど)、ICS/LABA合剤として、プロピオン酸フルチカゾン・サルメテロール(アドエアなど)、ブデソニド・ホルモテロール(シムビコート、ブデホル)、フランカルボン酸フルチカゾン・ビランテロール(レルベア)、プロピオン酸フルチカゾン・ホルモテロール(フルティフォーム)、モメタゾン・インダカテロール(アテキュア)、ICS/LAMA/LABA合剤として、モメタゾン・グリコピロニウム・インダカテロール(エナジア)、フランカルボン酸フルチカゾン・ウメクリジニウム・ビランテロール(テリルジー)がある。セレベントは一回25 - 50μgを一日二回投与が一般的である。アドエアでは一回にサルメテロールが50μg含まれている。かつてはβ刺激薬の心臓作用が気管支喘息患者の突然死の原因と考えられていたが、ICSの普及によってむしろ炎症コントロールの程度が突然死とかかわりあっていると考えられるようになった。食品医薬品局(しょくひんいやくひんきょく、FDA:Food and Drug Administration)は、喘息長期管理(慢性期治療)における、LABAの単独使用を避けるよう警告している。
- 貼付剤、内服薬などの剤形もあり、年齢・症状にあわせてそれぞれ用いられる。
- 貼付剤としては小児科領域ではツロブテロール製剤のホクナリンテープがよく用いられる。0.5 - 3歳未満ならば0.5mg、3歳から9歳未満ならば1mg、9歳以上ならば2mgで胸部や背部や上腕部に貼付する。副作用は内服薬と同様で吸入薬よりは強い。また、効果発現時間は極めて遅いため急性期の対応では全く役に立たないが、服薬が難しい小児の分野では使い勝手の良さから非常に好まれる。内服薬ではアトック(ホルモテロール)やホクナリン錠、メプチン錠など多くの製剤がある。
- メチルキサンチン系薬物
- テオフィリン(テオロング、テオドール他)製剤である。テオフィリンは気管支拡張作用と抗炎症作用を併せ持つ。かつては気管支喘息の中心となる極めて頼りになる薬物であった。その薬物動体を理解して上手く使えば気管支喘息治療の極めて有効な治療薬となっていたが、その特性を理解しておかないと、残念ながらその血中有効濃度域が狭くかつ脱水・心不全・肝障害・併用薬剤相互作用・個人差等で簡単に中毒域に入ってしまうために、その使用法が難しく敬遠されるようになってしまった。中毒症状は多彩で重度のものは不整脈・痙攣・意識障害もある。分かり易いものは嘔気・嘔吐・動悸・食欲不振等がある。慢性難治性でβ blocked stateでβ刺激剤に反応不良の気管支喘息発作でも効果が期待できた。
- 錠剤やカプセルの形態で徐放性製剤としては経口投与を行い、急性増悪ではテオフィリンおよびそのジエチルアミン塩であるアミノフィリンの静脈内投与を行うことができる。アミノフィリン静注では急速静注は禁止であり、ゆっくり1~2分以上かけて静注する。又は点滴静注が無難である。急速静注は酸素需給バランスの破綻によるとされる心筋障害を生じる。
- β刺激薬がアデニル酸シクラーゼを活性化させcAMPを上昇させるのに対して、テオフィリンはホスホジエステラーゼを阻害することでcAMPを上昇させる、結果はどちらもPKA活性化による気管支の拡張である。また、気管支喘息とCOPDに対してヒストン脱アセチル化酵素活性の増強作用による抗炎症作用や横隔膜の収縮力増強や呼吸中枢刺激作用も報告されている。徐放性テオフィリン製剤は喘息症状の改善のほか、肺機能の改善、就寝前の内服で夜間症状の改善、運動誘発性喘息の予防、低濃度での抗炎症作用が知られている。しかし治療域は非常に狭く、代謝に個人差があるため投与量の設定も個人ごとに異なり5 - 15μg/mlに血中モニタリングが必要である。また多くの薬物との相互作用が知られている。副作用には中枢神経の賦活作用による痙攣、悪心、頻脈、振戦、不整脈などがある。このような調節が難しいことから長時間作用型のβ刺激吸入薬の普及に伴い、あまり用いられない傾向にある。テオフィリン関連痙攣と呼ばれる副作用が報告され、日本のガイドラインでは小児に対してはその位置づけが後退傾向にある。この痙攣も典型的な中毒症状の一つである。テオフィリン系は心筋の酸素需要を高めるので急速静注は酸素需給バランスを悪化させて不整脈等を惹起しかねないので数分掛けてのゆっくり静注ないし点滴が好ましい。
- 小児では抗炎症効果を期待して低用量の10mg/kg/dayから使用を開始し血中濃度を10μg/ml程度を目安にするのが一般的である。血中濃度は迅速キットで測定可能であるため、内服量が不明な時もERで追加が可能である。そのためアミノフィリンは発作治療薬としてしばしば用いられている。
- テオフィリン内服薬も吸収率は約100%と良好なのでネオフィリン等静脈注射用薬と同様の注意は必要である。例えば脱水状態になれば通常量でも容易に中毒域に入ってしまう。使用法のノウハウは日本でも米国でもかつて様々に工夫されて1970年代までは米国でもアミノフィリン100mgワンショット静注が良く効くと主張する医師もいた。しかし100mg静注でも急速に行えば心筋障害や不整脈を誘発しかねないし、脱水著明等全身状態が悪ければゆっくり数分かけて静注しても中毒症状が出ることがある。これらの臨床薬理学的検討は1970年代に石崎高志らにより詳細に検討されて(Japanese Journal of Allergology 29(5): 203-212, 1980. 、Medicina21巻4号1984. https://doi.org/10.11477/mf.1402218985等)、使用法も理解されるようになったが残念ながら一般化されることなく、安易な使用での痙攣などの副作用(中毒症状)が前面に出てきて問題化され近年は敬遠されるようになってきている。なお、血中濃度有効域は10-20㎍/mlとされたが、それより低濃度でも効果があることが主張されるようになってからは少量投与で使われることが多くなっている。医師による全身状態の定期的チェックなしで漫然と使うのはやはり控えた方が良い。
- 抗コリン薬
- 吸入抗コリン薬はβ2刺激薬に比べ、気管支拡張効果が弱く、効果発現が遅い。また、呼吸器粘膜から吸収されることにより口渇感、前立腺肥大、頻脈、緑内障といった副作用が出現する恐れがある。アトロピンの4級アンモニウム塩であるイプラトロピウム臭化物(アトロベント等)ではこのような副作用は軽減されている。日本ではイプラトロピウムはMDIとしてのみ供給されており、次のような状況では有用性はある。βブロッカーにより気管支収縮が起こった場合、吸入β刺激薬に反応しない急性増悪時、モノアミンオキシターゼ阻害薬を服用している場合、重度の不整脈や不安定狭心症を合併しているため、交感神経系の刺激を回避したい場合などである。作用機序は気道が副交感神経にてトーヌスが維持されているため、トーヌスの維持を解除することで気管支拡張を得る。イプラトロピウム(アトロベントなど)、オキシトロピウム(テルシガン)は気道粘液の粘稠度を増加させないため非常に使いやすいとされている。作用持続時間は6 - 9時間である。
- COPDに対する定期治療薬として用いられるチオトロピウムは、近年、一部の喘息症例において、喘息コントローラーとしても有効であることが報告され、「スピリーバ®2.5µg レスピマット®60吸入」および「スピリーバ®1.25µg レスピマット®60吸入」は、気管支喘息を適応とした承認を取得している。また、抗コリン薬の一つであるグリコピロニウムおよびウメクリジニウムは、ICS/LABA/LAMA3成分配合剤として、気管支喘息に適応がある(商品名は、順に、エナジアおよびテリルジー)。
日本で喘息に適応を有する生物学的製剤
編集日本アレルギー学会の喘息治療ステップガイドラインには、以下の生物学的製剤は、いずれも、治療ステップ4における長期管理薬基本治療のオプションとして記載されており、全身性ステロイドの副作用に対する懸念から、近年、経口ステロイドよりも優先して推奨される傾向にある。
- ゾレア(一般名 オマリズマブ)(ノバルティス)
- ヌーカラ(一般名 メポリズマブ)(グラクソ・スミスクライン)
- ファセンラ(一般名 ベンラリズマブ)(アストラゼネカ)
- デュピクセント(一般名 デュピルマブ)(サノフィ)
- テゼスパイア(一般名 テゼペルマブ)(アストラゼネカ)
これらの生物学的製剤の内、デュピルマブのみが、日本アレルギー学会の喘息治療ステップガイドラインに、治療ステップ3における長期管理薬基本治療のオプションとしても記載されている。
その他
編集- 抗TNF抗体
- 近年注目されている分子標的薬である。
- 去痰剤
- ムコダイン,ムコサールなどがよく処方される。排痰に伴い、気道の抵抗が少なくなる。
- 14員環マクロライド
- エリスロマイシンなどの少量長期投与を行う医師もいる。慢性気管支炎、びまん性汎細気管支炎などの合併例には有効である。
- 漢方薬
- 麻杏甘石湯、小青竜湯、五虎湯、神秘湯、麦門冬湯などを、証に応じて処方。
気管拡張剤エフェドリンは、麻杏甘石湯、小青竜湯などに配合される生薬の麻黄から1885年(明治18年)長井長義によって単離抽出された。
減感作療法
編集中程度あるいは他の方法で喘息が制御できない場合はアレルゲンを繰り返し注射するアレルゲン免疫療法(減感作療法)を行う場合もある。90%以上がダニアレルゲンが原因である小児喘息の場合はアレルゲン免疫療法は有効性が高いという意見もある[26]。
WHOの見解書では、アレルゲン免疫療法(減感作療法)が喘息の自然経過を変える唯一の根本的治療法として記述されている[27]。
その他の治療
編集野菜と果物の摂取は、喘息のリスクと重症度を下げる[10]。ブロッコリー、モロヘイヤ、クレソンなどにはヒアルロニダーゼ抑制作用がある。ヒアルロニダーゼはアレルギーを引き起こす原因物質ヒスタミンの放出に関係しており、その働きを抑えることでアレルギー症状の軽減が期待される。また、キュウリ、野沢菜、クレソンなどにはヒスタミンの放出に関係する脱顆粒抑制作用がある。特にクレソンは高いレベルでヒアルロニダーゼと脱顆粒の両方を抑制する作用がある[28][29]。妊娠初期にアブラナ科の野菜(ブロッコリー、カリフラワー、キャベツ、クレソンなど)を摂取すると幼児の喘息症状の発生率軽減に寄与する可能性が示唆されている[12]。
古くから水泳によって改善するといったことも言われているが、呼吸筋を鍛えたことにより病状が良くなったと感じるため(ピークフロー値の上昇)で、炎症が治まったわけではない。場合によってはプールの塩素によってさらに悪化することもあり注意が必要である。水泳による疲労、塩素で喘息を発病した患者もいる。
直接の治療行為には該当しないが、ピークフローメーターにより日頃のピークフロー値の記録をしておくことで自覚症状のない軽い発作を発見できたり、発作がおきやすい時期、時間帯等を把握しやすくなるため、喘息の管理に有効である。ピークフローは症状の変化に先行し変化することが知られている。また重篤な患者ほど自覚症状が出現しにくいためピークフローによって客観的な評価が必要である。ピークフローは3回測定を行い、最高値を記録する。
慢性呼吸不全の患者には在宅酸素療法を行う。
管理
編集長期管理
編集喘息のガイドラインとして、国際的に最も信頼されているのは、WHOによるThe Global Initiative for Asthma (GINA) である。Evidence-levelの高い優れた最新の文献を基に、数年毎にアップデートされている。世界中の国・地域において、各々のローカルな喘息ガイドラインが存在するが、多くは、このGINAを参考に作成されている。他に、国際的に知られている喘息のガイドラインとして、米国喘息管理・治療ガイドライン (EPR3) がある。日本では、主に、日本アレルギー学会が作成する喘息予防・管理ガイドライン2021(JGL2021)および日本小児アレルギー学会が作成する小児気管支喘息治療・管理ガイドライン2023 (JPGL2023) が用いられる。
- 喘息に特徴的な症状
- 発作性の呼吸困難、喘鳴、夜間や早朝に出現しやすい咳。
- 可逆性気流制限
- 自然にあるいは治療により寛解する気流制限が認められる。PEF(ピークフロー)値の日内変動が20%以上、β2刺激薬吸入によって1秒率が12%以上増加、かつ絶対量で200ml以上の増加が認められる。
- 気道過敏性の亢進
- アセチルコリン、ヒスタミン、メサコリンに対する気道収縮反応の亢進が認められる。気道過敏性を認める疾患は喘息だけではなく、咳喘息、アレルギー性鼻炎、慢性閉塞性肺疾患、鬱血性心不全、ウイルス性呼吸器感染後などでも認められる。
これらによって気管支喘息と診断をしたら、長期管理を開始する。なお、発作中であったら発作の治療を優先する。長期管理の方法はガイドラインによってわずかな差異があるものの基本はほとんど同じであるためGINA2006に基づいて説明する。なおICSは吸入ステロイド、LABAは長期作用型β2刺激薬、LTRAはロイコトリエン受容体拮抗薬である。
| 薬物療法 | ステップ1 | ステップ2 | ステップ3 | ステップ4 | ステップ5 |
|---|---|---|---|---|---|
| 第一選択 | なし | 低用量ICS | 低用量ICS+LABA | 高用量ICSプラスLABA | 経口ステロイド |
| オプション | なし | なし | 高用量ICSまたはLABAの代わりにLTRA | LABAの代わりにLTRA | なし |
GINA2006では治療目標である良好なコントロールに関して問診によって評価できるとしている。
- 日中に週3回以上症状が出現
- 喘息によって日常生活によって制限がある
- 夜間に喘息症状のために早朝おきることがある
- 症状を抑えるために気管支拡張薬を週に3回以上使用
- ピークフローが自己最高値もしくは予測値の80%未満
- 喘息増悪発作が過去1年に1回以上ある
上記の6項目のうち3項目以上に該当したらコントロール不良であり、ひとつでも該当すればコントロール不十分、また喘息増悪発作が最近認められたらそれだけでコントロール不十分とする。3ヶ月ごとに治療効果判定を行い、コントロール良好群であれば、ステップダウンし、コントロール不良群であればステップアップする。コントロール不十分が持続する場合もステップアップを検討する。
JGL2006ではステップ1が症状によって規定されており、その症状にコントロールするようにコントローラーを決定する。ステップ2のコントローラーでステップ2の症状が認められればコントロール不良でありステップ3にステップアップする。
one airway one disease
編集喘息とアレルギー性鼻炎や副鼻腔炎がよく合併することはよく知られており、これらは独立した危険因子であるが関連が深く「one airway one disease」[注 1]として知られ[30]、同時に治療することで治療効果が高まると考えられている。特に、アレルギー性鼻炎や花粉症の合併は多い。アレルギー性鼻炎の治療は症状に合わせて選択される。
| 薬剤のタイプ | 鼻漏 | 鼻閉 | くしゃみ | かゆみ | 眼症状 |
|---|---|---|---|---|---|
| 経口抗ヒスタミン薬 | ++ | ± | ++ | ++ | ++ |
| 経口抗ロイコトリエン薬 | + | ++ | + | + | + |
| 点鼻抗ヒスタミン薬 | + | ± | + | + | - |
| 点鼻ステロイド薬 | ++ | ++ | ++ | ++ | + |
| 点鼻血管収縮薬 | - | ++ | - | - | - |
| 点鼻抗コリン薬 | ++ | - | - | - | - |
| 点鼻抗肥満細胞薬 | + | + | + | + | - |
急性発作
編集初期治療としては酸素投与とリリーバー投与となるが、呼吸困難、喘鳴の原因が心疾患など喘息発作以外の可能性もある。
喘息発作の程度は小発作(呼吸困難はあるが横になれ動ける)、中発作(呼吸困難で横になれないが動ける)、大発作(呼吸困難で動けない)に分類される。
| 軽度 | 中等度 | 重度 | |
|---|---|---|---|
| 呼吸困難 | 苦しいが横になれる | 苦しくて横になれない | 苦しくて動けない |
| 会話 | 通常会話 | 短い文章 | 単語のみ |
| 呼吸状態 | 呼吸補助筋の使用なし | 呼吸補助筋の使用あり | 胸骨上部陥凹(陥没呼吸) |
| PEF値 | > 80% | 60 - 80% | <60% |
| SpO2 | > 95% | 91 - 95% | <90% |
発作時の対処
編集- 初期治療
- まずは初期治療として酸素投与、および吸入β2刺激薬の投与を行う。シムビコートタービュヘイラー吸入を行う。
- また酸素飽和度 (SpO2) が92%以上になるようにコントロールする。定量噴霧式吸入器 (MDI) によってうまく吸入できない高齢者や重度の気流制限を認められる場合は超音波ネブライザーを用いて吸入を行う。
- サルブタモール吸入液(ベネトリン他)0.3ml - 0.5ml (1.5mg - 2.5mg) を生理食塩水2mlと混ぜて吸入を行うことが多い。サルブタモールと生理食塩水の量、比に関しては十分量の吸入がされていれば治療効果に差はないとされており、ネブライザーの形状にあった量とすることが重要である。ネブライザーでもMDIと同様、20分毎3回の吸入を行い、少しでも効果が見られたら2時間まで20分毎の吸入を繰り返してよいとされている。
- 初期治療で改善が認められない場合や中等度以上の発作、あるいは窒息死のリスクファクターがある場合はさらにステロイドの点滴を追加する。
- メチルプレドニゾロン(ソルメドロール他)40mgを生理食塩水50mlに融解し30分の点滴投与やヒドロコルチゾン(ソルコーテフ他)200mgを生理食塩水50mlに融解し30分の点滴投与を行う。これらはコハク酸エステル型のステロイド剤であるためNSAIDsにて喘息が誘発される場合や鼻疾患の合併がある場合はベタメタゾン注(リンデロン他)4mg - 6mgやデキサメタゾン注(デカドロン他)6mgに変更した方が安全である(経口ステロイドではこのようなことは注意する必要はない)。
- ステロイド投与を行い2時間経過しても改善が認められない場合は入院の適応になる。
- 十分な効果が得られず、呼吸困難が持続する場合はアドレナリン(ボスミン)0.3mgの皮下注を行う。同剤の適応は45歳以下で、高血圧、虚血性心疾患、不整脈、頻脈がない場合である。20分毎に反復投与を行ってよいが血圧、脈拍、動悸、振戦に注意が必要である。心拍数を130bpm以下に保つために心電図モニタリングが必要である。アドレナリンを使用する症例では気管挿管が必要となる場合もあるため、準備を行う。なお、エピネアドレナリンは子宮動脈の収縮作用があるため妊婦の場合はテルブタリン(ブリカニール他)0.2mgの皮下注に変更する。オプションとして経気道的な気管支拡張薬投与が不可能な場合はテオフィリン製剤の点滴を考慮する。アミノフィリン6mg/kgを5%ブドウ糖液250mlで希釈し半量を15分で残りを45分で点滴静注するのが一般的である。
- 軽症〜中等症では無効とされているが重症喘息ではマグネシウムを1g - 2g(マグネゾール2g/20mlまたはコンクライトMg1Aやアミサリン100mg/1ml)の静注はステロイドやSABAが使用されたうえでは効果が認められる。
- 後療法
- 発作が中等度以上であった場合は経口プレドニゾロン15mgを一日二回5日分ほど処方し、近日中に専門医やかかりつけ医の受診を促す。MDIが十分に残っていることを確認する。発作が中等度でも1時間以内に改善した場合は帰宅可能であるが、軽度でも窒息死のリスクファクターがある場合は入院治療が必要である。
- 気管挿管の適応
- 初期治療を行ったにもかかわらず、呼吸減弱、呼吸停止や意識障害が認められたり、酸素投与下でもPaO2が50Torr以下やPaCO2が50Torr以上やpHが7.25以下、不整脈の頻発の場合は気管内挿管を行い、入院治療を行う。
- 入院の適応
- 入院が必要な場合としては、中等度以上の発作であり、気管支拡張薬やステロイド全身投与にもかかわらず2時間経過しても反応がない場合や治療後でも酸素飽和度90%以下の低酸素状態が継続する場合、治療後もPEF値が60%未満の場合や、窒息死のハイリスクグループである場合などがあげられる。入院では酸素療法の継続、気管支拡張薬吸入の継続(サルブタモール吸入液の吸入を4時間毎、20分以上あけて追加投与可能)、その他メチルプレゾニドロン60mgを1日3回ほど点滴静注する。テオフィリン製剤を用いる場合もある。喘息の治療に影響を与える因子としては感染症、鼻炎、副鼻腔炎、アレルギー性鼻炎、鼻ポリープ、GERD、薬物(βブロッカーやACEI)、アレルギー、喫煙、声帯機能不全(夜間に症状がないのに早朝急に嗄声などの症状が出現する)をはじめとする心因性疾患などがありこれらも可能な限り治療を行っていく。コントローラーのステップアップにて症状が安定し、他疾患の除外ができれば退院となる。
喘息死の危険因子
編集これらのリスクファクターがある患者はより慎重な治療が求められる。
- ステロイド薬の全身投与中または中止したばかりである。
- 過去一年間に喘息発作による入院または救急外来受診した。
- 喘息発作で気管内挿管や人工呼吸管理を必要とした。
- 短時間作用性β2刺激薬を月に2本以上と過剰使用している。
- 鎮静薬を使用している。
- 喘息の治療計画に従わない。
気管支喘息と鑑別を要する疾患
編集- 慢性閉塞性肺疾患(Chronic Obstructive Pulmonary Disease:COPD)
- 非喫煙者や、特異的遺伝子変異をもつ若年者に発症することもあるが、多くは、高齢者に発症し、喫煙との関連が強い。労作時の呼吸困難、息切れ、β2刺激剤の吸入後の1秒率が70%未満であること、胸部画像診断における気腫性変化等が重要であるが、軽症例では、所見に乏しいこともある。喘息、COPDにおいて、典型例では、病態を形成する炎症性細胞、サイトカイン、ケモカインなどのprofileに対照的な特徴が認められるが、非典型例では両者の差異が不明瞭となり、しばしば、鑑別困難となる。両者の合併例も少なくなく、近年、ACO(Asthma COPD Overlap)という概念が提唱されている。喘息と同様に、急性増悪(喘鳴、呼吸困難などの増強)を来しうる疾患であり、気道感染や心不全が誘因となる。従来、喘息よりも気管支拡張剤に対する反応が悪く、気道可逆性の有無が両者の鑑別において有用とされてきたが、近年では、典型的な喘息と同様の気道可逆性を示すCOPD症例が報告されている。
- アレルギー性気管支肺アスペルギルス症(Allergic BronchoPulmonary Aspergillosis:ABPA)
- 気管支喘息患者の1%程度にみられると報告される。真菌の一つであるアスペルギルスに対するアレルギーによりおこり、喀痰中の粘液栓、中枢性気管支拡張、X線写真における肺浸潤影などを特徴とする。
- 好酸球性多発血管炎性肉芽腫症(チャーグストラウス症候群)
- 気管支喘息患者の5,000人に1人程度に発症すると報告される。病気の本体は全身の小動脈〜細動脈の炎症(血管炎)であり、発熱、手足のしびれ(末梢神経炎)、筋肉痛、関節痛など多彩な症状を呈する。一過性の肺浸潤影が認められることもある。ロイコトリエン拮抗薬との関連が指摘されているが、否定的な報告もある。
- ブロンコレア(気管支漏)
- 卵の白身のような外観を呈した喀痰を1日に100ml以上、難治時に喀出する病態。患者はかなりの苦痛を伴うがほとんどの場合心理的なものと判断され、診断も治療も受けられず難治化していく。専門医による適切な診断と専門医の下での治療が必要。喘息にブロンコレアが合併すると難治性喘息に移行することが多い。
脚注
編集注釈
編集- ^ 直訳では一つの気道に一つの病気がある。
出典
編集- ^ Gong, Henry (1990), Walker, H. Kenneth; Hall, W. Dallas, eds., Wheezing and Asthma (3rd ed.), Butterworths, ISBN 978-0-409-90077-4, PMID 21250199 2023年10月26日閲覧。
- ^ “吸気性喘鳴(stridor) - 05. 肺疾患”. MSDマニュアル プロフェッショナル版. 2023年10月26日閲覧。
- ^ Marketos SG, Ballas CN. Bronchial asthma in the medical literature of Greek antiquity. J Asthma. 1982;19(4):263-9. PMID 6757243, doi:10.3109/02770908209104771。
- ^ Q9-4 たばこの煙で発作が起こることがありますか?
- ^ 小田嶋博, 「喫煙の気管支喘息への影響」『日本小児アレルギー学会誌』 2005年 19巻 3号 p.237-246, 日本小児アレルギー学会, doi:10.3388/jspaci.19.237, NAID 10020563061。
- ^ 萱場広之, 「2 稲作地域における環境因子と気管支喘息 : 穀物粉塵と野焼きを中心に(化学物質過敏症の診断・治療と問題点)」『アレルギー』 2004年 53巻 2-3号 p.224-, 日本アレルギー学会, doi:10.15036/arerugi.53.224_1, NAID 110002432669。
- ^ 線香の煙の吸入が喘息を悪化させる可能性を示唆 九州大学 - 大学ジャーナルオンライン — Mozilla Firefox
- ^ 火山噴火 その時どうする?|災害列島 命を守る情報サイト|NHK NEWS WEB — Mozilla Firefox
- ^ Gruzieva O, Gehring U, Aalberse R, et al. (2014). “Meta-analysis of air pollution exposure association with allergic sensitization in European birth cohorts”. J. Allergy Clin. Immunol. 133 (3): 767-76.e7. doi:10.1016/j.jaci.2013.07.048. PMID 24094547.
- ^ a b Hosseini B, Berthon BS, Wark P, Wood LG (2017). “Effects of Fruit and Vegetable Consumption on Risk of Asthma, Wheezing and Immune Responses: A Systematic Review and Meta-Analysis”. Nutrients 9 (4). doi:10.3390/nu9040341. PMC 5409680. PMID 28353635.
- ^ Seyedrezazadeh E, Moghaddam MP, Ansarin K, Vafa MR, Sharma S, Kolahdooz F (2014). “Fruit and vegetable intake and risk of wheezing and asthma: a systematic review and meta-analysis”. Nutr. Rev. 72 (7): 411-28. doi:10.1111/nure.12121. PMID 24947126.
- ^ a b 国立研究開発法人 国立成育医療研究センター
- ^ Nurmatov U, Devereux G, Sheikh A (2011). “Nutrients and foods for the primary prevention of asthma and allergy: systematic review and meta-analysis”. J. Allergy Clin. Immunol. 127 (3): 724-33.e1-30. doi:10.1016/j.jaci.2010.11.001. PMID 21185068.
- ^ Nagel G, Weinmayr G, Kleiner A, Garcia-Marcos L, Strachan DP (2010). “Effect of diet on asthma and allergic sensitisation in the International Study on Allergies and Asthma in Childhood (ISAAC) Phase Two”. Thorax 65 (6): 516-22. doi:10.1136/thx.2009.128256. PMID 20522849.
- ^ Bartley J, McGlashan SR (2010). “Does milk increase mucus production?”. Med. Hypotheses 74 (4): 732-4. doi:10.1016/j.mehy.2009.10.044. PMID 19932941.
- ^ Takkouche B, González-Barcala FJ, Etminan M, Fitzgerald M (2008). “Exposure to furry pets and the risk of asthma and allergic rhinitis: a meta-analysis”. Allergy 63 (7): 857-64. doi:10.1111/j.1398-9995.2008.01732.x. PMID 18588551.
- ^ Linehan MF, Nurmatov U, Frank TL, Niven RM, Baxter DN, Sheikh A (2014). “Does BCG vaccination protect against childhood asthma? Final results from the Manchester Community Asthma Study retrospective cohort study and updated systematic review and meta-analysis”. J. Allergy Clin. Immunol. 133 (3): 688-95.e14. doi:10.1016/j.jaci.2013.08.007. PMID 24084077.
- ^ Lambert KA, Bowatte G, Tham R, et al. (2017). “Residential greenness and allergic respiratory diseases in children and adolescents - A systematic review and meta-analysis”. Environ. Res. 159: 212-221. doi:10.1016/j.envres.2017.08.002. PMID 28803150.
- ^ 気管支ぜんそく/咳ぜんそく 日本医科大学呼吸ケアクリニック
- ^ せき(咳)・たん・ぜんそく(気管支ぜんそく)について アスゲン製薬
- ^ Jenkins, C; Costello, J; Hodge, L (2004), “Systematic review of prevalence of aspirin induced asthma and its implications for clinical practice”, BMJ 328: 434-439, PMID 14976098full text
- ^ Beasley R. "The global burden of asthma report. Global initiative for ashma(GINA)" 2004
- ^ 平成8年度厚生省長期慢性疾患総合研究事業
- ^ 日本アレルギー学会喘息ガイドライン専門部会監修『喘息予防・管理ガイドライン2006』協和企画、2006年、22頁。
- ^ Busse WW, and others. Combined Analysis of Asthma Safety Trials of Long-Acting β2-Agonists. N Engl J Med 2018; 378:2497-2505 DOI: 10.1056/NEJMoa1716868
- ^ 長屋宏、「日本のアレルギー診療は50年遅れている」、メディカルトリビューン社。ISBN 978-4-89589-336-7
- ^ Bousquet J, Lockey R, Malling HJ. (Oct 1998). “Allergen immunotherapy: therapeutic vaccines for allergic diseases. A WHO position paper”. J Allergy Clin Immunol. 102 (4 Pt 1): pp.749-794.PMID 9802362
- ^ スーパークレソン
- ^ 県産野菜の機能性評価(山梨県) (PDF)
- ^ One airway One disease 葛西よこやま内科・呼吸器内科クリニック 2022年3月10日閲覧。
参考文献
編集- EBMに基づいた喘息治療ガイドライン2004 厚生科学研究班編 ISBN 4877940634(Minds医療情報サービス)
- 小児気管支喘息治療・管理ガイドライン2020 ISBN 9784877942052 一般社団法人日本小児アレルギー学会
- アレルギー総合ガイドライン2019 ISBN 9784877942069 日本アレルギー協会
- 喘息予防・管理ガイドライン〈2018〉ISBN 9784877941932 日本アレルギー学会 喘息ガイドライン専門部会
- レジデントのためのアレルギー疾患診療マニュアル ISBN 4260001450
- レジデントのための呼吸器診療マニュアル ISBN 9784260005630
- Dr.岡田のアレルギー疾患大原則(第3巻) ISBN 4903331776
- 内科レジデントマニュアル 第6版 ISBN 4260001981
関連人物
編集関連項目
編集外部リンク
編集- 日本呼吸器学会
- 喘息(ぜんそく)の症状・原因 - くすりと健康の情報局
- The Global Initiative for Asthma(GINA)
- 喘息 - MSDマニュアル
- 『気管支喘息』 - コトバンク